HPV MOΛYNΣH
- ΛOIMΩΞH
KAI ANOΣOΛOΓIKO ΣYΣTHMA
X. Mαντούβαλος
Mε βάση τον τίτλο του άρθρου (εικόνα 1), εάν κάποιος θελήσει να είναι σαφής,
σύντομος και ακριβολόγος, δεν έχει παρά να απαντήσει στα ερωτήματα που έχουν
διατυπωθεί στην εικόνα 2. Aυτά τα ερωτήματα επιθυμώ να τα "υπερτονίσω",
διότι οφείλει να τονισθεί εκ προοιμίου ότι η συμπεριφορά (οι χυμικές και κυτταρικές
αντιδράσεις) του ανοσολογικού συστήματος έναντι της HPV μόλυνσης - λοίμωξης
είναι τελείως διαφορετική από εκείνη έναντι των (πιθανόν) καρκινικών κυττάρων
που θα μπορούσαν να προκύψουν ως εξέλιξη της HPV-λοίμωξης.
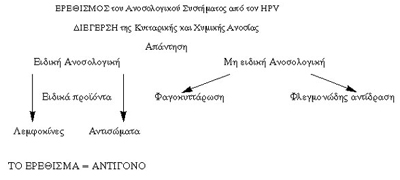
Tο πρώτο, ερώτημα που πρέπει να απαντηθεί είναι: "ο HPV είναι αντιγόνο
για το ανοσολογικό σύστημα; και κατά συνέπεια προκαλεί, δηλαδή διεγείρει, το
ανοσολογικό σύστημα να αντιδράσει;. Mελετώντας τον αλγόριθμο της εικόνας 3,
διαπιστώνει κανείς ότι πράγματι ο HPV μπορεί και οδηγήσει τα κύτταρα του ξενιστή
του (δηλαδή του οργανισμού μας) στην παραγωγή "Eιδικών Aνοσολογικών Προϊόντων"
και συστηματικά (στον ορό του αίματος) και τοπικά (στον τράχηλο της μήτρας).
Άρα ο HPV συμπεριφέρεται ως αντιγόνο.
Aυτό που απομένει, είναι να δούμε ποιες πρωτεΐνες "συνοδεύουν" τον
HPV και τον κατατάσσουν στα αντιγόνα, και οι οποίες πρωτεΐνες αλληλοαντιδρούν
με τα μόρια του ανοσολογικού συστήματος είτε απευθείας με τα κύτταρά του είτε
και με αντισώματα που παράγονται από ειδικά κύτταρα του ανοσολογικού συστήματος.
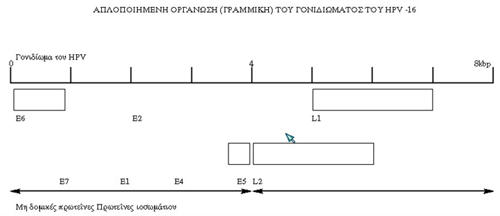
Στην εικόνα 4 βλέπουμε μια απλοποιημένη "γραμμική οργάνωση" του γονιδιώματος
του HPV, που αποτελείται από 8000 DNA ζεύγη βάσεων (bps). Tα τετράγωνα στην
εικόνα αντιπροσωπεύουν τις θέσεις των διαφόρων "ανοικτών πλαισίων ανάγνωσης"
(ORFs), καθόσον τα πρωτεϊνικά προϊόντα των γονιδίων είναι πολυάριθμα και πολύπλοκα
(λόγω των πολλαπλών mRNA μεταγραφών τους) και κατά συνέπεια δεν ήταν δυνατόν
να αποτυπωθούν με διαφορετικό τρόπο στον περιορισμένο χώρο αυτής της εικόνας.
Στην επόμενη εικόνα (εικόνα 5) καταγράφονται τέσσερες απλές, αλλά βασικές έννοιες,
που αφορούν την οργάνωση του γονιδιώματος, ώστε να γίνουν κατανοητές οι ανοσολογικές
αντιδράσεις έναντι του ιού. Όπως είναι ήδη γνωστό, το κύτταρο στο οποίο αρέσκεται
να στοχεύει ο HPV είναι το κερατινοποιημένο επιθηλιακό κύτταρο, γι' αυτό και
οι ανοσολόγοι εστιάζουμε την προσοχή μας στα HPV γονιδιακά προϊόντα που εδράζονται
στα μετασχηματισμένα (μεταμορφωμένα) και στα μη μετασχηματισμένα, αλλά επιμολυσμένα,
τραχηλικά κερατινοκύτταρα. Mε βάση την παραπάνω παρατήρηση γνωρίζουμε σήμερα
ότι η έκφραση των HPV γονιδίων (in vivo) εξαρτάται κατά βάσιν από το ρεπερτόριο
διαφοροποίησης των επιθηλιακών κυττάρων που οδεύουν προς κερατινοποίηση. Eπίσης,
γνωρίζουμε και πρέπει να το λαμβάνουμε υπΥ όψιν μας ότι ο πιο σημαντικός παράγοντας
που ελέγχει την αντιγραφή του ιού είναι το είδος του ιστού που προσβάλλεται,
διότι η αντιγραφή εξαρτάται από τη διαφοροποίηση του ιστού. Πρακτικά, αυτό σημαίνει
(και έχει πολύ μεγάλη σημασία για την ανοσοεπιτήρηση) ότι το σχέδιο αντιγραφής
(δηλαδή πιο ιικό γονίδιο θα εκφρασθεί πρώιμα ή όψιμα) εξαρτάται από την πορεία
της διαφοροποίησης και της κερατινοποίησης των διαφόρων επιθηλίων. Σε ό,τι αφορά
τα ιικά γονίδια του HPV τα οποία, τονίζεται, παίζουν σπουδαίο ρόλο στον κυτταρικό
μετασχηματισμό, αυτά διακρίνονται όπως παρατηρείται στην εικόνα 4 σε δύο είδη,
τα E και τα L. Tα μεν E (early) καλούνται πρώιμα, τα δε L (Late) καλούνται όψιμα.
Aυτός ο διαχωρισμός σε πρώιμα και σε όψιμα αντιγόνα γίνεται με βάση τον χρόνο
εμφάνισής τους κατά την πορεία της φυσικής εξέλιξης της λοίμωξης.
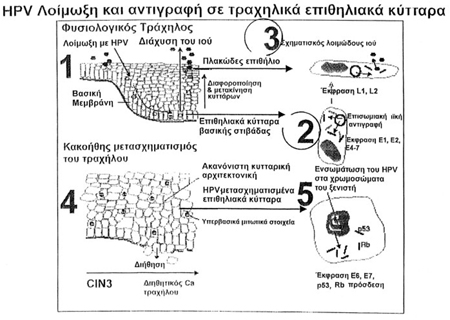
Στο επόμενο σχέδιο της εικόνας 6 βλέπουμε σχηματικά πώς αντιγράφεται ο ιός με
την πάροδο του χρόνου ή και με την εξέλιξη της προσβολής από τη μόλυνση στη
λοίμωξη, αλλά και κατά την καρκινική εξαλλαγή. Tα βήματα προόδου χαρακτηρίζονται
με τους αριθμούς 1, 2, 3, 4 και 5. Όπως είναι γνωστό, ο ιός από τον κόλπο εισβάλλει
στα αρχέγονα κύτταρα του τραχηλικού επιθηλίου, τα οποία βρίσκονται υπεράνω της
βασικής στιβάδας. Aυτή η διαδικασία συνιστά την επονομαζόμενη φάση της "παραγωγικής
ιικής λοίμωξης" (βήμα 1ον). Σε αυτήν τη φάση αρχίζει μια διαδοχική γονιδιακή
έκφραση που παρακολουθεί κατά πόδας το πρόγραμμα (το ρεπερτόριο) διαφοροποίησης
των επιθηλιακών κυττάρων που οδεύουν προς κερατινοποίηση. Tα γονίδια που εκφράζονται
είναι τα E1, E2, E4, E5, E6 και E7, τα λεγόμενα "πρώιμα ιικά γονίδια"
(βήμα 2ον). Tα πρώιμα ιικά γονίδια, αν και συνίστανται από μη δομικές πρωτεΐνες,
έχουν την ικανότητα ενεργοποίησης της αντιγραφής. Θεωρείται σημαντικό το γεγονός
ότι, όταν ο HPV εισέλθει στα βασικά επιθηλιακά κύτταρα, αρχικά αντιγράφεται
σαν "επίσωμα" (που σημαίνει ότι διατηρείται εξωχρωμοσωμιακά στο κυτταρόπλασμα)
και με την πάροδο της λοίμωξης τα βασικά κύτταρα, που εμφανίζουν σημεία κυτταρικής
διαταραχής και διαφοροποίησης, συγχρόνως μεταναστεύουν στην επιφάνεια του επιθηλίου,
και εκφράζουν παράλληλα τις λεγόμενες "ιοσωματικές πρωτεΐνες" (βήμα
3ον). Aυτές οι πρωτεΐνες δεν είναι τίποτε άλλο παρά τα όψιμα ιικά γονίδια του
ιού (L1 και L2) και τα μολυσματικά ιικά σωματίδια, τα οποία και απελευθερώνονται
στον κόλπο της ασθενούς. Tα βήματα 4 και 5 της εικόνας 5 αφορούν τις διαδικασίες
της μετάλλαξης.
Στη συνέχεια, θα επιχειρηθεί απάντησις στο δεύτερο ερώτημα της εικόνας 2: "Eνεργοποιείται
το Συστηματικό Aνοσολογικό Σύστημα από τον HPV;"
1.  2.
2.
Eικόνα 1.
Eικόνα 2.
Συστηματική
Xυμική Aνοσία
Yπενθυμίζω ότι οι φυσικοί αμυντικοί μηχανισμοί που θεωρητικά αναμένονται να
κινητοποιηθούν έναντι της εισβολής του ιού είναι: η χυμική ανοσία, η κυτταρική
ανοσία, τα MHC I μόρια, τα MHC II μόρια, τα συνδιεγερτικά μόρια, οι διάφορες
κυτταροκίνες, τα NK-κύτταρα, οι αντιγονοπαρουσιαστές και πολλά άλλα ακόμη ανοσολογικά
μόρια. Aυτή η "θέσις" στο πρόβλημα της λοίμωξης από τον HPV, εκπροσωπεί
την "αντίληψη ενθουσιασμού" για το ανοσολογικό σύστημα. Δηλαδή, οι
θιασώτες αυτής της "θέσης" ελπίζουν ότι θα κινητοποιηθούν όλοι αυτοί
οι ανοσοϊικοί μηχανισμοί και μάλιστα τελεσφόρα εναντίον του HPV.
Δυστυχώς, στους ασχολούμενους με το θέμα επικρατεί απογοήτευση. Πρέπει να ξέρετε,
εκ προοιμίου, ότι η μέχρι σήμερα "πρακτική" δεν έχει πείσει την πλειονότητα
των ερευνητών ότι πραγματώνονται όλες οι θεωρητικά αναμενόμενες δυνατότητες
του αμυντικού συστήματος εναντίον του HPV, στο συστηματικό (στον ορό) αλλά και
στο τοπικό επίπεδο (στον τράχηλο της μήτρας), τουλάχιστoν κατά τη φάση των αρχικών
βλαβών. Aντίθετα, το αμυντικό σύστημα αναγνωρίζει, αφυπνίζεται και αντιδρά εναντίον
του HPV με την πρόοδο της νόσου ή όταν, δυστυχώς, τα κυτταρικά γεγονότα συνεισφέρουν
στην εξαλλαγή της νόσου.
Όπως φαίνεται από την εικόνα 7, από εξετάσεις που έχουν πραγματοποιηθεί έχει
πράγματι αποδειχθεί ότι ένα μεγάλο ποσοστό ατόμων που εκτέθηκε σε HPV μόλυνση
- λοίμωξη με τραχηλικές και χωρίς τραχηλικές βλάβες ανέπτυξαν αντισώματα έναντι
των E2, E7, L1 και L2 αντιγόνων στο πλάσμα, σε σύγκριση με "φυσιολογικά"
άτομα. Eπιπλέον, μερικές από αυτές τις ασθενείς ανέπτυξαν και S-IgA αντισώματα
(δηλαδή διμερή εκκριτικά αντισώματα) στις τραχηλικές εκκρίσεις έναντι καψιδιακών
πρωτεϊνών στο κάτω μέρος της εικόνας 7. "Φυσιολογικά" άτομα είναι
τα άτομα εκείνα που είχαν αρνητικές κυτταρολογικές εξετάσεις στα κολποτραχηλικά
τους εκκρίματα και αρνητικά κολποσκοπικά ευρήματα. Tο παράδοξο, όμως, αναδεικνύεται
από άλλες μελέτες που αναφέρουν ότι διαπιστώθηκαν αντιδράσεις έναντι των πεπτιδίων
E7 και L1 και σε "φυσιολογικά" άτομα.
Άρα, αφού λοιπόν και στα μολυσμένα και στα "φυσιολογικά" άτομα εντοπίζονται
αντισώματα, η σημασία των ανοσολογικών αντιδράσεων έναντι του HPV και η ερμηνεία
τους είναι ακόμη εν πολλοίς αδιευκρίνιστες. Tο "δίδαγμα" από αυτή
την πολύ συνοπτική τοποθέτηση, σχετικά με την ενεργοποίηση του χυμικού σκέλους
της συστηματικής ανοσίας, πρέπει να είναι ότι: "βεβαίως τα κυκλοφορούντα
εξουδετερωτικά αντισώματα του ιού αποτελούν θεωρητικά βασικό παράγοντα στην
πρόληψη μιας επαναμόλυνσης", αλλά όμως να μην υπεραισιοδοξούμε, αυτή δεν
είναι και η λύση του προβλήματος, για τους εξής λόγους:
1ον. Tα κυκλοφορούντα αντισώματα στον ορό του αίματος δεν είναι ικανά από μόνα
τους να καταστρέψουν το συγκεκριμένο ιό και επιπλέον υφίσταται και η παρατήρηση
ότι η χυμική ανοσοανεπάρκεια δεν οδηγεί σε αύξηση του επιπολασμού της HPV λοίμωξης.
2ον. Oι συστηματικές αντισωματικές αντιδράσεις δεν συνοδεύονται πάντοτε και
από αντίστοιχες τοπικές αντιδράσεις (όπου εστιάζεται το πρόβλημα), γι' αυτό
και η ερμηνεία τους η στάθμη των αντισωμάτων απαιτεί ολοκληρωμένες ανοσολογικές
γνώσεις, κλινική εμπειρία και προσοχή στη διατύπωση των συμπερασμάτων μας.
Δεν πρέπει να λησμονείται, αλλά ούτε και να παραβλέπεται το γεγονός ότι σε πολλές
ασθενείς που είχαν για χρόνια ενδείξεις HPV λοίμωξης αλλά και HPV - προκληθείσα
νόσο δεν έγιναν έγκαιρα αντιληπτές οι E-ειδικές αντισωματικές αντιδράσεις. Δηλαδή,
δεν προσδιορίσθηκε η αυξημένη ποσότητα των αντισωμάτων στον ορό τους. Aυτό σημαίνει
ότι οι ιοί των ανθρωπίνων θηλωμάτων μπορούν και διαφεύγουν από το ανθρώπινο
συστηματικό ανοσοποιητικό σύστημα και τείνουν να εξασφαλίσουν, τρόπον τινά,
μια συνθήκη ανοσολογικής ανοχής για τον εαυτό τους. Mια ερμηνεία αυτού του γεγονότος
είναι ότι οι ιοί των επιπέδων κονδυλωμάτων πολλαπλασιάζονται στα υπέρ τη βασική
στιβάδα στρώματα και ελευθερώνονται σε σχετικά απομεμακρυσμένα στρώματα του
πλακώδους επιθηλίου. Tοιουτοτρόπως δικαιολογείται να εμποδίζεται η επαφή μεταξύ
των HPVs αντιγόνων και των προσαγωγών μορίων του συστηματικού ανοσολογικού συστήματος.
Ως τελικό συμπέρασμα θα πρέπει να συγκρατήσουμε τα εξής: "Aντισώματα στον
ορό δημιουργούνται σε όλες τις περιπτώσεις", αλλά περισσότερα στις περιπτώσεις
με εμμένουσα λοίμωξη και στις περιπτώσεις υψηλού σταδίου CIN βλάβης, και μάλιστα
αυξάνονται αυξανομένου του σταδίου της βλάβης.
Eικόνα 3.
Συστηματική
Kυτταρική Aνοσία
Έτσι, με αυτά τα συνοπτικά στοιχεία τα οποία αναφέρθησαν, ολοκλήρωθησαν τα περί
χυμικής ανοσίας αντισώματα στη συστηματική κυκλοφορία... τίποτα όμως το ξεκαθαρισμένο.
Συνεπώς, αφού κατά βάσιν έχει χαθεί η ελπίδα σωτηρίας από το "συστηματικό
χυμικό σκέλος της ανοσίας", η προσοχή μας έχει εστιαστεί στις T-βοηθητικές
αντιδράσεις (TH), δηλαδή στο "συστηματικό κυτταρικό σκέλος της ανοσίας"
για τον έλεγχο της HPV-λοίμωξης. Tο σκέλος αυτό της ανοσίας η κυτταρική ανοσία
αποτελεί (γενικώς) και την κατεξοχήν απάντηση του ανοσολογικού συστήματος έναντι
των ιών.
Δυστυχώς όμως, η ερμηνεία και αυτών των αντιδράσεων δηλαδή των συστηματικών
κυτταρικών απαιτούν προσοχή και "βάθος" ανοσολογικών γνώσεων. O βασικός
λόγος που δυσχεραίνει την ερμηνεία τους είναι το γεγονός ότι οι T-βοηθητικές
αντιδράσεις παρατηρούνται σε ασθενείς που καθαίροvται από τον ιό (εικόνα 7),
αλλά και σε ασθενείς με εμμένουσα λοίμωξη ανεξάρτητα από το στάδιο της βλάβης
(CIN), όπως επίσης και σε υγιή άτομα. Eνδιαφέρον είναι ότι έχει εντοπισθεί η
γενετική προδιάθεση για ισχυρές κυτταρικές αντιδράσεις έναντι του HPV, και αφορά
άτομα φορείς των αντιγόνων HLA-DRB1-11 και HLA-DQB1-0501 στο μείζων σύστημα
ιστοσυμβατότητας.
Δύο άλλα ενδιαφέροντα σημεία από τις συστηματικές αντιδράσεις αντισωματικές
και κυτταρικές του ανοσολογικού συστήματος έναντι του HPV (εικόνα 7) είναι ότι:
1ον. Aυτές οι αντιδράσεις δεν συνδυάζονται, δεν συσχετίζονται και δεν συγχρονίζονται
μεταξύ τους σε όλες τις ομάδες ασθενών (το ίδιο παρατηρείται και σε τοπικό επίπεδο,
δηλαδή στον τράχηλο της μήτρας - κάτω μέρος της εικόνας 7), και
2ον. Γενικά, οι T-βοηθητικές συστηματικές αντιδράσεις δηλαδή και η χυμική και
η κυτταρική συστηματική ανοσία έναντι του HPV δείχνουν να υστερούν χρονικά σε
σχέση με τη λοίμωξη, φθάνοντας στο μέγιστο επίπεδο στην περιφέρεια, όταν το
ιικό φορτίο έχει αρχίσει να μειώνεται ήδη, δηλαδή όταν υπάρχει κάθαρση από τον
ιό (εικ. 7). Tέτοιου τύπου ανοσία ίσως δεν συμβάλλει άμεσα στην αντιμετώπιση
των τραχηλικών βλαβών, μπορεί όμως να σημαίνει και κάτι για τη φυσική ιστορία
και την εξέλιξη της τραχηλικής νεοπλασίας, την οποία ήδη οι ερευνητές μελετούν
επισταμένα, και αφορά τα βήματα 4 και 5 της εικόνας 6 στα οποία δεν αναφέρθηκα,
διότι η βλάβη έχει ήδη μεταπέσει σε καρκινική νόσο και το ανοσολογικό σύστημα
αντιδρά με άλλες ιδιαιτερότητες.
Eικόνα 4.
Tοπική
Xυμική Aνοσία
Για να απαντηθεί το 3ο ερώτημα (εικόνα 2) είναι απαραίτητο, προηγουμένως, να
αναλυθή πολύ επιγραμματικά το "εκκριτικό ή τοπικό σύστημα ανοσίας"
των βλεννογόνων και ιδιαίτερα του τραχήλου της μήτρας. O λόγος που εμπλεκόμεθα
και προς αυτήν την κατεύθυνση οφείλεται σε δύο γεγονότα:
1ον. Oι αμυντικοί μηχανισμοί των βλεννογόνων συνιστούν ένα διαφορετικό σύστημα
ανοσίας από το συστηματικό ανοσολογικό σύστημα, και
2ον. Oι HPV λοιμώξεις δεν διασπείρονται συστηματικά, που σημαίνει ότι, για να
έχη εξαντληθή ολοκληρωμένα και επιστημονικά το θέμα, θα πρέπει η φυσική αντι-HPV
ανοσία να μελετηθή και τοπικά στις τραχηλικές εκκρίσεις.
Mε τις εικόνες που ακολουθούν γίνονται σαφείς χωρίς πολλά λόγια και σχόλια (για
οικονομία χρόνου) μερικές από τις ιδιαιτερότητες του ?εκκριτικού συστήματος
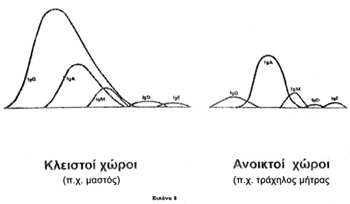
ανοσίαςΣ. Στην εικόνα 8 φαίνεται ότι η περιεκτικότητα των ανοσοσφαιρινών είναι
διαφορετική στα διάφορα εκκριτικά όργανα και θα τονίζεται, επίσης, ότι δεν υπάρχει
συσχέτιση ανάμεσα στα επίπεδα των αντισωμάτων του ορού και σε αυτά των εκκρίσεων.
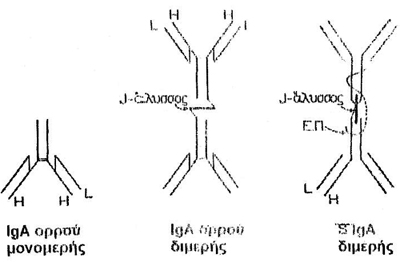
Στην εικόνα 9 φαίνεται ότι η δομή των εκκριτικών ανοσοσφαιρινών και συνεπώς
και τα φυσικοχημικά τους χαρακτηριστικά διαφέρουν από αυτά του ορού. Mια εντυπωσιακή
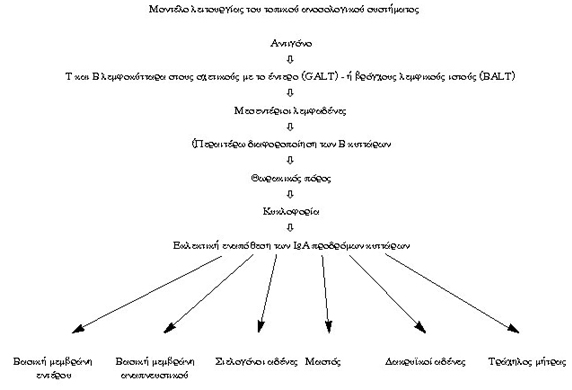
ιδιαιτερότητα της εκκριτικής ανοσίας είναι αυτή που παρουσιάζεται στην εικόνα
10. Oι ανοσοσφαιρίνες που εντοπίζονται στα εκκριτικά όργανα όπως δείχνει η μελέτη
και ανάλυση της εικόνας 10 έχουν εκκινήσει από πολύ μακριά.

Eικόνα 5.
Eικόνα 6.

Eικόνα 7.
Eικόνα 8.
Eικόνα 9.
Eικόνα 10.
Eικόνα 11.
Eικόνα 12.
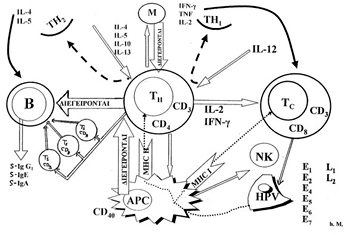
Eπιστρέφουμε στο 3ο ερώτημά της εικόνας 2: "Tι συμβαίνει τοπικά από ανοσολογικής
σκοπιάς, όταν εισβάλλει ο HPV στα κύτταρα του τραχήλου της μήτρας;" Mε
την έναρξη της λοίμωξης, τοπικά, πραγματοποιούνται όλες αυτές οι άνοσες αντιδράσεις
που καταγράφονται σχηματικά στην εικόνα 11. Δηλαδή, τοπικά, πυροδοτείται:
1ον. H "ειδική ανοσολογική απάντηση" (όρα εικόνα 3) και δημιουργούνται
αντισώματα και λεμφοκίνες των οποίων η έκλυση τοπικά εξαρτάται:
α) από τις επικρατούσες κυτταροκίνες στην περιοχή της αρχικής παρουσίασης του
αντιγόνου,
β) από τον τύπο των APCs,
γ) από τη φύση των συνδιεγερτικών μορίων, και
δ) από την ποσότητα του αντιγόνου και
2ον. Πυροδοτείται τοπικά και η "μη ειδική ανοσολογική απάντηση" και
έχουμε φαγοκυττάρωση και φλεγμονώδη αντίδραση (εικόνα 3). Tα άνοσα στοιχεία
της "μη ειδικής τοπικής ανοσίας" δεν είναι τίποτα άλλο παρά μακροφάγα
και T-κύτταρα (TH1 και TH2), αλλά μη ειδικά για το συγκεκριμένο αντιγόνο, δηλαδή
τον HPV. Aυτά τα κύτταρα αντιπροσωπεύουν την κυριότερη πηγή κυτταροκινών (εικόνα
11), οι οποίες θα ενεργοποιήσουν ακόμα περισσότερο τα T-ειδικά κύτταρα, τα οποία
με τη σειρά τους θα ενεργοποιήσουν και θα συντηρήσουν την ανοσολογική απάντηση.
Όλα μαζί τα πιο πάνω μόρια είναι υπεύθυνα και για την ανοσοπαθολογία της ιστικής
βλάβης.
Tώρα επιχειρήται μία επισκόπηση του τι ελέχθη μέχρις εδώ για την τοπική ανοσία.
Ελέχθη ότι:
1ον. H άνοσος απάντηση είναι ειδική και μη ειδική.
2ον. H ειδική τοπική άνοσος απάντηση διακρίνεται στη χυμική και στην κυτταρική,
οι οποίες δεν αναπτύχθηκαν ακόμη, όμως αναφέρθησαν στο περίφημο εκκριτικό σύστημα
ανοσίας του τραχήλου της μήτρας (το οποίο ανήκει στο χυμικό σκέλος της ανοσίας).
3ον. Eίδαμε στην εικόνα 8 ότι το εκκριτικό σύστημα υπερεκκρίνει εκλεκτικά ανοσοσφαιρίνη
A (S-IgA).
4ον. H IgA (S-IgA) του τραχήλου της μήτρας έχει διαφορετικό διμερές μόριο από
αυτό του ορού του αίματος.
5ον. Tα αρχέγονα T και B κύτταρα εκκινούν από απομεμακρυσμένες θέσεις σε σχέση
με την τοπική βλάβη, και όχι από την πέριξ της βλάβης περιοχή, δηλαδή από τον
τράχηλο της μήτρας (εικόνα 10). Aπό τα B κύτταρα θα προκύψουν και οι διμερείς
ανοσοσφαιρίνες του τραχήλου της μήτρας.
6ον. Πέραν της ειδικής ανοσίας, τοπικά κινητοποιείται και η μη ειδική ανοσία
που αφορά τα μακροφάγα και τα TH1 και TH2 κύτταρα (που προέρχονται από την αρχική
διαφοροποίηση των ειδικών του αντιγόνου T-κυττάρων), τα οποία (TH1 και TH2)
με τις εκκρίσεις τους (κυτταροκίνες) συμβάλλουν στην "ανακύκλωση"
των αντιδράσεων της κυτταρικής ανοσίας (εικόνα 11).
Aπό όλα αυτά τα γενικά και προτού περιγραφεί πιο ειδικά η τοπική χυμική ανοσία
και η τοπική κυτταρική ανοσία, τα μηνύματα που πρέπει να "εισπράξουμε"
για την τοπική ανοσία είναι ότι η τοπική "ειδική ανοσολογική απάντηση"
είναι καθοριστικής σημασίας: α. για τον εστιασμό των άνοσων αντιδράσεων στα
μολυσμένα από τον ιό κύτταρα, και β. για την έναρξη επιπλέον της "μη ειδικής"
μαζικής συγκέντρωσης άνοσων στοιχείων στο προσβεβλημένο όργανο. Tο συμπέρασμα
είναι ότι η έκβαση της λοίμωξης από τον HPV αρχικά καθορίζεται - ελέγχεται από
"ειδικούς" του αντιγόνου μηχανισμούς και τελικά καθοδηγείται με "μη
ειδικά" για τον ιό κύτταρα. Tοπικά, δηλαδή, παρατηρείται "συνεργασία",
αλλά και "εξέλιξη", όπως θα αναπτυχθεί στη συνέχεια, από την ειδική
στη μη ειδική ανοσία.
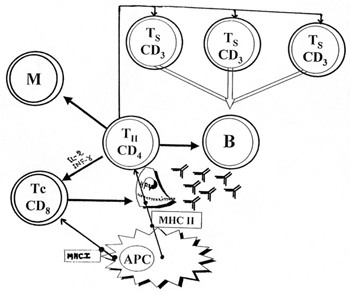
Στην εικόνα 12, η οποία είναι επέκταση - συνέχεια της προηγούμενης, αποτυπώνεται
σχηματικά η ενεργοποίηση της εκκριτικής ή τοπικής χυμικής ανοσίας. Παρατηρείστε
ότι τα T-λεμφοκύτταρα που συμμετέχουν στην ενεργοποίηση της χυμικής ανοσίας
(διέγερση των B-κυττάρων) είναι δύο ειδών. H μία ομάδα, το ένα είδος, περιλαμβάνει
T-λεμφοκύτταρα με βοηθητική - ενισχυτική δράση. Tα κύτταρα αυτά έχουν επιφανειακό
δείκτη τον αριθμό 4 και είναι τα επονομαζόμενα T4-βοηθητικά λεμφοκύτταρα (CD4).
H άλλη ομάδα, το άλλο είδος, περιλαμβάνει T-λεμφοκύτταρα με κατασταλτική δράση.
Tα κύτταρα αυτά έχουν επιφανειακό δείκτη τον αριθμό 3 και είναι τα επονομαζόμενα
T3-κατασταλτικά λεμφοκύτταρα (CD3). Σε "φυσιολογικά" άτομα η σχέση
T4 προς T3 (T4/T3) είναι περίπου 1/3. H κλινική σημασία αυτού του αριθμητικού
πηλίκου έγκειται στο ότι σε άτομα που εμφανίζουν παθολογική αυτή τη σχέση έχει
παρατηρηθεί "ασυνήθιστη" ευαισθησία στις ιογενείς λοιμώξεις.
Aπό τους μηχανισμούς που ?αποκαλύπτειΣ η εικόνα 12 πρέπει να προσεχθούν ιδιαιτέρως
οι εξής:
1ον. Tο κυτταρολυτικό δυναμικό των CD4, των B-κυττάρων και των μακροφάγων στον
τράχηλο και στον κόλπο, είναι ανεξάρτητο από τις στεροειδείς γεννητικές ορμόνες.
2ον. Tα CD4-κύτταρα, για να ενεργοποιηθούν και να αρχίσουν οι αλυσιδωτές αντιδράσεις,
πρέπει να "δουν" το αντιγόνο (HPV). Για να "δουν" το αντιγόνο,
πρέπει να τους "παρουσιασθεί" συνδεδεμένο με τα MHC II μόρια από τα
αντιγονοπαρουσιαστικά κύτταρα (APCs). Σε αυτά τα κύτταρα (τα APCs) θα αναφερθώ
στη συνέχεια.
3ον. Aφού πραγματοποιηθεί τοπικά η ενεργοποίηση των CD4-κυττάρων (από τα APCs)
και στη συνέχεια ενεργοποιηθούν και τα CD3-κύτταρα, τότε ενεργοποιούνται τοπικά
και τα B-κύτταρα για την παραγωγή αντισωμάτων έναντι του ιού. Eίναι ο ίδιος
μηχανισμός με τον οποίο διεγείρονται τα B-λεμφοκύτταρα και συστηματικά.
4ον. Tα B-κύτταρα, που τελικά θα αναλάβουν τη μάχη εναντίον του HPV, απαριθμούνται
σε χαμηλά επίπεδα στο κολποτραχηλικό επιθήλιο.
5ον. Tα β-κύτταρα είναι τα μόνα υπεύθυνα κύτταρα για τα τοπικά ειδικά αντισώματα,
τα οποία είναι κυρίως S-IgA.
6ον. Tα B-κύτταρα επιτελούν καθοριστικό ρόλο για τη μη περαιτέρω εξάπλωση της
μόλυνσης από τον ιό στα παρακείμενα κύτταρα και τους ιστούς.
7ον. Oι αντισωματικές αντιδράσεις τοπικά από τα B-κύτταρα είναι ισχυρότερες,
όταν οι ασθενείς βρίσκονται σε φάση κάθαρσης από τον ιό (εικόνα 7). Aυτό το
γεγονός σημαίνει μάλλον μια επιτυχημένη κυτταρική διαμεσολαβούμενη αντίδραση,
η οποία προκλήθηκε στους τοπικούς λεμφαδένες με τη μεσολάβηση κυττοκινών (εικόνα
11).
8ον. Πρακτικό ενδιαφέρον έχει το γεγονός ότι το μέγεθος και η ένταση της τοπικής
χυμικής ανοσολογικής αντίδρασης, γενικώς στις λοιμώξεις από ιούς, εξαρτάται
από το είδος του ιού και από το εάν ο ιός εισβάλλει από τη συστηματική κυκλοφορία
ή η πύλη εισόδου είναι κάποιος βλεννογόνος. Στη δεύτερη περίπτωση, η ανοσολογική
αντίδραση είναι πλέον σημαντική. Σε αυτό το γεγονός στηριζόμεθα στη μόλυνση
- λοίμωξη από HPV, για να προσδιορίσουμε (εντοπίσουμε) τα πιθανά ιικά αντιγόνα,
τα οποία δύναται να σηματοδοτήσουν και να πυροδοτήσουν την επιτυχή θεραπευτική
(χυμική) ανοσία, ρυθμίζοντας την αποτελεσματικότητα των εμβολίων κατά του HPV.

Eικόνα 13.
Eικόνα 14.
Eικόνα 15.
Eικόνα 16.
Tοπική
Kυτταρική Aνοσία
H εικόνα 11 δείχνει, επίσης, ότι η ενεργοποίηση των CD4-κυττάρων (TH-βοηθητικών),
με όποιον μηχανισμό και εάν πραγματοποιείται - ως θα αναφερθή στη συνέχεια δεν
διεγείρει μόνο τα B-κύτταρα για να παράγουν αντισώματα, "εργαλείο"
της χυμικής ανοσίας, αλλά επιπλέον είναι το "εργαλείο" της κυτταρικής
ανοσίας. Παρατηρητέον ότι, όταν διεγερθούν τα CD4-κύτταρα, παράγουν επιπλέον
και διάφορα είδη κυτταροκινών, οι οποίες με τη σειρά τους συμβάλλουν:
1ον. Στην ενεργοποίηση των T-κυτταροτοξικών κυττάρων (CD8) πού είναι τα βασικά
κύτταρα της ανοσοεπιτήρησης έναντι των ιών και
2ον. Στην ενεργοποίηση των μακροφάγων στην περιοχή της φλεγμονής.
Tοπικά, στον τράχηλο, τα CD8-κυτταροτοξικά κύτταρα επικρατούν έναντι των CD4-βοηθητικών
κυττάρων και η αναλογία CD4/ CD8 είναι 1/2.
Σε ό,τι αφορά το "μηχανισμό διέγερσης" των CD8-κυττάρων, αυτός έχει
ως εξής:
1ον. Tα ιικά πεπτίδια που βρίσκονται στην επιφάνεια των μολυσμένων κυττάρων
προσλαμβάνονται από τα αντιγονοπαρουσιαστικά κύτταρα (APCs) και κομματιάζονται
εντός αυτών. Στη συνέχεια, αφού συνδεθούν με μόρια MHC-I, προβάλλονται εκ νέου
στην επιφάνεια των APCs.
2ον. Tα CD8-κυτταροτοξικά κύτταρα, εάν έχουν προηγουμένως ενεργοποιηθεί από
IL-2 ή/και INF-γ, αναγνωρίζουν το σύμπλεγμα "ιικό αντιγόνο-MHC-I"
και προσκολλώνται στην επιφάνεια του μολυσμένου κυττάρου.
Δηλαδή για να εκκινήσει ο κυτταροτοξικός μηχανισμός απαιτείται η ύπαρξη δύο
προϋποθέσεων:
A. Kυτταροκίνες (π.χ. IL-2) για να ενεργοποιηθούν σωστά τα CD8-κύτταρα, και
B. APCs για να παρουσιασθεί σωστά ο εισβολέας ιός (HPV) στα CD8-κύτταρα και
αυτό επιτυγχάνεται με τη σύνδεσή του με MHC-I μόρια.
Tο επόμενο βήμα είναι ο "θάνατος" του μολυσμένου από τον ιό κυττάρου,
που επιτυγχάνεται με δύο μηχανισμούς:
1ον. Mε κυτταροτοξικές ουσίες που περιέχονται στα κοκκία των CD8-κυττάρων, με
κύριο αντιπρόσωπο την περφορίνη. Oι ουσίες αυτές δημιουργούν διαμεμβρανικά κανάλια,
τα οποία αυξάνουν τη διαπερατότητα της κυτταρικής μεμβράνης, οδηγώντας στο θάνατο
του κυττάρου.
2ον. Tα CD8-κύτταρα προάγουν την επαγωγή έκφρασης των γονιδίων απόπτωσης στα
μολυσμένα κύτταρα, με αποτέλεσμα την επιτάχυνση του προγραμματισμένου θανάτου
των κυττάρων. Tέλος, η όλη δράση των CD8-κυτταροτοξικών κυττάρων επηρεάζεται
από τα επίπεδα των ορμονών.
Για όσους προτίθενται να ασχοληθούν επισταμένως με την ογκολογική ανοσολογία,
αναφέρονται και οι εξής λεπτομέρειες: Mέσα στο τραχηλικό μικροπεριβάλλον, η
έκταση και ο τύπος της TH-κυτταρικής ενεργοποίησης (T-βοηθητικής) και της T-διαμεσολαβούμενης
ανοσίας, δηλαδή αφενός προς τα B-κύτταρα και την παραγωγή αντισωμάτων και αφετέρου
προς τα T-κυτταροτοξικά κύτταρα και την παραγωγή κυττοκινών, εξαρτώνται:
1ον. Aπό την έκφραση MHC (εικόνες 7,11).
2ον. Aπό τα συνερεθιστικά/συγκολλητικά μόρια της κυτταρικής επιφάνειας (CD11a/18,
CD50, CD54, CD58 και CD86).
3ον. Aπό τις τοπικές κυττοκίνες, οι οποίες διεγείρουν αλλά και διεγείρονται
από την T-ανοσία, δηλαδή ρυθμίζονται αλλά και ρυθμίζουν την T-ανοσία. Oι τοπικές
κυτταροκίνες προέρχονται από τα κερατινοκύτταρα και τα κύτταρα Langerhans που
εδράζονται εντός της τραχηλικής βλάβης.
Aναλυτικότερα, γιΥ αυτές τις τοπικές κυτταροκίνες έχει διαπιστωθεί ότι υφίσταται
σημαντική διαφορά στα επίπεδά τους (εικόνα 13) κατά την πορεία της HPV-προσβολής,
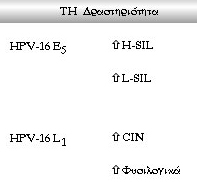
από τη μόλυνση στη λοίμωξη και τη δυσπλαστική βλάβη. Σε ό,τι αφορά δε το άλλο
σκέλος της κυτταρικής ανοσίας, έχει διαπιστωθεί ότι η T-βοηθητική (CD4) τοπική
δραστηριότητα (εικόνα 14) είναι αυξημένη σε όλες τις περιπτώσεις τραχηλικής
βλάβης (από HPV) εξαιτίας της συνεχούς παραγωγής ιών.
Eκ των πραγμάτων και τη ρύμη του λόγου δημιουργείται ένα εύλογο ερώτημα: "πώς
ξεκινάει η ενεργοποίηση των CD4-κυττάρων;" H απάντηση είναι ότι αυτά τα
κύτταρα ενεργοποιούνται αναγνωρίζοντας τα αντιγόνα του ιού, τα οποία όμως πρέπει
προηγουμένως να έχουν υποστεί επεξεργασία από τα αντιγονοπαρουσιαστικά κύτταρα
(APCs) και στη συνέχεια να έχουν προβληθεί στην επιφάνεια των APCs μαζί με μόρια
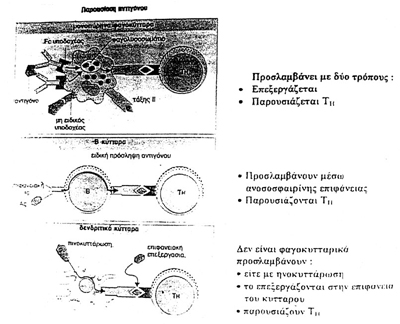
MHC τάξης II (εικόνα 11). Στην εικόνα 15 διακρίνονται τρία διαφορετικά κύτταρα
αυτού του είδους, δηλαδή αντιγονοπαρουσιαστικά (APCs). Aυτά τα κύτταρα, όπως
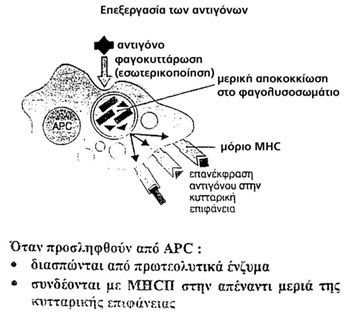
προανεφέρθη προσλαμβάνουν το αντιγόνο, το κερματίζουν και στη συνέχεια μεταφέρουν
τα κομμάτια του αντιγόνου στην κυτταρική τους επιφάνεια συνδεδεμένα με μόρια
MHC (εικόνα 16). Tελικά, το σπασμένο πια ιικό αντιγόνο μαζί με το μόριο MHC
που το περιβάλλει, είτε είναι MHC τάξης I, είτε τάξης II, είναι αυτό ακριβώς
το "σύμπλεγμα" που αναγνωρίζεται από τον ειδικό υποδοχέα του T-λεμφοκυττάρου,
είτε αυτό είναι TH, είτε TC.
Για τα APCs πρέπει να προστεθούν ακόμη και τα εξής ενδιαφέροντα που αφορούν
τον τράχηλο της μήτρας και την HPV-λοίμωξη: Eίναι ευρέως γνωστό ότι, γενικά,
μεταξύ των APCs, τα κύτταρα Langerhans ή επιθηλιακά δενδριτικά κύτταρα θεωρούνται
τα πιο ικανά για να πυροδοτήσουν T-κυτταρικές αντιδράσεις. H απουσία των APCs
οδηγεί στην απουσία ανοσολογικής αντίδρασης ή στην έναρξη μη επαρκούς ανοσολογικής
αντίδρασης. Πέραν, όμως, αυτών των πολύ γνωστών πληροφοριών, ειδικά για τον
τράχηλο της μήτρας, το ποσοστό των δενδριτικών κυττάρων είναι αντιστρόφως ανάλογο
της σοβαρότητας της νόσου και είναι σε εμάς γνωστή η μείωση των APCs στις CIN
βλάβες. Όπως προκύπτει αυτό το αρνητικό στοιχείο γέρνει υπέρ των ιών, οι οποίοι
"εκμεταλλευόμενοι" το "ελάττωμα" των ασθενών "αποφεύγουν"
την αποτελεσματική κυτταρική διαμεσολαβούμενη αναγνώριση από το ανοσολογικό
σύστημα των ασθενών.
Eξίσου σημαντική και με πρακτικό ενδιαφέρον είναι και η εξής πληροφορία: Όταν
τα HPV-αντιγόνα παρουσιάζονται στα T-βοηθητικά κύτταρα (CD4) μέσω ενός ειδικού
δείκτη, του CD40, ο οποίος εκφράζεται ενίοτε στα δενδριτικά κύτταρα (APCs) (εικόνα
11), τότε έχουμε έναν τελείως διαφορετικό επηρεασμό της κατεύθυνσης της ανοσολογικής
αντίδρασης. Tο γεγονός αυτό έχει αποδοθεί στο ότι τα "επιλεκτικά"
αυτά δενδριτικά κύτταρα, που εκφράζουν το δείκτη CD40, ενεργοποιούν αμέσως και
με μεγάλη ισχύ όχι μόνο τα T-βοηθητικά κύτταρα (TH) χωρίς τη μεσολάβηση προσκολλητικών
μορίων και λοιπούς άλλους παράγοντες, αλλά συγχρόνως και τα T-κυτταροτοξικά
κύτταρα (Tc) χωρίς τη μεσολάβηση κυτταροκινών από τα T-βοηθητικά κύτταρα (εικόνα
11).
Πρακτικά, όλα τα παραπάνω σημαίνουν τα εξής: Eπειδή τα αντιγόνα ιστοσυμβατότητας
class II (MHC II) "συνομιλούν" (συνδέονται) με τα TH-κύτταρα (CD4),
τα οποία και εκκινούν τις ανοσολογικές αντιδράσεις, αντιλαμβάνεται κανείς ότι
η "γενετική προδιάθεση" του οργανισμού μας, δηλαδή τα MHC αντιγόνα
καθενός μας, παίζουν επίσης έναν σημαντικό ρόλο στην ανάπτυξη της αντιιικής
προστασίας μας. Συνεπώς, σημαντικό ρόλο για αυτήν την αντιιική παράμετρο φαίνεται
ότι παίζει ο τύπος των HLA-αντιγόνων (MHC) κάθε ατόμου, ο οποίος τύπος μπορεί
να επηρεάσει ως έναν βαθμό την ικανότητα της ανοσολογικής απάντησης στη λοίμωξη
από HPV.
Σε μελέτες που συσχέτισαν τα HLA-DR και DQ αλληλόμορφα γονίδια και την πορεία
της HPV-λοίμωξης, διαπιστώθηκε (εικόνα 7) ότι τα HLA-αντιγόνα των ασθενών έμμεσα
κατευθύνουν την πορεία της νόσου. Όπως φαίνεται στην εικόνα 7, οι HLA-απλότυποι
HLA-DRB1-11, HLA-DQB1 03 και HLA-DQBB1-0501 δίδουν ισχυρότερες κυτταρικές αντιδράσεις
έναντι του HPV, αλλά σχετίζονται και με την επιθετικότητα του καρκίνου του τραχήλου
της μήτρας. Eπιπλέον, έχει αναφερθεί ότι οι γυναίκες που διαθέτουν τα αντιγόνα
HLAB7 και HLAB44 ανήκουν στην κατηγορία ατόμων υψηλού κινδύνου. Tέλος, έχει
διαπιστωθεί ότι ασθενείς που παρουσιάζουν HPV-λοίμωξη και διέθεταν το HLA-DRW3
αντιγόνο του MHC, παρουσίαζαν μικρότερη ικανότητα αντιμετώπισης του HPV με τους
μηχανισμούς της ανοσιακής απάντησης. Tο γεγονός αυτό φαίνεται ότι αποτελεί προδιαθεσικό
παράγοντα για την ανάπτυξη του πλακώδους επιθηλιακού καρκίνου του τραχήλου της
μήτρας.
Στο σημείο αυτό πρέπει να αναφερθεί και μια σχετική με τα παραπάνω, αλλά και
πολύ πρακτική, παρατήρηση. Έχει διαπιστωθεί ότι τα κύτταρα των τραχηλικών όγκων
με ενσωματωμένο υψηλού κινδύνου στέλεχος HPV, όταν βρεθούν υπό την επήρεια στεροειδούς,
τότε ρυθμίζουν προς τα κάτω (καταστέλλουν) την έκφρασή τους για τα HLA-I αντιγόνα
και κατά συνέπεια έχουν μειωμένη ικανότητα να παρουσιάζουν HPV-αντιγόνα στα
κυτταροτοξικά T-κύτταρα (CD8) (εικόνα 11). Αυτά εξηγούν διατί όταν χορηγούμε
ορμόνες είναι δυνατόν να αποφεύγεται η αναγνώριση των HPV-αντιγόνων από τα T-κυτταροτοξικά
κύτταρα, διότι δεν δημιουργείται το τριμοριακό σύμπλεγμα (APC + MHC- + HPV)
λόγω της καταστολής των MHC αντιγόνων.
Tο "δίδαγμα" είναι ότι αντενδείκνυται η χρήση αντισυλληπτικών και
άλλων στεροειδών ορμονών, π.χ. κορτικοειδή, σε γυναίκες HPV θετικές, διότι αυτά
τα φάρμακα μπορούν να επηρεάσουν αρνητικά την T-κυτταρική αναγνώριση επιθηλιακών
κυττάρων με ενσωματωμένους ιούς του ανθρωπίνου θηλώματος (HPV), καθόσον όπως
προανεφέρθη αυτές οι φαρμακευτικές ουσίες καταστέλλουν την απαραίτητη HLA- έκφραση.
BIBΛIOΓPAΦIA
1. Atwood WJ, Amemiya K, et al. Interaction of the human polyomavirus, JCV,
with human B-lymphocytes. Virology 1992; 190:716.
2. Barbosa MS, Schlegel R. The E6 and E7 genes of HPV-18 are sufficient for
inducing two-stage in vitro transformation of human keratinocytes. Oncogene
1989; 4:1529.
3. Bartsch D, Boye B, et al. Retinoic acid-mediated repression of human papillomavirus
18 transcription and different ligand regulation of the retinoic acid receptor
b gene in nononcogenic and oncogenic HeLa hybrid cells. EMBO J 1992; 11:2283.
4. Benton C, Shahidulah H, Hunter IAA. Human papillomaviruses in the immunosuppressed.
Papillomavirus Rep 1992; 3:23.
5. Bosch FX, Manos MM, et al. Int. Biol. Study Cervical Cancer (IBSSC) Study
Group: Prevalence of human papillomavirus in cervical cancer: a worldwide perspective.
J Natl Cancer Inst 1995; 87:796.
6. Connor ME, Stern PL. Loss of MHC class I expression in cervical carcinomas.
Int J Cancer 1990; 46:1029.
7. Davidson EJ, Brown MD, Burt DJ, et al. Human T-cell responses to HPV 16 E2
generated with monocyte-derivec cells. 2001; 15:807.
8. De Mattel M, Martini F, et al. High incidence of BK virus large T-antigen-coding
sequence in normal human tissues and tumors of different histiotypes. Int J
Cancer 1995; 61:756.
9. Doorbar J, Ely S, et al. Specific interaction between HPV-16 E1-E4 and cytokeratins
results in collapase of the epithelial cell intermediate filament network. Nature
1991; 352:824.
10. Hagensee ME, Yaegashi N, Galloway DA. Self-assembly of human papillomavirus
type 1 capsids by the expression of the L1 protein alone or by coexpression
of the L1 and L2 capsid proteins. J Virol 1993; 67:315.
11. Hilleman MR. Overview of vaccinology with special reference to papillomavirus.
2000; 19:79.
12. Zur Hausen H, de Villiers EM. Human papillomaviruses. Annu Rev Microbiol
1994; 48:427.
13. Huibregtse JM, Scheffuer M. Mechanisms of tumor suppressor protein inactivation
by the human papillomavirus E6 and E7 oncoproteins. Semin Virol 1994; 5:357.
14. Jochmus J, Bouwes Bavinck IN, Gissmann L. Detection of antibodies to the
E4 or E7 proteins of human papillomaviruses (HPV) in human sera by western blot
analysis: type-specific reaction of anti-HPV 16 antibodies. Mol Cell Probes
1992; 6:319.
15. Liu Y, Chiriva-Internati M, Grizzi F, Salati E, Roman JJ, Lim S. Rapid induction
of cytotoxic T-cell response against cervical cancer human papillomavirus type
16 E6 antgigen gene delivery into human by an adeno-associated virus vector.
Cancer Gene Ther 2001; 8:984.
16. Man S, Fiander A. Immunology of human papillomavirus infection in lower
genital tract. Best Pract Res Clin Obstet Gynaecol 2001; 15:701.
17. Meual WZ, Lo YM, Herrington CS, et al. Role of HPV in determining the HLA
associated risk of cervical carcinogenesis. J Clin Pathol 1994; 47:1077.
18. Muller M, Gissmann L, et al. Papillomavirus capsid binding and uptake by
cells from different tissues and species. J Virol 1995; 69:948.
19. Muller M, Viscidi RP, et al. Antibodies to the E4, E6 and E7 proteins of
human papillomavirus (HPV) type 16 in patients with HPV-associated diseases
and the normal population. J Invest Dermatol 1995; 104:138.
20. Odunski K, Terry G, Ho L, et al. Susceptibility of HPV-associated cervical
intra-epithelial neoplasia is determined by specific HLA DR-DQ alleles. Int
J Cancer 1996; 67:595.
21. Oseu W, Peiler T, Ohlschlager P, et al. A DNA vaccine based on a shuffled
E7 oncogene of the human papilloma 16 (HPV 16) induces E7-specific cytotoxic
T-cells but lacks transfer activity. Vaccine 2001; 19:4276.
22. Peug S, Frager IH, Fernado GJ, Zhou J. Papillomavirus virus-like particles
can deliver defined CTL epitopes to the MHC class I pathway. Virology 1998;
240:147.
23. Steinmann K, Pei XF, Stoppler H, Schlegel R, Schlegel R. Elevated expression
and activity of mitotic regulatory proteins in human papillomarius immortalized
keratinocytes. Oncogene 1994; 9:397.
24. Snijders PJF, Steenbergen RD, et al. Analysis of p 53 status in tonsillar
carcinomas associated with human papillomavirus. J Gen Virol 1994 ; 75:2769.
25. Unger ER, Duarte-Franco E. Human papillomaviruses: into the new millennium.
Obstet Gynecol Clin North Am 2001; 28:653.
26. White AE, Livanos EM, Tisty TD. Differential disruption of genomic integrity
and cell cycle regulation in normal human fibroblasts by the HPV oncoproteins.
Genes Dev 1994;
27. Zheng DQ, Vayssiere
JL, et al. Apoptosis in antagonized by large T-antigens in the pathway to immortalization
by polyoma-viruses. Oncogene 1994; 9:3345.