ΕΠΙΚΑΙΡΑ
ΘΕΜΑΤΑ ΙΙI
ΣΥΝΤΟΝΙΣΤΡΙΑ:
Μ. ΠΑΠΑΓΡΗΓΟΡΙΟΥ - ΘΕΟΔΩΡΙΔΟΥ
Μ.
Παπαγρηγορίου - Θεοδωρίδου:
Τα θέματα στα οποία θα αναφερθούν οι ομιλητές της τελευταίας συνεδρίας της 37ης
θεραπευτικής ενημέρωσης, έχουν κοινό σημείο συνάντησης τις λοιμώξεις. Είναι
γεγονός ότι οι λοιμώξεις τα τελευταία χρόνια βρίσκονται στο επίκεντρο του επιστημονικού
ενδιαφέροντος, δεδομένου ότι ο ορίζοντας των γνώσεων αυτού του τομέα συνεχώς
διευρύνεται.
Νέα λοιμώδη νοσήματα περιγράφονται, όπως το σύνδρομο της επίκτητης ανοσοανεπάρκειας
(AIDS), αναγνωρίζονται τα παθογόνα αίτια παλαιών κλινικών νοσημάτων (αιφνίδιο
εξάνθημα - ερπητοϊός 6), διευκρινίζονται παθογενετικοί μηχανισμοί που αφορούν
σε επιπλοκές γνωστών λοιμωδών νοσημάτων, όπως π.χ. η μικροβιακή μηνιγγίτις.
Καταλυτικό παράγοντα για την αλματώδη αυτή πρόοδο αποτέλεσε η εξέλιξη της βιοτεχνολογίας.
Εργαστηριακές μέθοδοι, όπως η αντίδραση της αλυσωτής πολυμεράσης (PCR), δημιούργησαν
νέες προοπτικές στο διαγνωστικό και θεραπευτικό τομέα.
Η πρώτη εισήγηση από την κυρία Βάνα Σπούλου αφορά στις νέες γνώσεις για τον
β-αιμολυτικό στρεπτόκοκκο της ομάδας Α. Στη συνέχεια η κυρία Θεώνη Πετροπούλου
θα αναφερθεί στο παρελθόν, το παρόν και το μέλλον των ανοσοσφαιρινών, ενώ η
κυρία Ιωάννα Παυλοπούλου θα εκφράσει τις επικρατούσες απόψεις και θέσεις για
εμβόλια που μας προβληματίζουν.
Στο τέλος της συνεδρίας θα δούμε πώς διαμορφώνεται το χρονοδιάγραμμα των εμβολιασμών
του 2004-2005.
Το πρόγραμμα των εμβολιασμών που προτείνεται από την εθνική επιτροπή διαμορφώνεται
και αναθεωρείται με βάση τα επιδημιολογικά δεδομένα της χώρας μας και την παρασκευή
και κυκλοφορία νέων εμβολίων.
Νεότερα για τις στρεπτοκοκκικές
λοιμώξεις
Β. ΣΠΟΥΛΟΥ
O β αιμολυτικός στρεπτόκοκκος
της ομάδας Α ή πυογόνος στρεπτόκοκκος, είναι ένας gram θετικός κόκκος που προκαλεί
τόσο επιπολής λοιμώξεις των βλεννογόνων και του δέρματος, όπως φαρυγγίτιδα,
αμυγδαλίτιδα, κυτταρίτιδα, ερυσίπελας, όσο και εν τω βάθει διεισδυτικές λοιμώξεις
με εκτεταμένες νεκρώσεις μυών και περιτονιών, όπως πυομυοσίτιδα και νεκρωτική
περιτονίτιδα (necrotizing fasciitis), ενώ οι πυρετογόνες τοξίνες του στρεπτοκόκκου
προκαλούν την οστρακιά.
Ιδιαίτερο ενδιαφέρον παρουσιάζουν και οι μη πυογόνες, ανοσολογικού τύπου κλινικές
εκδηλώσεις από το καρδιαγγειακό σύστημα, τα νεφρά, τις αρθρώσεις και το κεντρικό
νευρικό σύστημα (ΚΝΣ), που σχετίζονται με στρεπτοκοκκικές λοιμώξεις, όπως ο
ρευματικός πυρετός, η μεταστρεπτοκοκκική σπειραματονεφρίτιδα, η χορεία του Syndenham
και πρόσφατα το σύνδρομο Kawasaki και το σπάνιο παιδιατρικό νευροψυχιατρικό
σύνδρομο PANDAS (Paediatric autoimmune neuropsychiatric disorders associated
with streptococcal infections).

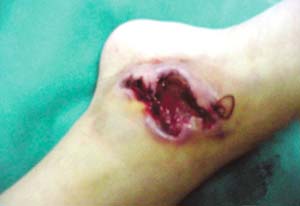
Εικόνα
1. Διεισδυτική στρεπτοκοκκική λοίμωξη σε κορίτσι 10 ετών μετά από
ανεμευλογιά.
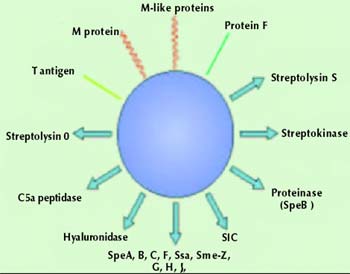
Σχήμα
2. Λοιμογόνοι παράγοντες στρεπτοκόκκου.
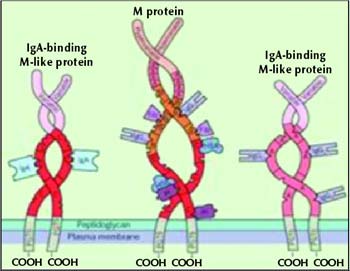
Σχήμα
3.
Δομή πρωτεΐνης Μ.
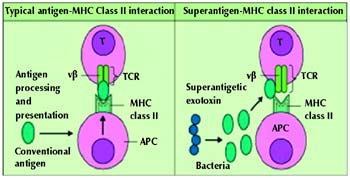
Σχήμα
4. Μηχανισμός
διέγερσης ανοσοποιητικού συστήματος από αντιγόνα και υπεραντιγόνα.
TCR: υποδοχέας Τ λέμφοκυττάρων, APC: αντιγονοπαρουσιαστικά κύτταρα, MHC class
II: μείζων σύμπλεγμα ιστοσυμβατότητας τάξης ΙΙ.
Διεισδυτικές
στρεπτοκοκκικές λοιμώξεις
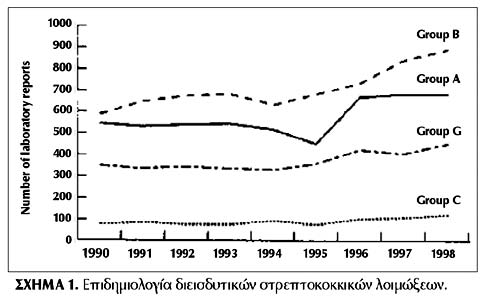
Η επιδημιολογία των διεισδυτικών στρεπτοκοκκικών λοιμώξεων παρουσιάζει σημαντικές
αλλαγές την τελευταία δεκαετία, με αύξηση της συχνότητας (σχήμα 1) αλλά και
της σοβαρότητας των κλινικών τους εκδηλώσεων. Είναι χαρακτηριστικό, επίσης,
ότι ενώ παλαιότερα οι εν των βάθει στρεπτοκοκκικές λοιμώξεις ήταν συνηθέστερες
σε ηλικιωμένους, άτομα με χρόνια νοσήματα όπως σακχαρώδη διαβήτη, νεφρική ανεπάρκεια,
αιματολογικά νοσήματα, ανοσοανεπάρκειες κ.λπ., τα τελευταία χρόνια, τα περισσότερα
περιστατικά συμβαίνουν σε νέα και χωρίς προδιαθεσικούς παράγοντες, άτομα. Στα
παιδιά παρατηρούνται συνήθως μετά από ανεμευλογιά (εικόνα 1).
Η νεκρωτική περιτονίτιδα, ή στρεπτοκοκκική γάγγραινα, είναι εν τω βάθει λοίμωξη
των υποδορίων ιστών που προκαλεί νέκρωση των περιτονιών και του λίπους, ενώ
αφήνει άθικτο το υπεράνω αυτών δέρμα. Η πύλη εισόδου είναι συχνά ένα μικρής
έκτασης τραύμα του δέρματος. Εξελίσσεται με πόνο, ερύθημα και οίδημα που επεκτείνεται
ταχύτατα, ενώ τις επόμενες ημέρες στην πύλη εισόδου εμφανίζονται φυσαλίδες και
ακολούθως η περιοχή γίνεται γαγγραινώδης. Στη στρεπτοκοκκική πυομυοσίτιδα, η
λοίμωξη των μυών γίνεται συνήθως αιματογενώς ή κατά συνέχεια ιστού, οπότε και
είναι δύσκολη η διαφοροδιάγνωση από τη νεκρωτική περιτονίτιδα. Στις περισσότερες
περιπτώσεις προσβάλλεται ένας μόνο μυς, υπάρχουν όμως και περιπτώσεις πολυσυστηματικής
προσβολής.
Τα τελευταία χρόνια, η κλινική συμπτωματολογία των διεισδυτικών αυτών στρεπτοκοκκικών
λοιμώξεων συνοδεύεται σε υψηλό ποσοστό, από πτώση της αρτηριακής πίεσης και
πολυσυστηματική προσβολή οργάνων, δηλαδή με εικόνα τοξικού shock. Στις περιπτώσεις
αυτές, η εξέλιξη της κλινικής συμπτωματολογίας είναι ταχύτατη, με εμφάνιση πολυσυστηματικής
οργανικής ανεπάρκειας μέσα σε 24-96 ώρες από την έναρξη των συμπτωμάτων και
θνητότητα που στη νεκρωτική περιτονίτιδα ανέρχεται σε 20-50% και στην πυομυοσίτιδα
σε 80-100%.
Λοιμογόνοι
παράγοντες στρεπτοκόκκου
Οι πρόοδοι της μοριακής βιολογίας αποκάλυψαν μεγάλο αριθμό γονιδίων που κωδικοποιούν
λοιμογόνους παράγοντες του στρεπτοκόκκου (σχήμα 2). Η συσσώρευση πολλαπλών τέτοιων
γονιδίων στο ίδιο στέλεχος, σχετίζεται με την αυξημένη λοιμογόνο έκφραση ορισμένων
στελεχών. Οι σημαντικότεροι λοιμογόνοι παράγοντες του στρεπτοκόκκου είναι οι
εξής:
Η πρωτεΐνη Μ, όπου πάνω από 80 διαφορετικοί τύποι της έχουν περιγραφεί μέχρι
σήμερα, που κωδικοποιούνται από την ομάδα γονιδίων emm. Η πρωτεΐνη έχει σπειροειδή
δομή που βοηθά στη διείσδυση του στρεπτοκόκκου στους εν τω βάθει ιστούς (σχήμα
3). Επίσης, σε συνδυασμό με το περίβλημα του στρεπτοκόκκου που αποτελείται από
επαναλαμβανόμενες μονάδες υαλουρονικού οξέος, βοηθά στην καλύτερη επιβίωση του
στρεπτοκόκκου στο αίμα και στους ιστούς. Αντισώματα έναντι της πρωτεΐνης Μ είναι
προστατευτικά έναντι του συγκεκριμένου οροτύπου.
Η πρωτεΐνη F (fibrinectin-binding protein), που βοηθά στην προσκόλληση του στρεπτοκόκκου
στα επιθηλιακά κύτταρα.
Οι στρεπτολυσίνες Ο και S, που εμποδίζουν τη φαγοκυττάρωση λόγω της κυτταροτοξικής
δράσης που έχουν στα φαγοκύτταρα.
Oι πυρετογόνες ή ερυθρογόνες εξωτοξίνες Α, B και C και οι λιγότερο γνωστές D,
Ζ-2, ο μιτογόνος παράγοντας SpeF και το στρεπτοκοκκικό υπεραντιγόνο SSA, που
είναι γνωστές και για τις ιδιότητές τους ως υπεραντιγόνα. Τα υπεραντιγόνα διαφέρουν
από τα συμβατικά αντιγόνα γιατί έχουν την ικανότητα να διεγείρουν μαζικά όλα
τα Τ λεμφοκύτταρα που φέρουν μια συγκεκριμένη αλληλουχία της β αλυσίδας του
υποδοχέα τους (Vβ2+ T λεμφοκύτταρα) και όχι μόνο εκείνα των οποίων ο υποδοχέας
παρουσιάζει δομική ομοιότητα με το υπεραντιγόνο επειδή προσκολλώνται άμεσα στη
συγκεκριμένη περιοχή της Vβ αλύσου των υποδοχέων των Τ λεμφοκυττάρων (σχήμα
4). Έτσι, ενώ τα συμβατικά αντιγόνα διεγείρουν περίπου 1 στα 10.000 κυκλοφορούντα
λεμφοκύτταρα, τα υπεραντιγόνα διεγείρουν 20-30% των κυκλοφορούντων λεμφοκυττάρων.
Η μαζική αυτή διέγερση των Τ λεμφοκυττάρων έχει ως αποτέλεσμα την απελευθέρωση
μεγάλης ποσότητας προφλεγμονωδών κυτταροκινών TNF-a, IL-1β, IL-6 που προκαλούν
πυρετό, πτώση της αρτηριακής πίεσης και εκτεταμένη καταστροφή των ιστών.
Οι πυρετογόνες εξωτοξίνες Α και Β κωδικοποιούνται από τα γονίδια speA και speB,
ενώ πρόσφατα ανακαλύφθηκε μια νέα οικογένεια γονιδίων που κωδικοποιούν υπεραντιγόνα,
τα γονίδια speG, speH και speJ.

ΣΧΗΜΑ
5. Παθογενετικός μηχανισμός στο σύνδρομο Kawasaki.
Νέες ανοσολογικές εκδηλώσεις στρεπτοκοκκικών λοιμώξεων
Στρεπτόκοκκος
και σύνδρομο Kawasaki
Οι ομοιότητες στην επιδημιολογία και την κλινική συμπτωματολογία που παρουσιάζει
το σ. Kawasaki με τις στρεπτοκοκκικές λοιμώξεις οδήγησε στην υπόθεση της συσχέτισης
του στρεπτοκόκκου με την παθογένεια του συνδρόμου. Η υπόθεση αυτή ενισχύθηκε
περισσότερο από την παρατήρηση ότι οι διαταραχές του ανοσολογικού συστήματος
που παρατηρούνται στο σ. Kawasaki είναι παρόμοιες με εκείνες που προκαλούν οι
τοξίνες του στρεπτοκόκκου, σε ασθενείς με εικόνα τοξικού shock. Υπάρχουν μάλιστα
βιβλιογραφικές αναφορές ασθενών, που ενώ παρουσίασαν αρχικά εικόνα τοξικού shock,
ακολούθως ανέπτυξαν ανευρύσματα των στεφανιαίων αγγείων που χαρακτηρίζουν το
σ. Kawasaki.
Είναι γνωστό ότι τα περιστατικά του σ. Kawasaki έχουν "επιδημική"
μορφή, με συσσώρευση των κρουσμάτων κυρίως το χειμώνα και την άνοιξη, περίοδος
που συμπίπτει επίσης με την αύξηση των στρεπτοκοκκικών λοιμώξεων. Η οξεία αυτοπεριοριζόμενη
φύση της νόσου, αλλά και η ηλικία των ασθενών, συνηγορούν για τη συσχέτιση του
συνδρόμου με λοιμογόνο παράγοντα. Το σ. Kawasaki παρατηρείται σε παιδιά 6-10
ετών που θεωρούνται ευάλωτα επειδή έχουν χάσει την προστασία από τα μητρικά
αντισώματα, ενώ δεν έχουν αναπτύξει ακόμα φυσική ανοσία στο συγκεκριμένο λοιμογόνο
παράγοντα.
Η κλινική συμπτωματολογία του σ. Kawasaki που χαρακτηρίζεται από πυρετό πάνω
από 5 ημέρες, επιπεφυκίτιδα, τραχηλική λεμφαδενοπάθεια, ερύθημα δέρματος και
βλεννογόνων, πολύμορφο εξάνθημα και απολέπιση των άκρων, είναι παρόμοια με την
κλινική συμπτωματολογία που προκαλούν οι τοξίνες του στρεπτοκόκκου σε ασθενείς
με οστρακιά ή τοξικό shock. Αλλά και οι ανοσολογικές διαταραχές στο σ. Kawasaki
είναι χαρακτηριστικές διέγερσης του ανοσοποιητικού συστήματος από βακτηριακά
υπεραντιγόνα και είναι οι ίδιες με αυτές που περιγράφονται στο τοξικό shock
από σταφυλόκοκκο ή στρεπτόκοκκο.
Η παθογένεια του σ. Kawasaki πιθανολογείται ότι εκδηλώνεται σε άτομα με γενετική
προδιάθεση, όταν αυτά αποικίζονται από στρεπτόκοκκο ή κάποιο μικροοργανισμό
που παράγει υπεραντιγόνα (σχήμα 5). Τα υπεραντιγόνα απορροφώνται από τους φλεγμαίνοντες
βλεννογόνους και προκαλούν διέγερση του ανοσοποιητικού συστήματος και υπερέκκριση
κυτταροκινών, που με τη σειρά τους ευθύνονται για τις κλινικές εκδηλώσεις του
σ. Kawasaki. Συγκεκριμένα, ο υψηλός πυρετός οφείλεται στην αύξηση των ΙL-1,
ΙL-6 και TNF-α, ενώ η τραχηλική λεμφαδενίτιδα στην αυξημένη ενεργοποίηση των
Β και Τ λεμφοκυττάρων. Σε απάντηση της διέγερσης από κυτταροκίνες, τα ενδοθηλιακά
κύτταρα των αγγείων γίνονται ευάλωτα σε κυτταροτοξικά αντισώματα και στη δημιουργία
θρόμβων. Η μυοκαρδίτιδα και η δημιουργία ανευρυσμάτων των στεφανιαίων αγγείων,
αποδίδονται στην ενεργοποίηση μιας υποομάδας Τ λεμφοκυττάρων που φέρουν υποδοχείς
έναντι των κυττάρων του ενδοθηλίου των αγγείων και του μυοκαρδίου και πυροδοτούν
την αλληλουχία των κυτταρικών και μοριακών γεγονότων που προκαλούν την αυτοάνοση
αγγειίτιδα που χαρακτηρίζει το σ. Kawasaki.
Σε μελέτη των Mc Cormick και συν, σε 13 από τους 16 ασθενείς με σ. Kawasaki
απομονώθηκαν βακτήρια που παράγουν υπεραντιγόνα. Η κατανόηση της παθογένειας
του σ. Kawasaki θα βοηθήσει στην καλύτερη διάγνωση και θεραπευτική αντιμετώπιση
της ασθένειας, που αποτελεί τη συχνότερη αιτία επίκτητης καρδιοπάθειας στην
παιδική ηλικία.

Στρεπτόκοκκος
και σύνδρομο PANDAS
Το σύνδρομο PANDAS (paediatric autoimmune neuropsychiatric disorders associated
with streptococcal infections) είναι μια σπάνια νευροψυχιατρική διαταραχή που
παρατηρείται σε παιδιά και οφείλεται σε βλάβες των βασικών γαγγλίων του εγκεφάλου
που αποδίδονται σε στρεπτοκοκκικές λοιμώξεις. Η παθογένεση του συνδρόμου αποδίδεται
σε αντιδράσεις αυτοανοσίας από αντισώματα κατά της πρωτεΐνης Μ που παρουσιάζουν
κυτταροτοξική δράση έναντι νευρώνων, οι οποίοι είναι υπεύθυνοι για την κινητικότητα
και τη συμπεριφορά. Τόσο τα παθολογοανατομικά ευρήματα σε ασθενείς με σ. PANDAS,
που είναι παρόμοια με εκείνα που παρουσιάζουν οι ασθενείς με χορεία του Sydenham,
όσο και η παρουσία αυτοαντισωμάτων έναντι των νευρώνων των βασικών γαγγλίων,
συνηγορούν για τη συσχέτιση του συνδρόμου με στρεπτοκοκκικές λοιμώξεις.
Είναι δύσκολο να υπολογισθεί η συχνότητα του σ. PANDAS στο γενικό πληθυσμό,
λόγω της σπανιότητάς του. Παρόλα αυτά, υπολογίζεται ότι 1 στα 7 παιδιά με μανιοκαταθλιπτικές
διαταραχές μπορεί να εμπίπτει στην ξεχωριστή κλινική οντότητα του σ. PANDAS,
όταν παρουσιάζει συγκεκριμένα διαγνωστικά κριτήρια (πίνακας 1):
1. Ύπαρξη μανιοκαταθλιπτικών διαταραχών, με ή χωρίς συνύπαρξη καθ' έξιν κινήσεων
(τικς).
2. Έναρξη στην παιδική ηλικία, από 3 ετών έως και την έναρξη της εφηβείας. Γενικά,
η μέση ηλικία έναρξης των συμπτωμάτων είναι τα 7 χρόνια και είναι περίπου 3
χρόνια νωρίτερα από εκείνη στην οποία εμφανίζονται αμιγείς νευροψυχιατρικές
διαταραχές. Σε μελέτη των Swedo και συν, η μέση ηλικία έναρξης των συμπτωμάτων
ήταν τα 7 χρόνια.
3. Ύπαρξη περιοδικής εμφάνισης των κλινικών συμπτωμάτων. Η κλινική πορεία χαρακτηρίζεται
από απότομη έναρξη και δραματική επιδείνωση των συμπτωμάτων σε συγκεκριμένες
χρονικές στιγμές. Μεταξύ των κρίσεων, τα συμπτώματα παρουσιάζουν ύφεση και σε
ορισμένες περιπτώσεις εξαφανίζονται.
4. Συσχέτιση με στρεπτοκοκκικές λοιμώξεις. Η επιδείνωση των συμπτωμάτων μπορεί
περιστασιακά να σχετίζεται με στρεπτοκοκκικές λοιμώξεις που επιβεβαιώνονται
με θετικές καλλιέργειες φαρυγγικού και αύξηση του τίτλου αντιστεπτολυσίνης.
Η στρεπτοκοκκική λοίμωξη πρέπει να προηγείται το πολύ μέχρι 6 εβδομάδες πριν
από την επιδείνωση των συμπτωμάτων. Για την επιβεβαίωση της διάγνωσης απαιτούνται
τουλάχιστον 2 τεκμηριωμένες στρεπτοκοκκικές λοιμώξεις που συνοδεύονται από επιδείνωση
των κλινικών συμπτωμάτων. Παρόλα αυτά, θα πρέπει να τονισθεί ότι συχνά η επιδείνωση
των συμπτωμάτων μπορεί να προκληθεί και από άλλες μικροβιακές ή ιογενείς λοιμώξεις.
Σε μελέτη των Swedo και συν σε 50 παιδιά με σ. PANDAS και πολλαπλές υποτροπές
των συμπτωμάτων, στρεπτοκοκκική λοίμωξη επιβεβαιώθηκε στο 42% των περιπτώσεων.
5. Συσχέτιση με νευρολογικές διαταραχές. Κατά τη διάρκεια επιδείνωσης των συμπτωμάτων,
οι ασθενείς παρουσιάζουν παθολογικά νευρολογικά ευρήματα, όπως υπερκινητικότητα
και χορειόμορφες κινήσεις, σε αντίθεση με τα παιδιά που παρουσιάζουν μόνο ψυχιατρικές
διαταραχές και στα οποία η νευρολογική εξέταση είναι συνήθως φυσιολογική.
Για τη θεραπευτική αντιμετώπιση ασθενών με σ. PANDAS, συστήνεται η χορήγηση
αντιμικροβιακής αγωγής και επί επιμονής των συμπτωμάτων, η αμυγδαλεκτομή. Οι
Μurphy και Pichichero δημοσίευσαν προοπτική μελέτη 12 παιδιών με σ. PANDAS,
στην οποία ανέφεραν ότι υπήρχε βελτίωση των συμπτωμάτων μετά τη χορήγηση χημειοπροφύλαξης
με πενικιλλίνη, ενώ η Οrvidas ανέφερε ύφεση των συμπτωμάτων σε 2 παιδιά με σ.
PANDAS μετά από αμυγδαλεκτομή.
Τα νέα δεδομένα για τις πυώδεις και ανοσολογικού τύπου κλινικές εκδηλώσεις που
σχετίζονται με το στρεπτόκοκκο, επιβάλλουν την επαγρύπνιση των παιδιάτρων για
την έγκαιρη διάγνωση και προσεκτική θεραπευτική αντιμετώπιση των στρεπτοκοκκικών
λοιμώξεων.
ΒΙΒΛΙΟΓΡΑΦΙΑ
Davies HD, Kirck V, Jadavji T, Kotzin BL. Simultaneous presentation of Kawasaki
disease and toxic syndrome in an adolescent male. Pediatr Infect Dis J 1996;
155:1.136-1.137.
Heubi C, Shott SR. PANDAS: Pediatric autoimmune neurophysiatric disorders associated
with streptococcal infections-an uncommon, but important indication for tonsillectomy.
Int J of Pediatr Otorhinolaryngology 2003; 67:837-840.
Hoare S, Abinum M, Cant A. Overlap between Kawasaki disease and group A streptococcal
infection. J Pediatr Inf Dis 1997; 16(6):633-634.
Leung DYM, Meissner HC, Fulton DR, Murray DL, Kotzin BL, Schlievert PM. Toxic
shock syndrome toxin-secreting Staphylococcus aureus in Kawasaki syndrome. Lancet
1993; 342:1.385-1.387.
Madeleine W, Cunningham. Pathogenesis of group A streptococcal infections. Clin
Microbiol Rev 2000; 13(3):470-511.
McCormick JK, Yarwood JM, Schlievert PM. Toxic shock syndrome and bacterial
superantigens: an update. Annu Rev Microbiol 2001; 55:77-104.
Meissner CH, Leung DYM. Kawasaki syndrome: Where are the answers? Pediatrics
2003; 672-675.
Meissner CH, Leung DYM. Superantigens, conventional antigens and the etiology
of Kawasaki syndrome. Pediatr Infect Dis J 2000; 19:91-94.
Murphy ML, Pichichero ME. Prospective Identification and Treatment of children
with Pediatric Autoimmune Neuropsychiatric Disorder Associated with Group A
Streptococcal Infection (PANDAS). Arch Pediatr Adolesc Med 2002; 156:356-361.
Orvidas LJ, Slattery MJ. Pediatric Autoimmune neurophysiatric Disorders and
Streptococcal Infections: Role of Otolaryngologist. The Laryngoscope 2001; 111:1.515-1.519.
Proft T, Sriskandan S, Yang L, Fraser JD. Superantigens and Streptococcal Toxic
Shock Syndrome. Emerg Infect
Dis 2003; 9(10).
Stevens DL. The flesh-eating Bacterium:What's next? J Inf Dis 1999; 179(2):366-374.
Swedo SE, Leonard HL, Garvey M, Mittleman B, Allen AJ, Perlmutter S, Lougee
L, Dow S, Zamkoff J, Dubbert B. Pediatric Autoimmune Neurophysic disorders associated
with streptocococcal infections: Clinical Description of the first 50 cases.
Am J Psychiatry 1998; 155(2):264-271.
Yarwood JM, Leung DYM, Sclievert PM. Evidence for the involvement of bacterial
superantigens in psoriasis, atopic dermatitis, and Kawasaki syndrome. FEMS Microbiol
Letters 2000; 192:1-7.