Μετάγγιση αίματος στη Μαιευτική
και Γυναικολογία - Κίνδυνοι
Π. Ταμπακούδης,
Γ. Ταμπακούδης,
Ι. Μπόντης
Α' Μαιευτική - Γυναικολογική Κλινική ΑΠΘ
Κατατέθηκε: 10/2/2003, Εγκρίθηκε: 7/3/2003
Αλληλογραφία: Π. Ταμπακούδης Πλ. Συντριβανίου 4 54621 Θεσσαλονίκη Τηλ. 2310 228497
Κατατέθηκε: 2/3/2003, Εγκρίθηκε: 22/3/2003
Περίληψη
Η μετάγγιση ομολόγου αίματος ή προϊόντων αίματος αποτελεί βασικό θεραπευτικό παράγοντα. Η ανάγκη για μετάγγιση αίματος σε μαιευτικές ασθενείς είναι συχνή, ποικίλη και διαμορφώνεται ως εξής: σε ασθενείς με σιδηροπενική αναιμία και τοκετό από την κολπική οδό στο 0,37%, σε περίπτωση καισαρικής τομής στο 6,8%, σε βαριές ετερόζυγες β-ΜΑ στο 4,5-5%, σε δρεπανοκυτταρική νόσο στο 60-79,2% και στην ομόζυγη β-ΜΑ δια βίου ανά μήνα, με μία ή δύο φιάλες αίματος των 300cc, οι οποίες γίνονται περισσότερες κατά τη διάρκεια της εγκυμοσύνης. Σε γυναικολογικές ασθενείς, τα ποσοστά μετάγγισης στην κολπική υστερεκτομή είναι 2,3%, σε κοιλιακή ολική υστερεκτομή κυμαίνονται από 2,8 έως 8,6%, ενώ αυξάνουν έτι περισσότερο σε γυναίκες με πυελικές φλεγμονώδεις νόσους και συμφύσεις των έσω γεννητικών οργάνων. Oι αντιδράσεις των μεταγγίσεων περιλαμβάνουν την ανοσοκαταστολή, το καρδιογενές πνευμονικό οίδημα και κυρίως τον κίνδυνο μετάδοσης νόσων. Τα κυριότερα λοιμογόνα αίτια είναι τα εξής: α) ιοί (HIV-1/2, HTLV-1/II, HAV, HBV, HCV, HDV, HEV, HGV, TTV, CMV, HHV-8, Parvo B19), β) βακτήρια (Treponema pallidum, Yarsinia enterocolitica) γ) παράσιτα (Plasmodium SP, Filariasis, Trypanosomiasis) και δ) η νόσος Creutzfeld-Jacob (CJD). Απώτερος στόχος είναι η μείωση κατά το δυνατόν της συχνότητας μετάγγισης, του ποσού του αίματος και η αποφυγή της μετάδοσης νόσων χάρις στις μεθόδους της μοριακής βιολογίας.
Όροι ευρετηρίου: Μετάγγιση αίματος, μαιευτική, γυναικολογία, κίνδυνοι.
ΟΡΙΣΜΟΣ ΤΗΣ ΑΝΑΙΜΙΑΣ ΣΤΗΝ ΚΥΗΣΗ
Αναιμία είναι η κατάσταση στην οποία παρατηρείται χαμηλή συγκέντρωση αιμοσφαιρίνης στο αίμα, με τιμή αυτής κάτω από ένα όριο. Το όριο αυτό βρίσκεται κατά δύο μέσες αποκλίσεις κάτω από τη μέση τιμή ενός υγιούς πληθυσμού της ιδίας ηλικίας, φύλου και ηλικίας κύησης(1). Αυτός, όμως, είναι ένας ορισμός με βάση τη στατιστική και όχι εύκολα κατανοητός και εύχρηστος. O ορισμός του Παγκόσμιου Oργανισμού Υγείας για τη διάγνωση της αναιμίας της κύησης είναι συγκέντρωση αιμοσφαιρίνης κάτω από 11g/dl και αιματοκρίτης χαμηλότερος από 33%, ενώ το κέντρο για τον έλεγχο των ασθενειών στις ΗΠΑ (CDC) προτείνει όριο 10.5g/dl στο 2ο τρίμηνο(2).
Η αναιμία είναι η συχνότερη παθολογική επιπλοκή στην εγκυμοσύνη και έχει κυμαινόμενη επίπτωση, αιτιολογία και βαρύτητα σε διαφορετικούς πληθυσμούς, με μεγαλύτερη συχνότητα στις μη βιομηχανικές χώρες(3). Η σιδηροπενική αναιμία είναι η συχνότερη διατροφική έλλειψη της κύησης, ακολουθούμενη από την έλλειψη φυλλικού οξέος. Η έλλειψη της Β12 είναι σχετικά σπανιότερη στις μη βιομηχανικές χώρες(4,5).
Σε 150 εκατομμύρια τοκετούς που γίνονται παγκοσμίως κάθε χρόνο, περίπου 600.000 γυναίκες πεθαίνουν από επιπλοκές της κύησης και του τοκετού, 30-40 εκατομμύρια υποφέρουν από οξείες επιπλοκές και 15-20 εκατομμύρια έχουν μακροπρόθεσμες επιπλοκές(6,7). Η αναιμία είναι υπεύθυνη για το 40-60% των θανάτων των σχετιζομένων με την κύηση στις μη βιομηχανικές χώρες(8). Προκαλεί άμεσους και έμμεσους θανάτους από καρδιακή ανεπάρκεια, αιμορραγία, λοίμωξη και προεκλαμψία. Επίσης, αυξάνει τη νεογνική θνησιμότητα και νοσηρότητα που σχετίζεται με πρόωρους τοκετούς, υπολειπόμενη ενδομήτρια ανάπτυξη, χαμηλά αποθέματα σιδήρου, σιδηροπενική αναιμία, καθώς και τις νοητικές και συναισθηματικές διαταραχές του νεογνού(1). Η ταξινόμηση των αναιμιών αναφέρεται στον πίνακα 1(9).
| Πίνακας 1. Ταξινόμηση αναιμιών |
| 1. Υπόχρωμες αναιμίες i) σιδηροπενική ii) σιδηροβλαστικές iii) αλκοολικές iv) δηλητηρίαση από μόλυβδο v) πορφυρίες α) συγγενής ερυθροποιητική πορφυρία β) συγγενής ερυθροποιητική πρωτοπορφυρία |
| 2. Μεγαλοβλαστικές αναιμίες i) από έλλειψη φυλλικού οξέος ii) από έλλειψη βιταμίνης Β12 iii) ανωμαλίες μεταβολισμού της Β12 ή του φυλλικού οξέος iv) άλλες αιτίες |
| 3. Αιμολυτικές αναιμίες α) Κληρονομικές αιμολυτικές αναιμίες i) με φυσιολογική μεμβράνη ερυθρού ii) από αντιγόνα ομάδων αίματος iii) κληρονομική σφαιροκυττάρωση iv) κληρονομική ελλειπτοκυττάρωση v) στοματοκυτταρική κληρονομική ελλειπτοκυττάρωση vi) άλλες σπάνιες κληρονομικές ανωμαλίες vii) με φυσιολογικό μεταβολισμό του ερυθρού viii) από έλλειψη G6PD ix) από έλλειψη πυρουβικής κινάσης x) από έλλειψη της 5-πυριμιδινικής νουκλεοτιδάσης β) Επίκτητες αιμολυτικές αναιμίες i) αυτοάνοση αιμολυτική αναιμία ii) φαρμακευτική άνοση αιμολυτική αναιμία iii) ισοάνοση αιμολυτική αναιμία iv) δευτεροπαθής αιμολυτική αναιμία v) παροξυσμική νυκτερινή αιμοσφαιρινουρία vi) σύνδρομα κατάτμησης ερυθροκυττάρου vii) άλλες αιμολυτικές αναιμίες |
| 4. Γενετικές διαταραχές της αιμοσφαιρίνης α) Θαλασσαναιμίες i) μείζων β-ΜΑ ii) ενδιάμεση β-ΜΑ iii) ελάσσων β-ΜΑ iv) α-ΜΑ β) Παθολογικές αιμοσφαιρίνες i) Δρεπανοκυτταρική αναιμία ii) Άλλες δομικές διαταραχές Hb iii) β-ΜΑ με επικρατούντα φαινότυπο iv) Κληρονομική παραμονή της HbF |
| 5. Απλαστικές, δυσερυθροποιητικές και δευτεροπαθείς αναιμίες i) απλαστική αναιμία ii) απλασία ερυθράς σειράς iii) κληρονομική δυσερυθροποιητική αναιμία iv) δευτεροπαθής αναιμία |
ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΑΝΑΙΜΙΑΣ ΣΤΗΝ ΚΥΗΣΗ
Σιδηροπενική αναιμία
Στη μητέρα
Η ήπια αναιμία ενδέχεται να μην έχει καμία επίπτωση στην κύηση και τον τοκετό, εκτός του ότι η μητέρα θα έχει πολύ χαμηλά αποθέματα σιδήρου και μπορεί να υποφέρει από μέτρια έως βαριά αναιμία σε επόμενες κυήσεις. Η μέτρια αναιμία μπορεί να προκαλέσει αυξανόμενη αδυναμία, απώλεια ενεργητικότητας, κόπωση και κακή απόδοση στην εργασία. Η γυναίκα μπορεί να έχει αίσθημα παλμών, ταχυκαρδία, λαχάνιασμα, αυξημένο καρδιακό έργο που μπορεί να οδηγήσει σε καρδιακό stress, το οποίο με τη σειρά του μπορεί να προκαλέσει αποσταθεροποίηση της ασθενούς, καρδιακή ανεπάρκεια ή και θάνατο(10,11). Η σιδηροπενική αναιμία αποτελεί το 90% των αναιμιών στην κύηση στο δυτικό κόσμο. Η αυξημένη συχνότητα εμφάνισης πρόωρου τοκετού (28,2%), προεκλαμψίας (31,2%) και σήψης έχουν συσχετιστεί με την αναιμία(1,8).
Στο έμβρυο
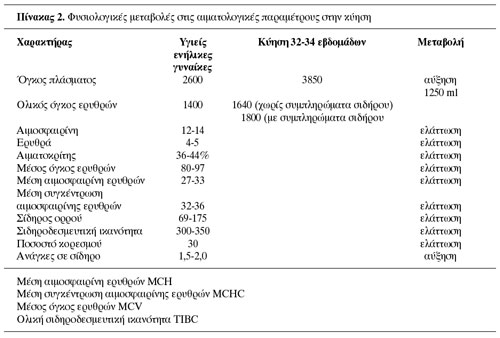
Άσχετα με τα χαμηλά αποθέματα σιδήρου, το έμβρυο έχει την τάση να εξασφαλίζει σίδηρο από τη μητρική τρανσφερρίνη, με τη δέσμευσή του από τον πλακούντα και τη γρήγορη και ενεργητική μεταφορά του στην εμβρυική κυκλοφορία. Σταδιακά ωστόσο, αυτά τα έμβρυα τείνουν να εμφανίσουν χαμηλά αποθέματα σιδήρου εξαιτίας των αντίστοιχων χαμηλών μητρικών αποθεμάτων. Επιπτώσεις με τη μορφή πρόωρων και υπολειπόμενης ανάπτυξης νεογνών και αυξημένα ποσοστά περιγεννητικής θνησιμότητας έχουν παρατηρηθεί σε κυήσεις αναιμικών γυναικών(12). Η αγωγή με συμπληρώματα σιδήρου βελτιώνει το περιγεννητικό αποτέλεσμα. Το μέσο βάρος στον τοκετό, το Apgar score και τα επίπεδα αιμοσφαιρίνης 3 μήνες μετά τον τοκετό ήταν σημαντικά υψηλότερα στα παιδιά των γυναικών της ομάδας υπό αγωγή με συμπληρώματα σιδήρου, από ό,τι της ομάδας υπό αγωγή με placebo(13). Oι φυσιολογικές μεταβολές στις αιματολογικές παραμέτρους κατά τη διάρκεια της κύησης φαίνονται στον πίνακα 2 και οι κατηγορίες αναιμίας στον πίνακα 3.

Μεσογειακή αναιμία (ΜΑ)
Oι θαλασσαναιμίες, οι πιο κοινές μονογονιδιακές διαταραχές, αποτελούν τη συχνότερη ετερογενή ομάδα κληρονομικών αιμοσφαιρινοπαθειών που χαρακτηρίζεται από την απουσία ή τη μειωμένη σύνθεση, σε ποικίλο βαθμό, μιας ή περισσοτέρων σφαιρινικών αλύσων και δημιουργεί προβλήματα δημόσιας υγείας σε αρκετές χώρες, τόσο κλινικά και γενετικά, όσο και κοινωνικοοικονομικά. Ανάλογα με την υπολειπόμενη άλυσο χαρακτηρίζονται ως α, β, δβ και γδβ ΜΑ. Oι συνήθεις κλινικές μορφές είναι η β-ΜΑ και η α-ΜΑ. Επίσης, αναφέρονται εδώ η αιμοσφαιρινοπάθεια Lepore, E, Κνωσσός και C, και η κληρονομική παραμονή της εμβρυϊκής αιμοσφαιρίνης (Hereditary Persistence of Fetal Hemoglobin - HPFH). Χάρη στην κατανόηση, τα τελευταία 35 χρόνια, της μοριακής γενετικής των ΜΑ, είναι πλέον καλά καθιερωμένη για την πλειονότητα των διαταραχών αυτών και ειδικά στις χώρες της Δύσης, η παθολογική και η μαιευτική αντιμετώπιση, με απόλυτο στόχο τη θετική περιγεννητική έκβαση. Απαιτείται έλεγχος των φορέων και προγεννητικός έλεγχος από εμβρυϊκό αίμα, αμνιακό υγρό και χοριακές λάχνες (CVS), με ανάλυση του DNA με Southern-Blotting, με τεχνικές PCR (Polymerase Chain Reaction) ή RFLPs (Restriction Fragment Length Polymorphisms), ή τώρα τελευταία, από τα εμβρυϊκά κύτταρα της μητρικής κυκλοφορίας ή προεμφυτευτικά (ζυγώτης 8 κυττάρων), τόσο με PCR όσο και με FISH (Fluorescent In Situ Hybridization). Oι έγκυες με ΜΑ, και ειδικότερα οι ομόζυγες, είναι περιστατικά υψηλού κινδύνου και χρήζουν ιδιαίτερης παρακολούθησης σε τμήματα εμβρυομητρικής ιατρικής καθΥ όλη την κύηση, αλλά ειδικότερα κατά το β' και γ' τρίμηνο, λόγω των πολυπαραγοντικών προβλημάτων της μητέρας και του εμβρύου. Η ομόζυγη α-ΜΑ είναι ασύμβατη με τη ζωή και καταλήγει συνήθως υπό τη μορφή του εμβρυϊκού ύδρωπα, ενώ οι πάσχουσες από ομόζυγη β-ΜΑ μπορεί να έχουν πιο ευνοϊκή πρόγνωση, όσον αφορά στο προσδόκιμο επιβίωσης και την ποιότητα ζωής. Oι ασθενείς που πάσχουν από ομόζυγη β-ΜΑ εμφανίζουν σοβαρή αναιμία, υπερσπληνισμό και είναι εξαρτημένες από τις μεταγγίσεις αίματος. Βέβαια, η θεραπεία της μείζονος θαλασσαναιμίας απαιτεί εκτίμηση των υπαρχόντων θεραπευτικών επιλογών για κάθε ασθενή και του λόγου κίνδυνος/όφελος, για μια υποστηρικτική (αποσιδήρωση, μέθοδοι αύξησης της παραγωγής HbF, θεραπεία γοναδικής δυσλειτουργίας) έναντι μιας θεραπευτικής προσέγγισης (χρήση αρχέγονων αιμοποιητικών κυττάρων, όπως αίμα ομφαλίου λώρου, εμβρυϊκό ήπαρ, αλλογενής μεταμόσχευση και τελευταία γονιδιακή θεραπεία)(14-18).
Γεωγραφική κατανομή των ΜΑ
Μια ομάδα εργασίας του Παγκόσμιου Oργανισμού Υγείας (ΠOΥ) έχει υπολογίσει ότι υπάρχουν πάνω από 240 εκατομμύρια φορείς των κληρονομούμενων αιμοσφαιρινικών διαταραχών και ότι κάθε έτος γεννώνται 100.000 με 300.000 σοβαρά προσβεβλημένοι ομοζυγώτες ή συνδυασμένοι βαρείς ετεροζυγώτες(19).
Η συχνότητα στον ελλαδικό χώρο κυμαίνεται από 3,5 έως 20,5% (ΜΤ 7,8%)(20).
Δρεπανοκυτταρικά σύνδρομα
Τα μείζονα δρεπανοκυτταρικά σύνδρομα, όπως η δρεπανοκυτταρική νόσος (HbSS), η νόσος HbSC και η μικροδρεπανοκυτταρική αναιμία (Hbs-βΑ-Thal και Hbs-β+-Thal), αποτελούν μια κληρονομική πολυσυστηματική διαταραχή. Τα κύρια χαρακτηριστικά τους είναι η χρόνια αιμολυτική αναιμία, η αυξημένη ευαισθησία στις λοιμώξεις και οι επαναλαμβανόμενες -ιδίως κατά το βΥ ήμισυ της κύησης- επώδυνες κρίσεις, που σχετίζονται με το ποσό της HbS μέσα στο ερυθροκύτταρο. Η ετερόζυγη μορφή (HbAS) σχετίζεται μόνο με αυξημένη ευαισθησία στις λοιμώξεις από το ουροποιητικό. Τα τελευταία 35 χρόνια, χάρη στην κατανόηση της μοριακής γενετικής των δρεπανοκυτταρικών συνδρόμων, είναι πλέον καλά καθιερωμένη, ιδίως την τελευταία δεκαετία και κυρίως στις χώρες της Δύσης, η παθολογική και η μαιευτική αντιμετώπιση, με απώτερο στόχο τη βελτιωμένη περιγεννητική έκβαση και τη μείωση της μητρικής θνησιμότητας (0-4,5%). Απαιτείται γενετική καθοδήγηση, έλεγχος των φορέων και προγεννητικός έλεγχος από εμβρυϊκό αίμα, αμνιακό υγρό και χοριακές λάχνες (CVS) με ανάλυση του DNA. Oι έγκυες με δρεπανοκυτταρικά σύνδρομα είναι περιστατικά υψηλού κινδύνου και χρήζουν ιδιαίτερης παρακολούθησης σε τμήματα εμβρυομητρικής ιατρικής καθ' όλη τη διάρκεια της κύησης, αλλά ειδικότερα κατά το β' και γ' τρίμηνο, λόγω των πολυπαραγοντικών προβλημάτων της μητέρας και του εμβρύου. Επειδή υπάρχουν διαφωνίες όσον αφορά στη χρήση της μετάγγισης ως θεραπεία στις έγκυες με μείζονα δρεπανοκυτταρικά σύνδρομα, θα πρέπει να εφαρμόζεται εξατομίκευση βάσει της ιδιαιτερότητας της ασθενούς και βάσει της εμπειρίας των θεραπόντων ιατρών (Μαιευτήρας και Αιματολόγος), γιατί αυτό είναι ένας παράγοντας «κλειδί» στην επιτυχή αντιμετώπιση των εγκύων αυτών. Νέα θεραπευτικά σχήματα (5-αζακυτιδίνη, υδροξυουρία, ερυθροποιητίνη, μεταμόσχευση μυελού, γονιδιακή θεραπεία) φαίνονται στον ορίζοντα για τις ασθενείς με μείζονα δρεπανοκυτταρικά σύνδρομα, αλλά η εφαρμογή τους στην κύηση απαιτεί περαιτέρω μελέτη(21-23).
Oι Ταμπακούδης και συν.(24) μελέτησαν αναδρομικά, μεταξύ των ετών 1980-1996, 46 επιτυχείς μονήρεις κυήσεις, σε σύνολο 64 κυήσεων και 36 ασθενών με δρεπανοκυτταρική (SS) (20) και μικροδρεπανοκυτταρική αναιμία (SB)(16). Το συνολικό ποσοστό επιτυχούς κύησης ήταν 72,4%. Από αυτές τις κυήσεις, οι 28 επεπλάκησαν με SS και οι 18 με SB και είχαν μέση ηλικία 25,2±4,9 και 22,5±0,7 έτη αντίστοιχα. Στις δύο ομάδες (SS και SB) παρατηρήθηκε υψηλή συχνότητα επώδυνων κρίσεων (50% και 38,3% αντίστοιχα), προεκλαμψίας (42,8% και 27,7%), λοιμώξεων των ουροφόρων οδών (42,8% και 38,3%), οξείας αναιμίας (7,1% και 11,1%) και πρόωρου τοκετού (32,1% και 27,7%). Το μέσο βάρος γέννησης ήταν 2.640±450g και 2.830±720g -τα νεογνά <2.500g- (42,8% και 27,7%) και το Apgar Score στα 5Υ (9 και 9) σε αναλογία 82,2% και 88,8% αντίστοιχα στις ομάδες SS και SB. Μετάγγιση αίματος από 2 έως 9 φιάλες έγινε σε ποσοστό 78,4% και 79,2% σε SS και SB αντίστοιχα, σε αναλογία στις εξής κυρίως περιπτώσεις: Hb <8,5g/dl, επώδυνες κρίσεις, καρδιαγγειακή αστάθεια και προεγχειρητικά. Τα ποσοστά των καισαρικών τομών στην SS και στη SB ήταν αντίστοιχα 46,4% (13/28 έγκυες) και 44,4% (7/18 έγκυες). Δεν παρατηρήθηκε μητρική θνησιμότητα στο υλικό της μελέτης μας και η περιγεννητική θνησιμότητα κυμάνθηκε στο 4,3%. Συμπερασματικά, φαίνεται ότι η παρακολούθηση των εγκύων με αιμοσφαιρινοπάθεια S, σε οργανωμένα κέντρα εμβρυομητρικής ιατρικής σε αγαστή συνεργασία με άλλες ιατρικές ειδικότητες και ιδία του Αιματολόγου, συνετέλεσε στη δραματική μείωση την τελευταία 10ετία τόσο της περιγεννητικής, όσο και της μητρικής νοσηρότητας και θνησιμότητας, ειδικά στις αναπτυσσόμενες χώρες.
Oι δρεπανοκυτταρικές αιμοσφαιρινοπάθειες απαντούν στην Αφρική, στη Μέση και Άπω Ανατολή και σε χώρες της Μεσογείου, στους δε νέγρους των ΗΠΑ σε αναλογία 12%(22). Η συχνότητα των δρεπανοκυτταρικών συνδρόμων στον ελλαδικό χώρο κυμαίνεται μεταξύ 0,97-0,98%(20,25).

Μεγαλοβλαστική αναιμία
Η μεγαλοβλαστική αναιμία χαρακτηρίζεται από μακροκυττάρωση ως αποτέλεσμα της διαταραχής είτε της σύνθεσης νουκλεοτιδίων, δηλαδή του σχηματισμού πουρινών και πυριδιμινών απαραίτητων για την ωρίμανση και τον πολλαπλασιασμό των νέων κυττάρων, είτε της μετατόπισης των αμινοξέων κυρίως στις αντιδράσεις μεθυλίωσης στον κύκλο της μεθιονίνης - ομοκυστίνης που παρατηρούνται στην έλλειψη φυλλικού οξέος(1,9).
Η καθυστέρηση στην ωρίμανση του πυρήνα επηρεάζει τα ερυθροκύτταρα, τα λευκοκύτταρα και τα αιμοπετάλια, γιΥ αυτό είναι δυνατό να παρατηρηθεί όχι μόνο αναιμία, αλλά ακόμη λευκοπενία και θρομβοπενία. Αυτή η διαταραχή της σύνθεσης του DNA είναι αποτέλεσμα διατροφής (έλλειψη φυλλικού οξέος ή βι-ταμίνης Β12), σε ποσοστό μεγαλύτερο από το 95% των περιπτώσεων(9,26).
Η αναιμία λόγω έλλειψης φυλλικού οξέος συνδυάζεται με την πρόωρη αποκόλληση του πλακούντα, τις αυτόματες εκτρώσεις, τον ενδομήτριο θάνατο, την προεκλαμψία, τη μείωση του όγκου αίματος στη μητέρα, το IUGR, την ανεπάρκεια πλακούντα, την προωρότητα και με τις ανοικτές βλάβες του ΚΝΣ(9,26,27).
Oι ανοικτές βλάβες του ΚΝΣ (ΑΒΝ) ακολουθούν από πλευράς συχνότητας τις καρδιακές γενετικές ανωμαλίες και διαγιγνώσκονται εύκολα κατά την κύηση υπερηχογραφικά. Διακρίνονται σ' αυτές που αφορούν στην έλλειψη των οστών του θόλου του κρανίου, με σπουδαιότερες βλάβες την ανεγκεφαλία και τις μηνιγγομυελοκήλες, και σ' εκείνες που αποτελούν τις δυσραφίες, με συχνότερη βλάβη τη δισχιδή ράχη. Είναι συχνότερες στη Μ. Βρετανία και τη Β. Ιρλανδία, απ' ότι στην υπόλοιπη Ευρώπη και τις ΗΠΑ. Oι ΑΒΝ είναι πολυπαραγοντικής αιτιολογίας, με επικράτηση των περιβαλλοντικών και γενετικών παραγόντων. Υποστηρίζεται ότι η επίδραση της θερμότητας κατά τις πρώτες 6 εβδομάδες όπως και οι λοιμώξεις από ιούς και βακτηρίδια και η λήψη βαλπροϊκού νατρίου και καρμπαμαζεπίνης, καθώς και Zn, συντελεί στη συχνότερη εμφάνιση των ΑΒΝ. Αντίθετα, πρόσφατα ενισχύεται η άποψη ότι η λήψη φυλλικού οξέος στα αρχικά στάδια της εγκυμοσύνης συντελεί στην πρόληψη των ΑΒΝ κατά 73%. Πρέπει να τονισθεί ότι την ομάδα «υψηλού κινδύνου» για ΑΒΝ αποτελούν: α) έγκυες με οικογενειακό ιστορικό, β) έγκυες με υψηλά επίπεδα AFP στον ορό, γ) έγκυες χαμηλού κοινωνικού - οικονομικού επι-πέδου. Η συχνότητα των χρωμοσωμικών ανωμαλιών είναι 9% όταν η βλάβη είναι μονήρης, φτάνει το 22% όταν συνυπάρχει IUGR, ενώ σε σύνδρομο πολλαπλών γενετικών βλαβών, το ποσοστό των χρωματοσωμικών ανωμαλιών ανέρχεται στο 29% και αν συνυπάρχει IUGR εγγίζει το 40%(27).
Η συχνότητα της μεγαλοβλαστικής αναιμίας κατά τη διάρκεια της κύησης φθίνει προοδευτικά λόγω της ευρύτερης σήμερα χορήγησης του συνδυασμού φυλλικού οξέος και σιδήρου και ξεκινά από 0,5-3% στις χώρες της Δύσης, μέχρι 24% στη Μαλαισία και στις χώρες του Τρίτου Κόσμου(9,26).
Oι Ταμπακούδης και συν.(28) αναφέρουν μία μόνο σπάνια περίπτωση πρωτοτόκου γυναίκας ηλικίας 29 ετών, η οποία διακομίστηκε στην ΑΥ Μαιευτική - Γυναικολογική του ΑΠΘ με Ht 24,2% και Hb 8,2%, ενώ βρισκόταν στην 40η εβδομάδα της κύησης. O έλεγχος του περιφερικού αίματος και του μυελογράμματος έθεσε τη διάγνωση της μεγαλοβλαστικής αναιμίας της εγκυμοσύνης από έλλειψη φυλλικού οξέος. Αφού χορηγήθηκαν φυλλικό οξύ, βιταμίνη Β12 και 1.200cc αίματος, γέννησε την 41η εβδομάδα με καισαρική τομή λόγω παράτασης τοκετού, ένα ζων θήλυ, αρτιμελές νεογέννητο, βάρους 3.120g.
ΙΣΤΟΡΙΑ ΤΗΣ ΜΕΤΑΓΓΙΣΗΣ ΑΙΜΑΤΟΣ
Περιγραφές για τις μυστικές ιδιότητες του αίματος εμφανίσθηκαν νωρίς, το 200μ.Χ., όταν η αφαίμαξη πραγματοποιούταν για την απελευθέρωση των δαιμονισμένων. Η πρώτη επιτυχής μετάγγιση πραγματοποιήθηκε στους ανθρώπους από τον Richard Lower, ο οποίος μετάγγισε αίμα από αμνό (ετερόλογη μετάγγιση) σ' ένα παράφρονα άνδρα. Μολονότι ο ασθενής ανένηψε, μεταγενέστερες εμπειρίες με ετερόλογες μεταγγίσεις οδήγησαν σε επιπλοκές και ήταν το 1818 όταν ο James Blundell εισήγαγε την πρώτη ειδική (από άνθρωπο σε άνθρωπο - ομόλογη) μετάγγιση για οξεία αιμορραγία.
Παρά αυτές τις επιτυχίες, οι ομόλογες μεταγγίσεις συχνά είχαν ως αποτέλεσμα βαριές και συχνά θανατηφόρες αντιδράσεις μέχρι το 1911, όταν ο Ottenberg ανέπτυξε την ιδέα και πρακτική του προκαταρκτικού ελέγχου συμβατότητας του αίματος πριν την χορήγησή του, η οποία και οδήγησε στην εγκαθίδρυση της πρώτης τράπεζας αίματος στο Cook County νοσοκομείο, το 1937.
Κατά τη διάρκεια του δευτέρου παγκοσμίου πολέμου οργανώθηκε πρόγραμμα συλλογής και φύλαξης μεγάλων ποσοτήτων ομάδας O ή IV αίματος για τις ανάγκες των στρατιωτικών νοσοκομείων των ΗΠΑ. Αυτή η εμπειρία εγκαθίδρυσε τη σημασία της μετάγγισης αίματος στη θεραπεία του υποογκαιμικού shock. Ωστόσο, επειδή το αίμα είναι πολύτιμη πηγή παραγώγων και οι μεταγγίσεις παρουσίαζαν αρκετούς κινδύνους, η κλινικά αποδεκτή προσέγγιση είναι η οριοθέτηση ειδικών ενδείξεων χρήσης των παραγώγων του αίματος(29-31).

ΓΕΝΙΚΕΣ ΚΑΤΕΥΘΥΝΣΕΙΣ ΓΙΑ ΤΗ ΜΕΤΑΓΓΙΣΗ ΑΙΜΑΤΟΣ
Τα τελευταία 23 έτη υπάρχει μια γενική τάση ελάττωσης της χρήσης της μετάγγισης αίματος στη μαιευτική και γυναικολογική πρακτική. Ανάμεσα στις αιτίες(32) είναι:
- Φόβοι ασθενών και κλινικών σχετικά με τους κινδύνους, ειδικά μετά την ανακάλυψη του ιού HIV.
- Αναγνώριση ότι η μετάγγιση αίματος δεν είναι απαραίτητη για αρκετές περιπτώσεις που αντιμετωπίζονταν στο παρελθόν με αυτόν τον τρόπο.
- Λόγοι κόστους.
Αρκετές μελέτες αποδεικνύουν την ελάττωση των μεταγγίσεων. Oι Camman και συν.(33) διαπίστωσαν ελάττωση του αριθμού των μεταγγίσεων κατά τη διάρκεια καισαρικών, από 6% στο 3%, σε μία τετραετία. Άλλη μελέτη, διάρκειας πάνω από τέσσερα έτη, έδειξε 63% μείωση των τιμών των μεταγγίσεων παρά την αύξηση των καισαρικών στο 77%(33). Η μελέτη απέδειξε βελτίωση με τη θεραπεία υποκατάστασης με σίδηρο, αποφεύγοντας έτσι τις μεταγγίσεις στις γυναίκες με σιδηροπενική αναιμία προ και μετά τον τοκετό. O Sharma(10) αναφέρει λήψη φυλλικού οξεός καθΥ όλη τη διάρκεια της κύησης, ενώ προκειμένου για τη χορήγηση του σιδήρου <30 εβδομάδες, συνιστά λήψη per os, ενίοτε im ή iv. Μεταξύ 30ης-36ης εβδομάδας συνιστά λήψη per os, im ή iv, ενώ μετά τις 36 εβδομάδες συνιστά μετάγγιση αίματος.
Oι Ταμπακούδης και συν.(34) μελέτησαν την αποτελεσματικότητα της συμπληρωματικής χορήγησης πρωτεϊνοηλεκτρικού Fe στην κύηση. Παρατήρησαν ότι τα μητρικά επίπεδα ερυθροποιητίνης του ορού ήταν αυξημένα στην ομάδα που δεν ελάμβανε συμπλήρωμα σιδήρου, δείχνοντας μια τάση για υποξυγοναιμία. Αν και η τελευταία έλειπε από κάθε κλινική συνέπεια στη μελέτη, αυτό το γεγονός πρέπει να λαμβάνεται υπόψη στην απόφαση για το αν θα χορηγήσουμε συμπλήρωμα σιδήρου και φυλλικού οξέος στην εγκυμοσύνη ή όχι. Oι Achadi και συν.(35) αναφέρουν ότι το επίπεδο Fe του νεογέννητου συνδέεται με το βάρος (α172g) και το ύψος (α1 cm) αυτού.
Παρά τη μείωση των μεταγγίσεων αίματος, η μαιευτική έκβαση βελτιώθηκε. Επιπλέον, παρόμοια τάση υπάρχει και στη Γυναικολογία. O Benjamin(36) σύγκρινε τον αριθμό των περιεγχειρητικών μεταγγίσεων σε γυναίκες που υποβλήθηκαν σε ριζική υστερεκτομή, προ και μετά την ανακάλυψη του HIV. Αυτοί βρήκαν σημαντική ελάττωση των μεταγγίσεων ερυθρών από 91% στο 44%, όταν ο HIV αναγνωρίσθηκε ως κίνδυνος των μεταγγίσεων αίματος. Επίσης, άλλες μελέτες δείχνουν μείωση των μεταγγίσεων με την εισαγωγή της προληπτικής εκπαίδευσης(37). Η μείωση των μεταγγίσεων ακολουθήθηκε από δύο ανακαλύψεις. Πρώτη ήταν αυτή της αυτόλογης μετάγγισης και δεύτερη αυτή των ομάδων και του screening. Λόγω της θεώρησης σχετικά με τις επίκτητες λοιμώξεις από τις μεταγγίσεις, η δυνατότητα της χρήσης της αυτόλογης μετάγγισης στη μαιευτική και γυναικολογική πρακτική ερευνήθηκε το 1970 και το 1980. Oι περισσότερες από αυτές τις πρώιμες μελέτες έδειξαν ότι αυτή η τεχνική είναι ασφαλής(32). Η αυτόλογη μετάγγιση αίματος ελαττώνει τον κίνδυνο των ανοσολογικών προβλημάτων από τη λήψη αίματος(38). Όμως, η πιθανότητα της μετάγγισης μετά τον τοκετό δεν ήταν πάντα προβλέψιμη και συχνά σε χαμηλό ποσοστό(39).
Κατά τη δεκαετία του Υ80, περισσότερες μονάδες ελέγχονταν για ομάδα και υποβάλλονταν σε screening έλεγχο, ως εναλλακτική λύση για τη διαδικασία της διασταύρωσης, με αποτέλεσμα να ελαττωθούν οι μεταγγίσεις και να προληφθούν οι ασυμβατότητες(40). Αυτές οι διαδικασίες μείωσαν επίσης τις διασταυρώσεις, με σημαντικά οικονομικά οφέλη, ενώ έχει υποστηριχθεί ότι μια ομάδα και ένας screening έλεγχος είναι αρκετά για εκείνες τις γυναίκες στις οποίες οι εγχειρήσεις έχουν λιγότερο από 10% πιθανότητα αναζήτησης αίματος και στις εγχειρήσεις που η σχέση διασταύρωση προς μετάγγιση ήταν μεγαλύτερη από 2:1(41). Oριστικές διαφορές υπάρχουν στην πρακτική των μητρικών μονάδων ακόμη να διασταυρώνονται, με 56% και 29% για εκλεκτική καισαρική και εμβρυϊκή δυσφορία στον τοκετό αντίστοιχα(42). Oι δυσμενείς ανοσολογικές αντιδράσεις της μετάγγισης αίματος είναι δυνατόν να διακριθούν σε δύο ομάδες: τις ήπιες (αλλεργικές) σε ποσοστό 2-4% και τις σοβαρές σε αναλογία 0,0004% από οξεία αιμόλυση λόγω μετάγγισης από ασύμβατο αίμα. Η βαρύτητα της αντίδρασης εξαρτάται από τον τίτλο των αντισωμάτων, τη συγγένεια των αντισωμάτων και την ποσότητα των μεταγγισθέντων ερυθροκυττάρων. Βαριές αιμολυτικές αντιδράσεις κατά τη μετάγγιση επισυμβαίνουν σε ποσοστό 1:600/μονάδες μετάγγισης και η συχνότητα θανάτου είναι 1:100.000/μονάδες μετάγγισης(31,42).
ΠΟΣΟΣΤΑ ΜΕΤΑΓΓΙΣΕΩΝ
Η ανάγκη για μετάγγιση αίματος σε μαιευτικές ασθενείς είναι συχνή, ποικίλη και διαμορφώνεται ως εξής: σε ασθενείς με σιδηροπενική αναιμία με τοκετό από την κολπική οδό 0,37%(31), σε περίπτωση καισαρικής τομής 6,8%(31), σε βαριές ετερόζυγες β-ΜΑ 4,5-5%(16), στη δρεπανοκυτταρική νόσο οι Ταμπακούδης και συν.(24) αναφέρουν ποσοστά από 78,4 έως 79,2%, ενώ οι Rust και Perry(22) ποσοστό 60-75% και δια βίου σε περιπτώσεις ομόζυγης β-ΜΑ(16,18).
Σήμερα, εφαρμόζεται το σύστημα των υπερμεταγγίσεων σε περιπτώσεις ομόζυγης ΜΑ, ώστε τα επίπεδα της Hb να είναι >10g/dl(17). Παρά τα σημαντικά βήματα που έχουν γίνει αναφορικά με την αντιμετώπιση των ασθενών με χρόνιες αναιμίες (απλαστική αναιμία, αιμοσφαιρινοπάθειες), η μεταγγισιοθεραπεία συνεχίζει να κατέχει πρωταρχική θέση στη θεραπεία τους(16,17).
Με κάθε μονάδα συμπυκνωμάτων ερυθροκυττάρων χορηγούνται στις ασθενείς περίπου 200-250mg σιδήρου(17). Ειδικά στις ασθενείς με ΜΑ στις οποίες επιπλέον παρατηρείται αυξημένη απορρόφηση σιδήρου, η αιμοσιδήρωση δημιουργεί δυσλειτουργία των διαφόρων οργάνων και ιδίως της καρδιάς, του ήπατος και των ενδοκρινών αδένων και επομένως επηρεάζει καθοριστικά την επιβίωση(16). Η συχνότητα των μεταγγίσεων στη Μαιευτική ποικίλει από 0,16 έως 2,6%(31,32,44). Επιπλέον, η Sanguis μελέτη από 43 ευρωπαϊκά νοσοκομεία βρήκε τεράστια διαφορά στο ποσοστό των ασθενών που μεταγγίστηκαν με ερυθρά στα διάφορα νοσοκομεία, ακόμη και στην ίδια χώρα(45).
Τα αίτια των αιμορραγιών στη Μαιευτική φαίνονται στον πίνακα 4(31). Μεταξύ 7 έως 37% των μεταγγίσεων ερυθρών στη Μαιευτική αφορούν σε περιπτώσεις προδρομικού πλακούντα και το 50% αυτών αντιμετωπίζονται με καισαρική τομή(32,46).
Τέσσερις μεγάλες μελέτες δείχνουν ευρήματα τα οποία ποικίλλουν. Έτσι: α) οι Clark και συν.(42) σε μία προοπτική ανάλυση 5.528 μητέρων βρήκαν αριθμό μεταγγίσεων για τοκετούς με σικύα (6,1%), σημαντικά υψηλότερο από εκείνους με εμβρυουλκούς (4,2%) και καισαρική τομή (1,4%). Αυτά τα ευρήματα διαφέρουν από άλλες μελέτες, στις οποίες οι τοκετοί με σικύα προκαλούν μικρότερη θνητότητα συγκρινόμενη με τους άλλους 2 τύπους τοκετού(32), β) οι Combss και συν.(47) σε μία ανάλυση 14.267 τελειόμηνων τοκετών βρήκαν ότι μετά από έλεγχο για διάφορες αιτίες αιμορραγίας δεν υπήρχε συσχέτιση μεταξύ μετάγγισης, προηγούμενης αιμορραγίας από τοκετό και προηγούμενης καισαρικής τομής, γ) Oι Camman και συν.(33) σε μία αναδρομική μελέτη 7.731 μητέρων βρήκαν ότι η ατονία της μήτρας και η κατακράτηση πλακούντα παρουσιάζονταν στο 44% όλων των μεταγγίσεων, με την προγεννητική αιμορραγία να ευθύνεται για το 12% των περιπτώσεων, δ) Oι Klapholzs συν.(48) σε μία ανάλυση 30.621 τοκετών έδειξαν ότι ανάμεσα σε άλλες ενδείξεις, η προηγούμενη αποβολή και το ολιγάμνιο ακολουθούνταν από ανεξήγητη υψηλή συχνότητα μεταγγίσεων.
Για προγραμματισμένους τοκετούς και καισαρικές τομές, η συχνότητα των μεταγγίσεων ποικίλλει από 1,5%-4,8% και 1,1%-6,4% αντίστοιχα(49). Η συχνότητα των μεταγγίσεων τελευταία πιθανόν μειώνεται, ώστε μία μελέτη δείχνει πτώση από 2,4% σε 1,1%, σε μία περίοδο πάνω από τέσσερα έτη(42).
ΓΥΝΑΙΚΟΛΟΓΙΑ
Η συχνότητα των διασταυρώσεων για υστερεκτομή αναφερόνταν σε 28% και τα ποσοστά μετάγγισης κυμαίνονταν μεταξύ 2,8%(50) και 8,6%(41). Η συχνότητα μετάγγισης για κοιλιακή υστερεκτομή αναφερόνταν στο 8,6%, συγκρινόμενη με 2,3% για κολπική υστερεκτομή. Oι Minz και συν.(51), επίσης, βρήκαν υψηλότερη συχνότητα μεταγγίσεων ανάμεσα σε γυναίκες με πυελικές φλεγμονώδεις νόσους και συμφύσεις, υφιστάμενες ολική υστερεκτομή (80%), και μεταξύ γυναικών που έχουν κολπορραφή ως μέρος της κολπικής υστερεκτομής, συγκρινόμενες με εκείνες τις γυναίκες που έχουν μόνο κολπική υστερεκτομή.
Πρόσφατα, σε ένα σύνολο 368 υστερεκτομών δεν αναφέρθηκε μετάγγιση αίματος σε καμιά από τις 55 κολπικές υστερεκτομές για πρόπτωση, ούτε στις 44 διορθωτικές επεμβάσεις που δεν πραγματοποιήθηκε υστερεκτομή(31). Στο 7,6% των κολπικών υστερεκτομών για μηνορραγία χρειάσθηκε μετάγγιση(32).
ΕΝΔΕΙΞΕΙΣ ΓΙΑ ΤΗΝ ΜΕΤΑΓΓΙΣΗ ΕΡΥΘΡΩΝ
Oι Μαιευτήρες - Γυναικολόγοι πρέπει να είναι ενήμεροι για τις ενδείξεις της μετάγγισης, ώστε οι ασθενείς να έχουν τα μέγιστα οφέλη με τους ελάχιστους κινδύνους. Ωστόσο, δεν υπάρχουν δημοσιεύσεις οδηγιών για τη χρήση της μετάγγισης ερυθρών στη Μαιευτική και Γυναικολογία(32). Oι Rosen και συν.(52), χρησιμοποιώντας τις αμερικανικές οδηγίες, καθόρισαν τη στρατηγική για τη χρήση των ερυθρών(53):
- οξεία απώλεια αίματος οποιουδήποτε ποσού, αν υπάρχει κλινική ένδειξη υποξυγοναιμίας,
- Hb <7g/dl (Ht 21%), αν δεν οφείλεται σε θεραπευτική αιτία,
- συμπτωματική αναιμία ανεξάρτητη του επιπέδου της Hb,
- ασθενείς λαμβάνοντες αναισθησία, εάν προεγχειρητικώς η Hb είναι <7g/dl,
- μεγάλη απώλεια αίματος κατά την εγχείρηση και Hb <10g/dl (Ht <30%).
Μια αναδρομική μελέτη(54) στη Victoria της Αυστραλίας, σχετικά με τις μεταγγίσεις σε καισαρικές τομές, αναφέρει μείωση αυτών κατά 50% όταν γίνονταν προσπάθειες εφαρμογής των παραπάνω προτάσεων(49,53). Oι περισσότερες τράπεζες αίματος χρησιμοποιούν στο μέγιστο, ως σταθερή πρακτική για ζήτηση αίματος, χειρουργικές προτάσεις, οι οποίες πάλι διαφέρουν μεταξύ νοσοκομείων. Για παράδειγμα, η τράπεζα αίματος του Bristol θα διασταυρώσει 4 μονάδες ερυθρών για μια ολική υστερεκτομή και καμία για μια καισαρική τομή. Τα περισσότερα χειρουργικά σχήματα αναπτύχθηκαν βάσει κλινικών ενδείξεων, αλλά μερικοί χρησιμοποίησαν μόνο διασταύρωση. Μια μελέτη έδειξε ότι η εισαγωγή της χρησιμοποίησης ελέγχου ομάδος - screening και χειρουργικού σχήματος παραγγελίας αίματος έχει ελαττώσει σημαντικά την παραγγελία μη απαραίτητου αίματος και τη χρήση του στη Μαιευτική και Γυναικολογία(55).
Oι Μαιευτήρες - Γυναικολόγοι του Βασιλικού Κολλεγίου (RCOG) προτείνουν τα παρακάτω κριτήρια για μετάγγιση σε καισαρική τομή: Hb <10g/dl, παρουσία αντισωμάτων έναντι ερυθρών, αιμορραγία κατά τον τοκετό, τρίτη ή και πλέον καισαρική, βαριά προεκλαμψία, αιμορραγική διάθεση, διάταση μήτρας οποιασδήποτε αιτίας και αποτυχών προγραμματισμένος τοκετός(56). Άλλοι συγγραφείς αναφέρουν τα παρακάτω κριτήρια για μεταγγίσεις αίματος: επίπεδο Hb, συμπτώματα αναιμίας, άλλοι παράγοντες νοσηρότητας, χρόνος νοσηλείας στο νοσοκομείο και βαθμός απώλειας αίματος(44).
ΜΑΙΕΥΤΙΚΕΣ ΑΙΜΟΡΡΑΓΙΕΣ
Oι φυσιολογικές μεταβολές κατά την κύηση, όπως π.χ. η αύξηση της μάζας των ερυθρών, του όγκου πλάσματος και η καρδιακή λειτουργία, αποτελούν αντισταθμιστικούς μηχανισμούς στην οξεία απώλεια αίματος κατά τον τοκετό(32). Oι μαιευτικές αιμορραγίες φαίνονται στον πίνακα 4(31). Σε απώλεια αίματος >15% (ή 750ml σε άτομο 64kg) συνιστώνται συνήθως κρυσταλλοειδή και κολλοειδή διαλύματα, ενώ σε απώλεια αίματος που συνεχίζεται (<1500ml) χορηγούνται τα παραπάνω διαλύματα και επιπλέον χορηγείται και αίμα. Καμιά σημαντική βλάβη δεν παρατηρείται όταν η Hb κυμαίνεται μεταξύ 6-8g/dl και υπάρχει ισοογκαιμία(57). Αξίζει επίσης να σημειωθεί ότι η μητρική θνητότητα λόγω μαιευτικής αιμορραγίας στην Αγγλία, μεταξύ 1991 και 1993, ήταν 6,4 ανά εκατομμύριο μητέρων(56).
ΚΑΙΣΑΡΙΚΗ ΤΟΜΗ
Oι Naef και συν.(49) βρήκαν ότι παρά το χαμηλό Ht μετά την καισαρική (μέση τιμή 23%) σε μη μεταγγιζόμενες ασθενείς, συγκρινόμενες με μεταγγιζόμενες (μέση τιμή Ht 28%), είχαν το ίδιο διάστημα νοσηλείας, τις ίδιες ενδείξεις μετεγχειρητικών λοιμώξεων και τις ίδιες επιπλοκές επούλωσης. Όμως, οι καισαρικές πριν τις 28 εβδομάδες κύησης ακολουθούνται με 14 φορές συχνότερη μετάγγιση, συγκρινόμενες με τις καισαρικές που γίνονται στο τέλος της κύησης(58). Υπάρχει απόδειξη ότι μόνο το 23% των μεταγγιζόμενων ασθενών, σε 43 ευρωπαϊκά κέντρα, είχαν πραγματική ένδειξη για μετάγγιση(45).
ΣΤΡΑΤΗΓΙΚΕΣ ΓΙΑ ΕΛΑΤΩΣΗ ΤΟΥ ΑΡΙΘΜΟΥ ΤΩΝ ΜΕΤΑΓΓΙΣΕΩΝ
Oι κίνδυνοι της μετάγγισης αίματος, αν και πιστεύεται ότι ελαττώνονται με την εφαρμογή ελέγχων και screening τεχνικών, είναι ακόμη σημαντικοί. Μαιευτήρες - Γυναικολόγοι πρέπει να γνωρίζουν τους κινδύνους, τις σχέσεις οφέλους από τις μεταγγίσεις ερυθρών στις ποικίλες κλινικές καταστάσεις, σε συνεργασία με τους Αναισθησιολόγους και Αιματολόγους(31,32). Oι τρεις κύριες ενδείξεις για μετάγγιση είναι η οξεία απώλεια αίματος κατά την εγχείρηση (κοιλιακή υστερεκτομή), η ερευνητική λαπαροτομία και η καισαρική τομή. Μη απαραίτητες μεταγγίσεις θα μπορούσαν να περιορισθούν με την τήρηση των απαραίτητων κριτηρίων(31,32,43).
ΝΟΣΟΙ ΠΟΥ ΜΕΤΑΔΙΔΟΝΤΑΙ ΜΕ ΜΕΤΑΓΓΙΣΗ ΑΙΜΑΤΟΣ
Τα λοιμογόνα αίτια που μπορούν να μεταδοθούν με το αίμα ή με τα παράγωγά του, είναι τα εξής: α) ιοί, β) βακτήρια (Treponema pallidum, Yersenia enterocolitica, γ) παράσιτα (Plasmodium sp. Filariasis Trypanosomiasis) και δ) η νόσος Creutzfeld - Jacob (CJD)(31,32,59).
1. HIV/AIDS
H HIV-πανδημία αντιπροσωπεύει την αρχή μιας νέας εποχής στην ιατρική και τη δημόσια υγεία. Η HIV-λοίμωξη είναι χρόνια, επίμονη, παγκόσμιας κατανομής, σεξουαλικά κυρίως μεταδιδόμενη νόσος και προχωρεί αργά (σε 10 έτη στη Δύση και σε 4,4 στην Αφρική), από μια ασυμπτωματική μορφή στη νόσο του AIDS. Υπολογίζεται ότι η μετάδοση μέσω σεξουαλικής επαφής ευθύνεται για το 80-95% των περίπου 42 εκατομμυρίων προσβεβλημένων από τον ιό HIV μέχρι σήμερα. Το AIDS παραμένει μία θανατηφόρος νόσος, παρά τη σημαντική μείωση της θνητότητας από τον επιτυχή συνδυασμό της θεραπείας με νουκλεοτιδικά ανάλογα και με αναστολείς της πρωτεάσης. Όμως, ο ρυθμός της αύξησης της HIV-λοίμωξης θα επηρεαστεί σημαντικά από το βαθμό επιτυχίας στην αποτροπή της σεξουαλικής, παρεντερικής, περιγεννητικής και διαπλακούντιας μετάδοσης του ιού. Η συχνότητα μόλυνσης στη Δύση είναι 1/250 ενήλικες (40% είναι γυναίκες), ενώ στην Ανατολική και Κεντρική Αφρική 30% και πλέον των εγκύων έχουν μολυνθεί. Όσον αφορά στην επίδραση της κύησης στο ρυθμό εξέλιξης της νόσου, το θέμα δεν έχει πλήρως επιλυθεί. Παρατηρείται αύξηση των αυτόματων εκτρώσεων, των προώρων και των χαμηλού βάρους νεογνών. Η κάθετη μετάδοση του ιού στο έμβρυο υπολογίζεται στο 15-20% στην Ευρώπη, στο 15-30% στις ΗΠΑ και στο 25-35% στην Αφρική. Η χρήση ZDV κατά την κύηση (πρωτόκολλο ACTG 076) προφυλάσσει το νεογνό από τη λοίμωξη κατά 68%. Επειδή τα 2/3 της μετάδοσης του ιού συμβαίνουν περιγεννητικά, είναι αντικρουόμενα τα βιβλιογραφικά δεδομένα όσον αφορά στη διενέργεια καισαρικής τομής ή φυσιολογικού τοκετού. O κίνδυνος μετάδοσης είναι τόσο μεγαλύτερος, όσο ο αριθμός των γυναικών που μολύνονται από ετεροσεξουαλική σχέση αυξάνει. Η αντι-ιική θεραπεία σχετίζεται με μείωση κατά 50% στη σεξουαλική μετάδοση του HIV. Η παρουσία λοίμωξης του γεννητικού συστήματος, όπως λοίμωξη από χλαμύδια, γονόρροια και τριχομονάδα, σχετίζεται με αύξηση κατά 60-340% της συχνότητας λοίμωξης από τον ιό και η περιτομή προφυλάσσει κατά 8 φορές τους άρρενες από την HIV-λοίμωξη, ενώ η εμμηνορρυσία αυξάνει τη συχνότητα λοίμωξης κατά 3,4 φορές. Χωρίς προγράμματα για την πρόληψη και τον έλεγχο του AIDS, είναι πιθανό η εξάπλωση της HIV-λοίμωξης να είναι τεράστια, ειδικότερα στην υπό τη Σαχάρα Ανατολική, Κεντρική Αφρική και ΝΑ Ασία και να έχει μια βαθιά επίδραση στην ιατρική, οικονομική και πολιτιστική δομή των εθνών για τα προσεχή χρόνια(60-62).
Ειδικότερα, κατά το έτος 2002 υπήρξαν 5 εκατ. νέες περιπτώσεις HIV λοίμωξης (HIV-1, HIV-2) και απεβίωσαν 3,1 εκατ. από AIDS. Στην υπό Σαχάρα Αφρική, οι νέες περιπτώσεις HIV λοίμωξης ανήλθαν στα 3,5 εκατ. και οι θάνατοι από AIDS στα 2,4 εκατ., ενώ στην Ασία, ο συνολικός αριθμός φορέων και πασχόντων ανήλθε σε 7,2 εκατ.(62).
Με την υποχρεωτική, από το 1985 σε παγκόσμια κλίμακα, εξέταση των αντισωμάτων έναντι του ιού HIV, παρατηρήθηκε θετικότητα για τον ιό HIV στον ορό των δοτών αίματος της Ευρώπης ως εξής: Δανία 0,001%, Μεγάλη Βρετανία 0,002%, Γερμανία 0,003%, Σουηδία 0,157%, Ισπανία 0,180%, Γαλλία 0,920%, όπου αργότερα κατήλθε στο 0,051%(59) και στην Ελλάδα 0,019%(63). Με τον έλεγχο του ιού HIV με το αντιγόνο p24 (Ag), ο υπολειπόμενος κίνδυνος για λοίμωξη(64) μειώθηκε κατά 27%.
2. Ανθρώπινος Τ-λεμφοτροπικός ιός τύπου 1 (HTLV-1) και τύπου 2 (HTLV-2)
Ιός HTLV-I
O HTLV-I αποδείχθηκε, με ορολογικές και μοριακές μεθόδους, ως η αιτία της λευχαιμίας - λεμφώματος και της πάρεσης από Τ-λεμφοκύτταρα των ενηλίκων (ATL), μιας νόσου που χαρακτηρίζεται από κακοήθη αύξηση των CD4+ Τ-λεμφοκυττάρων και συμπτώματα υπερασβεστιαιμίας, λεμφαδενοπάθειας και ανοσοανεπάρκειας(65). Η πρόγνωση της νόσου είναι κακή, με μέση επιβίωση μόνο λίγων μηνών από τη διάγνωση. Μόνο το 2-5% των ατόμων που έχουν μολυνθεί από τον HTLV-1 αναπτύσσουν ATL, με μια λανθάνουσα περίοδο αρκετών δεκαετιών μετά τη λοίμωξη. Ένα ιδιαίτερο χαρακτηριστικό των λευχαιμικών κυττάρων των ασθενών αυτών είναι η απουσία ανιχνεύσιμης έκφρασης των ιικών γονιδίων, κάτι που δείχνει ότι ίσως δεν απαιτείται η συνεχής έκφραση των γονιδιακών προϊόντων του ιού για τη διατήρηση του κακοήθους φαινοτύπου. O HTLV-1 κωδικοποιεί ένα ογκογονίδιο, το Tax, που ενοχοποιείται για την απορύθμιση της κυτταρικής αύξησης μέσω επαγωγής της έκφρασης των σχετικών με την αύξηση γονιδίων, όπως είναι το fos, και συγκεκριμένων λεμφοκινών(66).
3. Ιός HIV-II
Η αυξημένη συχνότητα μερικών όγκων σε ασθενείς με HIV-λοίμωξη είναι σχεδόν βέβαιο ότι οφείλεται στη χρόνια ανοσοκαταστολή της νόσου και όχι σε κάποια άμεση ογκογόνο δράση του HIV(61,65). Oι μελέτες των τύπων των όγκων που εμφανίζονται σΥ αυτούς τους ασθενείς δίνουν σαφή στοιχεία για το ρόλο των ιών στον καρκίνο και την τάση των καρκίνων που σχετίζονται με ιούς να αναπτύσσονται σε συνθήκες ανοσοκαταστολής. Εκτός από την αυξημένη συχνότητα των σχετικών με τον Epstein-Barr (EBN) ανοσοβλαστικών λεμφωμάτων και του σαρκώματος Kaposi σε ασθενείς με HIV-λοίμωξη, η υπόθεση της ανάμιξης ιών στην καρκινογένεση ενισχύεται και από την πρόσφατη παρατήρηση ότι οι πρωκτογεννητικοί καρκίνοι που έχουν σχέση με τους ιούς του θηλώματος (HPV)(67), κυρίως του τραχήλου στις γυναίκες και του πρωκτού στους άνδρες, είναι συχνότεροι σε ασθενείς με HIV-λοίμωξη(61).
Τονίζεται ότι η μετάγγιση, σχετιζόμενη με τη μετάδοση των παραπάνω ιών, μπορεί να καταλήξει εκτός των άλλων, σε τροπική σπαστική πάρεση των κάτω άκρων (Tropical spastic paraparesis-TSP) και μυελοπάθεια (HTLV-1 associated myelopathy, HAM) από ένα μήνα έως 4 έτη μετά τη μετάδοση(59,68,69). Προς αποφυγή της μετάδοσης των HTLV-Ι/II ιών μέσω της μετάγγισης, επιβάλλεται η υποχρεωτική εξέταση των δοτών αίματος στην Ιαπωνία, τις ΗΠΑ και σε αρκετές ευρωπαϊκές χώρες(64). Η σημειωθείσα επίπτωση των αναφερόμενων ιών ήταν 0,043% στις ΗΠΑ και μεταξύ 0,001 έως 0,005% στην Ευρώπη. Εκτιμάται ότι ο κίνδυνος είναι 1/6.000.000 δοτών αίματος στη Γαλλία και 1/641.000 στις ΗΠΑ(59,70).
4. Ηπατίτιδα Α
Η ηπατίτιδα Α προκαλείται από έναν RNA ιό. O χρόνος επώασης κυμαίνεται από 15 έως 50 ημέρες (ΜΤ 28-30 ημέρες). Τα κόπρανα περιέχουν την υψηλότερη συγκέντρωση σωματιδίων του ιού και η έκκριση του ιού φθάνει στο μέγιστο αργά στην περίοδο επώασης και πρώιμα στην πρόδρομη φάση της νόσου. Η διάρκεια της ιαιμίας είναι σύντομη και ο ιός φυσιολογικά δεν εκκρίνεται στα ούρα ή σε άλλα σωματικά υγρά. Λόγω της βραχείας παραμονής των ιών στο αίμα δεν μεταδίδεται γενικά με τη μετάγγιση αίματος. Έχουν αναφερθεί επιδημίες μικρού βαθμού σε μεταγγιζόμενους αιμορροφιλικούς, στους οποίους και συνιστάται εμβολιασμός(71,72).
5. Ηπατίτιδα Β
Η ηπατίτιδα Β προκαλείται από έναν μικρό DNA ιό. O ανέπαφος ιός αποκαλείται σωματίδιο του Dane. O ιός της ηπατίτιδας Β περιέχει τρία κύρια αντιγόνα. Το αντιγόνο επιφανείας της ηπατίτιδας Β (HBsAg) βρίσκεται στην επιφάνεια του ιού και κυκλοφορεί και ελεύθερο στον ορό, σε σφαιρικές και σε νηματοειδείς μορφές. Το μεσαίο τμήμα του σωματιδίου του Dane περιέχει το αντιγόνο του πυρήνα της ηπατίτιδας Β (HBcAg). Το αντιγόνο του πυρήνα βρίσκεται μόνο στα ηπατοκύτταρα και δεν κυκλοφορεί στο αίμα. Το αντιγόνο e της ηπατίτιδας Β (HBeAg) κωδικοποιείται από το ίδιο τμήμα του γονιδιώματος του ιού που κωδικοποιεί και το αντιγόνο του πυρήνα. Η παρουσία του HBeAg φανερώνει εξαιρετικά υψηλό ιικό φορτίο και ενεργό πολλαπλασιασμό του ιού(71,73).
Μόλυνση από ηπατίτιδα Β συμβαίνει παγκοσμίως. Στις Ηνωμένες Πολιτείες ευθύνεται για το 40-50% όλων των περιπτώσεων ηπατίτιδας. Περίπου 300.000 νέες περιπτώσεις ηπατίτιδας Β εμφανίζονται ετησίως και περισσότεροι από ένα εκατομμύριο Αμερικάνοι είναι χρόνιοι φορείς. Oξεία ηπατίτιδα Β παρατηρείται σε 1-2/1.000 κυήσεις. Χρόνια λοίμωξη βρίσκεται σε 5-15/1.000 κυήσεις(73), αλλά είναι πιο διαδεδομένη σε συγκεκριμένες φυλετικές ομάδες (π.χ. Ασιάτισσες, Εσκιμώες).
O ιός της ηπατίτιδας Β μεταδίδεται με την παρεντερική οδό και με τη σεξουαλική επαφή. Μεγαλύτερο κίνδυνο να μολυνθούν διατρέχουν τα άτομα με πολλούς ερωτικούς συντρόφους, άτομα που χρησιμοποιούν φάρμακα διαδερμικά, ή που έχουν ερωτικούς συντρόφους οι οποίοι ανήκουν σε κάποια από τις παραπάνω κατηγορίες υψηλού κινδύνου. Άλλοι σημαντικοί παράγοντες κινδύνου είναι η λήψη παραγώγων αίματος και η οικιακή ή η ιδρυματική επαφή.
Όλοι οι δότες αίματος ελέγχονται για HBsAg. Επομένως, η μετάδοση ηπατίτιδας Β με μετάγγιση αίματος ή παραγώγων του είναι σπάνια(71). Η χρήση ναρκωτικών είναι ένας σημαντικός παράγοντας κινδύνου για την οριζόντια μετάδοση του ιού της ηπατίτιδας Β. Η σεξουαλική επαφή είναι ένας ικανός μηχανισμός διάδοσης του ιού. Περίπου το 25% των τακτικών ερωτικών συντρόφων των προσβεβλημένων ατόμων έχουν και αυτοί καταστεί οροθετικοί.
Η θνητότητα που συσχετίζεται με την οξεία ηπατίτιδα Β είναι περίπου 1%. Από τους ασθενείς που μολύνονται, το 85-90% εμφανίζουν πλήρη υποχώρηση των συμπτωμάτων τους και αναπτύσσουν προστατευτικά επίπεδα αντισωμάτων. Το υπόλοιπο 10-15% των ασθενών καθίστανται χρόνιοι φορείς, συνεχίζουν να έχουν ανιχνεύσιμες συγκεντρώσεις HBsAg στον ορό, αλλά είναι ασυμπτωματικοί και δεν έχουν καμία βιοχημική ένδειξη ηπατικής δυσλειτουργίας. Σε 15-30% αυτών των χρόνιων φορέων, ο πολλαπλασιασμός του ιού συνεχίζεται και αυτό γίνεται εμφανές από την εμμονή του αντιγόνου e και την ενεργό σύνθεση του DNA του ιού. Αυτά τα άτομα κινδυνεύουν να αναπτύξουν στη συνέχεια χρόνια ή ανθεκτική ηπατίτιδα και κίρρωση, ενώ περίπου 4.000-5.000 πεθαίνουν ετησίως από επιπλοκές χρόνιας ηπατικής νόσου, συμπεριλαμβανομένου του ηπατοκυτταρικού καρκινώματος(74,75).
Επειδή ο ιός της ηπατίτιδας Β είναι υψηλά παθογόνος και μολυσματικός, η περιγεννητική μετάδοση της λοίμωξης συμβαίνει με σημαντικά υψηλή συχνότητα. Περίπου το 10-20% των γυναικών που είναι οροθετικές για το HBsAg μεταδίδουν τον ιό στα νεογνά τους, εφόσον δεν εφαρμοσθεί ανοσοπροφύλαξη. Σε γυναίκες που είναι οροθετικές και για το HBsAg και για το HBeAg, η συχνότητα κάθετης μετάδοσης αυξάνει περίπου στο 90%.
Σε ασθενείς με οξεία ηπατίτιδα Β, η συχνότητα κάθετης μετάδοσης εξαρτάται επίσης από το χρόνο της κυοφορίας στον οποίο συμβαίνει η μόλυνση της μητέρας. Όταν η μητρική μόλυνση γίνεται κατά το πρώτο τρίμηνο, ποσοστό μέχρι 10% των νεογνών θα είναι οροθετικά για HbsAg(71). Σε γυναίκες που μολύνονται οξέως κατά το τρίτο τρίμηνο, το 80-90% των απογόνων θα είναι προσβεβλημένοι.
Ένα ποσοστό μεταξύ 85% και 95% των περιπτώσεων της περιγεννητικής μεταβίβασης του ιού της ηπατίτιδας Β συμβαίνει ως αποτέλεσμα της ενδοπεριτοναϊκής έκθεσης του παιδιού σε μολυσμένο αίμα ή στις εκκρίσεις του γεννητικού σωλήνα. Oι υπόλοιπες περιπτώσεις είναι αποτέλεσμα αιματογενούς διαπλακουντιακής διασποράς, θηλασμού και στενής μετά τον τοκετό επαφής ανάμεσα στο παιδί και τον μολυσμένο γονέα. Παιδιά γυναικών που είναι θετικές για το HBsAg κατά το χρόνο του τοκετού θα πρέπει να λαμβάνουν τόσο άνοσο σφαιρίνη κατά της ηπατίτιδας Β (HBIG), όσο και το εμβόλιο της ηπατίτιδας Β μέσα σε 12 ώρες από τη γέννηση και να ακολουθήσουν άλλες δύο δόσεις του εμβολίου της ηπατίτιδας Β μέσα στους πρώτους έξι μήνες της ζωής τους.
Στην Ελλάδα, στις αρχές του 1970, το ποσοστό των φορέων HbsAg ήταν 4,1%, με μια επικράτηση της λοίμωξης HBV στο 26,5%, ενώ το 2000 έφθασε στο 0,9%(76). Από το 1988 εφαρμόζεται εμβόλιο για την ηπατίτιδα Β. Oι Ταμπακούδης και συν.(77) εξέτασαν όλες τις έγκυες που γέννησαν στην ΑΥ Μ/Γ κλινική του ΑΠΘ, κατά τη διάρκεια του 1991, για την παρουσία HBsAg. Σε όσες περιπτώσεις δεν υπήρξε έλεγχος κατά την κύηση, αυτός έγινε μετέπειτα, κατά την εισαγωγή στην κλινική. Σε σύνολο 1.206 εγκύων βρέθηκαν 41 περιπτώσεις (3,4%) με HBsAg (+) θετικό. Από τις 41 περιπτώσεις, οι 26 (63,5%) είχαν ελεγχθεί κατά την κύηση, ενώ οι 15 (36,5%) κατά την εισαγωγή τους στην κλινική. Από τις 41 περιπτώσεις μόνο οι 25 (16%) είχαν στο ιστορικό τους παράγοντα κινδύνου (ενδημικό περιβάλλον: 11/25 - 44%, ιστορικό ηπατίτιδας: 7/25 - 28%, μετάγγιση αίματος: 3/25 - 12%, ναρκωτικά: 2/25 - 8%, τατουάζ: 2/25 - 8%).
Σε όλα τα νεογέννητα έγινε συνδυασμένη ανοσοπροφύλαξη (ανοσοσφαιρίνη και εμβόλιο) σύμφωνα με τις οδηγίες της ACIP, ενώ διακόπηκε η γαλουχία στο σύνολο των γυναικών.
Συμπερασματικά, φαίνεται ότι: α) το ποσοστό των HBsAg (+) θετικών μητέρων είναι σημαντικά υψηλότερο του αντίστοιχου των δυτικών χωρών, β) σημαντικό ποσοστό οροθετικών μητέρων δεν έχουν γνωστό παράγοντα κινδύνου στο ιστορικό τους, γ) σημαντικό ποσοστό εγκύων δεν ελέγχονται κατά την κύηση και δ) το υψηλό ποσοστό οροθετικότητας επιβάλλει την εφαρμογή προγραμμάτων πληθυσμιακού ελέγχου στον ελλαδικό χώρο.
6. Ηπατίτιδα C
O ιός της ηπατίτιδας C (HCV) αποτελεί το κυριότερο αίτιο της ηπατίτιδας non-A/non-B. Αναγνωρίζεται ότι ο ιός της ηπατίτιδας C αποτελεί τη συχνότερη αιτία χρόνιας ηπατίτιδας (25-40%) και ιογενούς ηπατίτιδας μετά από μετάγγιση (90%) στο δυτικό κόσμο. Προκαλεί κίρρωση ήπατος και ηπατοκυτταρικό καρκίνωμα, ενώ στο 75% των περιπτώσεων η πορεία της νόσου είναι ασυμπτωματική. O ιός εμφανίζει 6 γονότυπους και 11 υπότυπους. Στους τρόπους μετάδοσης ανήκουν η χρήση ενδοφλέβιων ναρκωτικών (26,7%), η μετάγγιση αίματος (11,9%), η σεξουαλική μετάδοση (10%), η κάθετη μετάδοση (5,2% και σε συνύπαρξη HIV 23,4%) και τέλος, άγνωστη αιτιολογία σε σημαντικό ποσοστό (40-50%). Η ανίχνευση των αντισωμάτων του ιού πραγματοποιείται σε 8-12 εβδομάδες μετά τη λοίμωξη με τη μέθοδο ELISA, κυρίως όμως με τη μέθοδο RIBA, η δε ιαιμία με τη μέθοδο PCR. Πρόσφατα αναφέρθηκε ότι, ο κίνδυνος των νεογνών για HCV που ήταν 10% αυξήθηκε σε 36%, εφόσον τα βρέφη γεννήθηκαν από HIV-αρνητικές μητέρες με τίτλο HCV-RNA ³106αντίγραφα/ml, ενώ κανένα νεογνό δε μολύνθηκε από μητέρα με τίτλο HCV-RNA ²104αντίγραφα/ml. Δεν έχει αποδειχτεί μετάδοση με το μητρικό θηλασμό (HCV-RNA 101-104αντίγραφα/ml). Τα αντι-HCV αντισώματα διαπερνούν τον πλακούντα και παραμένουν στο βρέφος για 15 μήνες. Εμβόλιο για προφύλαξη από τον ιό δεν υπάρχει, λόγω της ιικής ετερογένειας και του υψηλού ποσοστού μεταλλάξεων στον ιό. Συνήθως τα παιδιά αναπτύσσουν προοδευτικά χρόνια ηπατίτιδα με σχετική καλοήθη πορεία. Η ύπαρξη ιαιμίας και επίμονων HCV-αντισωμάτων στα παιδιά πέραν των 18 μηνών, ή η de novo παραγωγή αυτών, είναι ενδεικτική λοίμωξης. Η θεραπεία εκτός εγκυμοσύνης μπορεί να γίνει με IFN-α, ριμπαβερίνη, ή συνδυασμό των δύο(78).
Η επικράτηση των θετικών ορών (Anti-HCV) μεταξύ των δωρητών αίματος ήταν 0,2-0,8% στη Βόρεια Ευρώπη, 0,5-1,7% στη Νότια Ευρώπη, 0,4-0,6% στις ΗΠΑ και 1-1,5% στην Ιαπωνία(59,79). Oι πληροφορίες για την επικράτηση του HCV στους δωρητές αίματος δεν αντανακλούν απαραίτητα αυτήν του γενικού πληθυσμού, από τη στιγμή που οι δότες αίματος επιλέγονται με αποκλεισμό των παραγόντων κινδύνου για ιούς που αναπτύσσονται στο αίμα. Συνεπώς, η επικράτηση του HCV στο γενικό πληθυσμό είναι πιθανό να είναι υψηλότερη. Στην Ελλάδα, το ποσοστό των οροθετικών HCV στους δωρητές αίματος είναι 0,2-0,4%, περισσότερο όμοιο με αυτό στη Βόρεια Ευρώπη παρά με τις άλλες γειτονικές μας χώρες(59,76).
7. Ηπατίτιδα D
Η ηπατίτιδα D απαιτεί την παρουσία του ιού της ηπατίτιδας Β για πολλαπλασιασμό και έκφραση, επομένως επισυμβαίνει μόνο σε άτομα που έχουν ήδη ηπατίτιδα Β. Στην οξεία ηπατίτιδα Β, μόλις γίνει η κάθαρση του HBsAg από το αίμα, γίνεται και για την ηπατίτιδα D. Περίπου το 20-25% των χρόνιων φορέων του ιού της ηπατίτιδας Β τελικά επιμολύνονται από τον ιό της ηπατίτιδας D(80). Στην οξεία ηπατίτιδα D επικρατούν τα IgM αντισώματα, ενώ IgG αντισώματα μπορούν να βρεθούν σε χρόνιες λοιμώξεις.
Η χρόνια ηπατίτιδα D προκαλεί σοβαρή νόσο συχνότερα από τις άλλες μορφές χρόνιας ηπατίτιδας. Από τους ασθενείς με ηπατίτιδα D, το 70-80% τελικά αναπτύσσουν κίρρωση και πυλαία υπέρταση, 15% των οποίων εμφανίζουν μία ασυνήθιστα ταχεία εξέλιξη προς κίρρωση μέσα σε δύο έτη από την έναρξη της οξείας νόσου. Η θνητότητα λόγω της ηπατικής ανεπάρκειας φθάνει το 25%(80,81). Αντίθετα, μόνο ένα ποσοστό 15-30% των ασθενών με χρόνια ηπατίτιδα Β αναπτύσσει κίρρωση και πυλαία υπέρταση, με την εξέλιξη της νόσου να είναι τυπικά πολύ πιο βραδεία. Κάθετη μετάδοση του ιού της ηπατίτιδας D έχει αποδειχθεί. Η μετάδοση δεν είναι συχνή, διότι τα μέτρα που χρησιμοποιούνται για την πρόληψη της περιγεννητικής λοίμωξης από τον ιό της ηπατίτιδας Β είναι, σχεδόν χωρίς εξαιρέσεις, αποτελεσματικά και στην πρόληψη της μετάδοσης της ηπατίτιδας D.
8. Ηπατίτιδα Ε
Oι επιδημιολογικοί χαρακτήρες της ηπατίτιδας Ε είναι παρόμοιοι με αυτούς της ηπατίτιδας Α. Λόγω της παροδικής αυξημένης παρουσίας στο αίμα, ο κίνδυνος μετάδοσης με μετάγγιση στις δυτικές χώρες είναι εξαιρετικά χαμηλός(82).
9. Ηπατίτιδα G
Η ηπατίτιδα G είναι πιο πιθανό να εμφανισθεί σε ανθρώπους που ήδη πάσχουν από ηπατίτιδα Β ή C. Απεδείχθη ότι ο ιός HGV μεταδίδεται με μετάγγιση αίματος καθώς και από τη μητέρα στο έμβρυο. Η επίπτωση του HGV στις χώρες της Δύσης κυμαίνεται μεταξύ 0,9 και 4,7(83).
10. Ανθρώπειος ιός Parvo B19
O ανθρώπειος ιός Parvo B19 ταυτοποιήθηκε το 1975 και έκτοτε η γνώση γύρω από αυτόν έχει εμπλουτισθεί, ιδιαίτερα με την ανοσοηλεκτροφόρηση για το επιφανειακό αντιγόνο της ηπατίτιδας Β. Πήρε το όνομά του από τη θέση της «ψευδούς θετικής» γραμμής στην πηκτή της ηλεκτροφόρησης. Δεν γνωρίζουμε την ύπαρξη άλλων ανθρώπειων παρβοϊών. Πολλές είναι οι ασθένειες που συνδέονται με τον ιό Β19, όπως για παράδειγμα αιμολυτικές κρίσεις σε έδαφος χρόνιας αιμολυτικής αναιμίας, λοιμώδες ερύθημα, αρθρίτιδα, χρόνιες αναιμίες σε ανοσοκατασταλμένους, νεκρωτική αγειΐτιδα και γενικευμένο οίδημα. Oι συνέπειες της μητρικής λοίμωξης από τον παρβοϊό στο έμβρυο περιλαμβάνουν ύδρωπας, αναιμία, μυοκαρδίτιδα και θάνατο. Η λοίμωξη του νεογνού συσχετίζεται με ηπατίτιδα και με αναιμία λόγω μετάγγισης(84). Η επίπτωση στους δότες αίματος είναι 1/3.300 έως 1/40.000 περιπτώσεις(85). Oι Kyriazopoulou και συν.(86) αναφέρουν επίπτωση των IgG αντισωμάτων, έναντι του ιού Parvo B19 στο θήλυ ελληνικό πληθυσμό (18-45 ετών), σε ποσοστό 57,8%.
11. Ανθρώπειος ιός έρπητα τύπου 8 (HHV-8)
O HHV-8 είναι ένας gamma ιός του έρπητα που βρέθηκε σε πάσχοντες από HIV με σάρκωμα Kaposi(59-61). Η επίπτωσή του στους δότες αίματος από την Ανατολική Αφρική, τη Νότιο Ιταλία και την Ελλάδα, ανέρχεται στο 15-50%(87), ενώ στη Δύση ανέρχεται στο 0-5% και στις ΗΠΑ στο 20%(88).
12.TTV
O TTV είναι ένας μικρός, κυκλικός, άνευ περιτύλιξης DNA ιός, με δύο ανοιχτά πλαίσια ανάγνωσης και αναγνωρίστηκε το 1997(59). Η επίπτωσή του στους δότες αίματος κυμαίνεται από 1,9% έως 80% και δεν σχετίζεται με ηπατίτιδα. Oι χρόνιοι φορείς παρουσιάζουν φυσιολογική λειτουργία του ήπατος(89,90).
13. Κυτταρομεγαλοϊός (CMV)
O CMV είναι ένας δίκλωνος ενδοκυττάριος DNA ιός που απαντά στα λευκοκύτταρα του περιφερικού αίματος. Η επίπτωση στους δότες αίματος ανέρχεται στο 20% έως το 80%(91). Σε περιπτώσεις ανοσοανεπάρκειας, η λοίμωξη με CMV προκαλεί συγγενείς ανωμαλίες στο έμβρυο και ενδεχομένως θάνατο στην έγκυο γυναίκα. Μονάδες αίματος CMV(-) διατίθενται σε υψηλού κινδύνου ασθενείς και σε έγκυες γυναίκες(32).
14. Σύφιλη
Η σύφιλη οφείλεται στην ωχρά σπειροχαίτη (Treponema Pallidum), αποτελεί σεξουαλικά μεταδιδόμενο νόσημα και είναι η πρώτη νόσος που αναφέρεται ότι μεταδίδεται με τη μετάγγιση αίματος. Σήμερα, ο κίνδυνος μετάδοσης λόγω της αποθήκευσης του αίματος στους 4oC περισσότερο από 72 ώρες έχει αντικειμενικά εξαλειφθεί(92-94).
Η διαγνωστική προσέγγιση στη συφιλιδική έγκυο είναι κλινική, ορολογική και βακτηριολογική, στο έμβρυο είναι υπερηχογραφική και ενδεχομένως βιολογική (εφαρμογή PCR στο αμνιακό υγρό), ενώ στο νεογέννητο κλινική, υπερηχογραφική, ακτινολογική και ορολογική. Η κλασική θεραπεία, τόσο της μητρικής όσο και της συγγενούς σύφιλης, είναι η πενικιλίνη.
Oι Ταμπακούδης και συν.(95) αναφέρουν περίπτωση μητρικής και συγγενούς σύφιλης, όπου πρωτότοκος έγκυος 22 ετών, ευρισκόμενη στην 33η εβδομάδα της κύησης, με υδράμνιο, υποβλήθηκε σε καισαρική τομή λόγω αλλοίωσης παλμών και γέννησε ένα ζων θήλυ νεογνό, βάρους 2.745g, με Apgar scores 1 και 5, στο 1ο και 5ο λεπτό. Το νεογνό εμφάνισε σοβαρό ύδρωπα και σύνδρομο αναπνευστικής δυσχέρειας, γενικευμένο εξάνθημα, αποφολιδωτικές πλάκες στην πρόσθια επιφάνεια του κορμού, των άνω και κάτω άκρων, καθώς και ηπατοσπληνομεγαλία. H CT εγκεφάλου έδειξε ισχαιμικές βλάβες, η ακτινογραφία οστών μεταφυσίτιδα και η ορολογική έρευνα σύφιλη. Το νεογνό έλαβε για 14 ημέρες αντιβίωση και συστήθηκε έλεγχος του εγκεφαλονωτιαίου υγρού με VDRL.
15. Ελονοσία
Oφείλεται στο Plasmodium SP, αριθμεί σε παγκόσμια κλίμακα 300-500 εκατ. πάσχοντες και ο κίνδυνος λόγω μετάγγισης απαντά στις περιοχές όπου ενδημεί, όπως και η φυλαρίαση, καθώς και η τρυπανοσωμίαση(31,96).
16. Βρουκέλλωση
Αποτελεί κίνδυνο μετάδοσης λόγω μετάγγισης στις περιοχές όπου ενδημεί(59).
17. Βακτηριακή μόλυνση
Η επίπτωση στους δέκτες ερυθρών είναι 1/1.000.000. Τα συνήθη αίτια είναι η Pseudomonas spp και η Yersinia enterocolitica(32,59,97). Η επίπτωση στους δέκτες αιμοπεταλίων είναι υψηλή (1/10.000 μεταγγίσεις). Τα συνήθη αίτια είναι οι σταφυλόκοκκοι, η σαλμονέλα, η Serratia marcescens και το Enterobacter spp. Η σηψαιμία λόγω μετάγγισης αίματος φθάνει στο 35%(99).
18. Νόσος των Creutzfeldt - Jacob (CJD)
H CJD αναφέρεται ως ανθρώπινη σπογγώδης εγκεφαλοπάθεια και διακρίνεται σε σποραδική, κληρονομική και επίκτητη. Είναι νόσος νευροεκφυλιστική, οφειλόμενη σε συσσώρευση στον εγκέφαλο της prion πρωτεΐνης και μακρού χρόνου επώασης. Το 1996 περιγράφηκε μια νέα ανθρώπινη prion νόσος (vCJD), η παραλλαγμένη CJD(59,100).
O Παγκόσμιος Oργανισμός Υγείας (WHO) προτείνει να αποκλειστούν μόνιμα άτομα τα οποία: α) υποφέρουν από CJD, vCJD ή παραφροσύνη, β) έχουν λάβει παράγωγα από ανθρώπινους αδένες (αυξητική ορμόνη και γοναδοτροπίνη), ή που έχουν αποτελέσει δέκτες σκληρής μήνιγγος ή παραγώγων του κερατοειδούς και γ) με οικογενειακό ιστορικό κλασικής CJD. Επιπλέον, στις ΗΠΑ και στην ΕΕ, τα παράγωγα πλάσματος αποσύρονται αν ένας δότης αίματος είναι ύποπτος βάσιμα πως έχει vCJD(59,101).
Summary
Blood transfusion in Obstetrics and Gynecology Risks.
Tampakoudis P, Tampakoudis G, Bontis J
1st Department of Obstetrics and Gynecology
Aristotle University of Thessaloniki
Ippokrateion Hospital
Hellen Obstet Gynecol 15(2): 103-118, 2003
Transfusion of whole blood or blood products is a basic therapeutic factor. The need for blood transfusion in obstetrical patients is common, variable and has the following frequency: in patients with iron-deficiency anemia and vaginal delivery 0.37%, in cases of cesarean section 6.8%, in severe heterozygous §-thalassemia life-long 1-2 units of blood (300 ml each unit) every month, and even more during pregnancy. In gynecological patients, the frequency of transfusion in vaginal hysterectomy is 2.3%, in total abdominal hysterectomy 2.8-8.6%, while in women with inflammatory disease and adhesions the frequency is increased. Reactions to transfusion are: immunosuppression cardiac pulmonary edema and mainly the risk of disease transmission. The main infectious agents are the following: a) viruses (HIV-1/2, HTLV-I/II, HAV, HBV, HCV, HDV, HEV, HGV, TTV, CMV, HHV-8, Parvo B19, b) bacteria (Treponema pallidum, Yersinia enterocolitica), c) parasites (plasmodium SP, Filariasis, Trypanosomiasis), and d) Creutzfeld-Jacob Disease (CJD). The long-term target is reduction of the frequency and the quantity of transfused blood and disease prevention with modern molecular biological methods.
Key words: Blood transfusion, Obstetrics, Gynecology, risks.
Βιβλιoγραφία
1. Sharma JB. Nutritional anaemia during pregnancy in non-industrialised countries. In Progress in Obstetrics and Gynaecology, edited by Studd J, vol. 15, Churchill Livingstone, Edinburgh London New York, Philadelphia, St Luis, Sydney, Toronto 2003; 103-122.
2. WHO/UNICEF/UNU. Indicators for Assessing Iron Deficiency and Strategies for its Prevention: WHO draft. Geneva: WHO, 1996.
3. Schwartz WJ, Thurnau GR. Iron deficiency anaemia in pregnancy. Clin Obstet Gynecol 1995; 38:443-454.
4. Diejomaeoh FME, Abdulaziz A, Adekile AD. Anemia in pregnancy. Int J Gynecol Obstet 1999; 65:299-301.
5. Kulier R, de Onis M, Gulmezoglu AM, Villar J. Nutritional interventions for the prevention of maternal morbidity. Int J Gynecol Obstet 1998; 63:231-246.
6. World Health Organization. Revised 1990 Estimates of Maternal Mortality. WHO / FRH / MSM / 96.1. Geneva: WHO, 1996.
7. Turmen T, AbouZahr C. Safe motherhood. Int J Gynecol Obstet 1994; 46:145-153.
8. Viteri FE. The consequences of iron deficiency and anaemia in pregnancy. Adv Exp Med Biol 1994; 352:127-139.
9. Hoffbrand AV, Pettit JE. Clinical Haematology, Second Edition, Sandoz Atlas, Mosby-Wolfe, Basle, Switzerland 1994; p:1-122.
10. Sharma JB. Medical complications in pregnancy. In: Sharma JB. (ed) The Obstetric Protocol, 1st edn. Delhi: Jaypee Brothers 1998:78-98.
11. Sharma JB, Arora BS, Kumar S, Goel S, Dhamija A. Helminth and protozoan intestinal infections: an important cause for anaemia in pregnant women in Delhi, India. J Obstet Gynecol Ind 2001; 51(6):58-61.
12. Lops VR, Hunter LP, Dixon LR. Anemia in pregnancy. Am Fam Physician 1995; 51:1189-1197.
13. Preziosi P, Prual A, Galan P, Daouda H, Boureima H, Hereberg S. Effect of iron supplementation on the iron status of pregnant women: consequences for newborns. Am J Clin Nutr 1997; 66:1178-1182.
14. Ταμπακούδης Π, Μανταλενάκης Σ. Η προγεννητική διάγνωση των αιμοσφαιρινοπαθειών. Ελληνική Μαιευτική και Γυναικολογία 1988; 1(3,4):198-214.
15. Ταμπακούδης Π. Προγεννητικός Έλεγχος. Ελληνική Μαιευτική και Γυναικολογία 2001; 13(1-2):59-79.
16. ACOG technical bulletin. Hemoglobinopathies in pregnancy. Int J Gynecol Obstet 1996; 53:184-194.
17. Ταμπακούδης Π, Μανταλενάκης Σ. Μεσογειακή αναιμία και κύηση. Ελληνική Μαιευτική και Γυναικολογία 1996; 8(2):135-153.
18. Tampakoudis P, Tsatalas C, Mamopoulos M, Tantanassis Th, Christakis J, Sinakos Z, et al. Transfusion - dependent homozygous §-Thalassaemia major: successful pregnancy in five cases. Eur J Obstet Gynecol Reprod Biol 1997; 74:127-131.
19. Kramer K, Cohen HJ. Anteatal diagnosis of hematologic disorders. In Hematology. Basic principles and Practice (eds): Hoffman R, Benz EJ, Furie B, Cohen HJ, Silberstein IE, Second Edition, Churchill Livingstone, Edinburgh 1995:2250-2265.
20. Σχίζας Ν, Τέγος Κ, Βουτσαδάκης Α, Αραμπατζής Γ, Αγγελοπούλου Π, Χρυσανθόπουλος Κ, και συν. Συχνότης και κατανομή β-μεσογειακής αναιμίας και παθολογικών αιμοσφαιρινών εις τον Ελληνικόν χώρον. Έρευνα επί 15.550 νεοσυλλέκτων. Ιατρική Επιθεώρησις Ενόπλων Δυνάμεων 1977, 11 (1): 197-209.
21. Ταμπακούδης Π, Τσαταλάς Κ, Πάντος Γ, Σινάκος Ζ, Μανταλενάκης Σ. Η προφυλακτική μετάγγιση ερυθρών αιμοσφαιρίων σε έγκυες με δρεπανοκυτταρική νόσο. Ελλην Μαιευτ Γυναικολ 1989; 2:219-224.
22. Rust OA, Perry KG. Pregnancy complicated by sickle hemoglobinopathy. Clin Obstet Gynecol 1995; 38:472-484.
23. Tampakoudis P, Tantanassis T, Tsatalas C, Christakis J, Venetis Ch, Lazaridis P, et al. Pregnancy and sickle cell disease. XV FIGO World Congress of Gynecology and Obstetrics, August 1997:3-8.
24. Ταμπακούδης Π, Ταντανάσης Τ, ΤσαταλάςΚ, Χριστάκης Ι, Βλαχάκη Ε, Βενέτης Χ, και συν. Δρεπανοκυτταρική αναιμία και εγκυμοσύνη. Αναφορά 46 περιπτώσεων. Εφηβ Γυν Αναπ Εμμην 1999; 11(4):295-302.
25. Ταμπακούδης Π. Δρεπανοκυτταρικά σύνδρομα και εγκυμοσύνη, Ελληνική Μαιευτική και Γυναικολογία, 1997; 9(3):197-212.
26. Milunsky A. Nutritional and other envirommental factors in the etiology of neural tube defects (NTDs). In «Abstracts from VI International Conference on Early Prenatal Diagnosis of Genetic Diseases From Gametes to Embryo», Milan, 18-20 May. Prenatal diagnosis (Supplement) 1992; 12:522.
27. Ταμπακούδης Π, Μανταλενάκης Σ. Προγεννητικός έλεγχος ανοικτών βλαβών του κεντρικού νευρικού συστήματος. Materia Medica Greca 1992; 20(5):413-414.
28. Ταμπακούδης Π, Γκριμπίζης Γ, Τσαλίκης Τ, Τζεβελέκης Φ, Γαρυπίδου Β, Σινάκος Ζ, και συν. Μεγαλοβλαστική αναιμία και εγκυμοσύνη. Αναφορά μιας περιπτώσεως. Ελληνική Μαιευτική και Γυναικολογία 1994; 6(4):395-398.
29. Morrison JC, Floyd RC, Martin RW, Dodson MK, Roberts WE, Morrison JS. Blood transufsions after postpartum hemorrhage due to uterine atony. J Matern Fetal Invest 1991; 1:209-212.
30. Consensus Development Conference Statement. National Institutes of Health. Guidelines for blood product infusion: cryoprecipitate. JAMA 1994; 271:777-781.
31. Naef RW, Morrison JC. Transfusion therapy in pregnancy. Clin Obstet Gynecol 1995; 38(3):547-557.
32. Ekeroma AJ, Ansari A, Stirrat GM. Blood transfusion in Obstertrics and Gynaecology. Br J Obstet Gynaecol 1997; 104:278-284.
33. Camman WR, Datta S. Red cell use during caesarean delivery. Transfusion 1991; 31:12-15.
34. Ταμπακούδης Π, Ταντανάσης Θ, Τσαταλάς Κ, Τσαλίκης Τ, Βλαχάκη Ε, Λαζαρίδης Ε, και συν. O ρόλος της μητρικής ερυθροποιητίνης ως δείκτου της αποτελεσματικότητάς της από του στόματος συμπληρωματικής αγωγής με πρωτεϊνοηλεκτρικό σίδηρο σε μονήρεις εγκυμοσύνες. Εφηβ Γυν Αναπ Εμμην 1997; 9(4):285-289.
35. Achadi EL, Hansell MJ, Sloan NL, Anderson MA. WomenΥs nutritonal status, iron consumption and weight gain during pregnancy in relation to neonatal weight and lenght in West Java, Indonesia, Inter J Gynecol Obstet 1995; 48:103-119.
36. Benjamin I, Barakat PR, Curtin JP, Jones WB, et al. Blood transfusion for radical hysterectomy before and after the discovery of transfusion-related HIV. Obstet Gynecol 1994; 84:974-978.
37. Morrison J, Sumrill D, Chevalier SP, et al. The effect of provider education on blood utilisation practices. Am J Obstet Gynecol 1993; 169:1240-1245.
38. Foglia G, Corticelli A, Podesta M, Valenzano M, Rissone R, Giannini G, et al. Preoperative autologous blood donation and transfusion in gynecology. Minerva Ginecol 2000; 52(9):333-337.
39. Roberts L, Andres MD, Kathleen M, et al. A reappraisal of the need for autologous blood donation in the obstetric patient. Am J Obstet Gynecol 1990; 163:1551-1553.
40. Hill T, Lavin P. Blood ordering in Obstetrics and Gynaecology: Recommendations for the type and screen. Obstet Gynecol 1993; 62:659-664.
41. Contreras M, editor. ABC of transfusion. BMJ 1992.
42. Clark VA, Wardall GJ. McGrady EM. Blood ordering practices in obstetric units in the United Kingdom. Anaesthesia 1993; 48:998-1001.
43. Naef RW III, Washburne JF, Martin RW, Magann EF, Scanlon PH Jr, Morrison JC. Hemorrhage associated with cesarean delivery: When is transfusion needed? J Perinatol 1995; 15:32-35.
44. Nichols MD, Whyte G. Red cell, plasma and albumin transfusion decision triggers. Anesthesia and Intensive Care 1993; 21:156-162.
45. Sirchia G, Giovanetti AM, McClelland DBL, Fracchia GN, editors. Safe and Good Use of Blood in Surgery (SANGUIS). European Commission, 1994.
46. Ταμπακούδης Π, Γκριμπίζης Γ, Τσαλίκης Τ, Λαζαρίδης Ε, Γιαννούλης Χ, Παπαλέτσος Μ, και συν. Καισαρική τομή: Τάσεις κατά τη δεκαετία 1984-1993. Ελληνική μαιευτική και γυναικολογία 1996; 8(1):66-70.
47. Combs CA, Murphy EL, Laros RK. Cost-benefit analysis of autologous blood donation in obstetrics. Obstet Gynecol 1992; 80:621-625.
48. Klapholz H. Blood transfusion in contemporary obstetric practice. Obstet Gynecol 1990; 75:940-943.
49. Naef RW, Washburne JF, Martin RW, Magann EF, et al. Haemorrhage associated with caesarean delivery: When is transfusion needed? Perinatol 1995; 15:32-35.
50. Ross A, Malkoutzis E. Blood transfusion practice in obstetric and gynaecological anaesthesia. Anaesthesia and Intensive Care 1995; 23:645.
51. Mintz PD, Sullivan MF. Preoperative crossmatch ordering and blood use in elective hysterectomy. Obstet Gynecol 1985; 65:389-392.
52. Rosen NR, Bates LH, Herod G. Transfusion therapy: Improved patient care and resource utili sation. Transfusion 1993; 33:341-347.
53. Indications for the use of red blood cells, platelets and fresh frozen plasma. Washington DC.US Report of Health and Human Services 1989.
54. Indications for use of Red Blood Cells, Platelet and Fresh Frozen Plasma. Victoria Australia. Red Cross Blood Bank 1993.
55. Atrah HI, Galea G, Urbaniak SJ. The sustained impact of a group and screen and maximum surgical blood ordering schedule policy on the transfusion practice in gynaecology and obstetrics. Clin Lab Haematol 1995; 17:177-181.
56. Hibbard BM, Anderson MM, O Drife J, et al. Report on Confidential Enquiries into Maternal Deaths in the United Kingdom 1991-1993. HMSO London 1996.
57. Martin C, Dildy GA. Blood component therapy. Contemp Obstet Gynaecol 1994:11-27.
58. Evans LC, Combs CA. Increase maternal morbidity after caesarean section delivery before 28 weeks of gestation. Int J Obstet Gynecol 1993; 40:227-233.
59. Theodossiades G, Makris M. Tranfusion, transmitted infections: epidemiology, risks and prevention. Haema 2001; 4(1):24-38.
60. Ταμπακούδης Π, Μανταλενάκης Σ. AIDS και Εγκυμοσύνη. Mat Med Gr 1991; 19:17-31.
61. Ταμπακούδης Π. AIDS στη Μαιευτική. Ελληνική Μαιευτική και Γυναικολογία 1999; 11(Ι):25-43.
62. UNAIDS/WHO working group of global HIV / AIDS and STD surveillance. Report on the global HIV/AIDS epidemic, Geneva, Switzerland November 2002.
63. Hatzidimitriou K, Kontopoulou I, Mandalaki T, et al. HIV seropositivity in Greek blood donors (1985-1990). Vox Sang 1991; 61:215-216.
64. Schreiber GB, Busch MP, Kleinman SH, Korelitz JJ. The risk of transfusion-transmitted viral infections. N Engl J Med 1996; 334:1685-1690.
65. Ταμπακούδης Π. Αιματολογικές κακοήθειες κατά την εγκυμοσύνη. Ελληνική Μαιευτική και Γυναικολογία 1997; 9(2):108-127.
66. Otigban C, Kelly A, Aitken C, Norman J, Jeffries D, Erskine KJ. Is HTLV-1 status another antenatal screening test that we need? Br J Obstet Gynaecol 1997; 104:258-260.
67. Ταμπακούδης Π. Ιός των θηλωμάτων στη Μαιευτική - Γυναικολογία. Ελληνική Μαιευτική και Γυναικολογία 2002; 14(2):128-146.
68. Gessain A, Barin E, Vernant JC, et al. Antibodies to human T-lymphotropic virus type-I in patients with tropical spastic paraparesis. Lancet 1985; ii:407-410.
69. Murphy EI, Engstrom JW, Miller K, et al. HTLV-II associated myelopathy in 43-year-old woman. Lancet 1993; 341:757-758.
70. Taylor GD. The epidemiology of HTLV-I in Europe. J Acq Imm Def Syndr Hum Retrovirol 1996; 13:8-14.
71. Centers for Disease Control. Protection against viral hepatitis. Recommendations of the Immunization Practices Advisory Committee (ACIP). MMWR 1990; 39(RR-2):1-26.
72. Totos G, Gizaris V, Papaevangelou G. Hepatitis A vaccine: persistence of antibodies 5 years after the first vaccination. Vaccine 1997; 15:1252-1253.
73. Sweet RL. Hepatitis B infection in pregnancy. Obstetrics/Gynecology Report 1990; 2:128-139.
74. Hoffnagle JH. Chronic hepatitis B. N Engl J Med 1990; 323:337-339.
75. Centers for Disease Control. Hepatitis B virus: A comprehensive strategy for eliminating transmission in the United States through universal childhood vaccination: recommendations of the Immunization Practices Advisory Committee (ACIP). MMWR 1991; 40(RR-13):1-25.
76. Kyriakis KP, Foudoulaki LE, Papoulia EI, Sofroniadou KE. Seroprevalence of hepatitis B surface antigen (HbsAg) among first-time and sporadic blood donors in Greece: 1991-1996. Transfusion Med 2000; 10:175-180.
77. Ταμπακούδης Π, Γκριμπίζης Γ, Μανταλενάκης Σ. Συχνότητα της οροθετικής ηπατίτιδας Β στις έγκυες. Ελληνική Ιατρική 1992; 58(4):248-252.
78. Ταμπακούδης Π. Ηπατίτιδα C και εγκυμοσύνη. Ελληνική Μαιευτική και Γυναικολογία 2001; 13(4):237-141.
79. WHO Weekly epidemiological record: Hepatitis C: global prevalence. WHO Weekly Epidemiological Record 1997; 72:341-344.
80. Hoofnagle JH. Type D (delta) hepatitis. JAMA 1989, 261: 1321-1325 Erratum in JAMA 1989; 261:3552.
81. Shattock AG, Irwin FM, Morgan BM, Hillary IB, Kelly MG, Fielding JF, et al. Increased severity and morbidity of acute hepatitis in drug abusers with simultaneously acquired hepatitis B and hepatitis D virus infections. BMJ 1985; 290:1377-1380.
82. Mannucci PM, Gringeri A, Santagostino E, et al. Low risk of transmission of hepatitis E virus by large - pool coagulation factor concentrates. Lancet 1994; 343:597-598.
83. Karayiannis P, Thomas HC. Current status of hepatitis G virus (GBV-C) in transfusion: is it relevant? Vox Sang 1997; 73: 63-69.
84. Rodis YF. Parvovirus infection. Clin Obstet bynecol 1999; 42(I):107-120.
85. Prowse C, Ludlam CA, Yap PL. Human parvovirus B19 and blood products. Vox Sang 1997;72:1-10.
86. Kyriazopoulou B, Simitsopoulou M, Bondis J, Diza E, Athanasiadis A, Frantzidou F, et al. Human parvovirus B19: Immunity of Greek females and prenatal investigation of hydrops fetalis. Eur J Obstet Gynecol Reprod Biol 1997; 74:157-160.
87. Gessain A. Human herpesvirus 8 and associated diseases: KaposiΥs sarcoma, body cavity based lymphoma and multicentric CastlemanΥs disease: clinical and molecular epidemiology. Bull Acad Natl Med 1997; 181:1023-1024.
88. Lennette ET, Blackbourn DJ, Jevy JA. Antibodies to human herpesvirus type 8 in the general population and in KaposiΥs sarcoma patients. Lancet 1996; 348:858-861.
89. Biagini P, Gallian P, Touinsi M, et al. High prevalence of TT virus infection in French blood donors revealed by the use of three PCR systems. Transfusion 2000; 40:590-595.
90. Wang JT, Lee CZ, Kao JH, et al. Incidence and clinical presentation of post transfusion TT virus infection in prospectively followed transfusion recipients: emphasis on its relevance to hepatitis. Transfusion 2000; 40:596-601.
91. Bowden RA. Transfusion-transmitted cytomegalovirus infection. Immunol Invest 1995; 24:117-128.
92. Narducci F, Switala I, Rajabally R, Decocq J, Delahouse G. Syphilis maternelle et congenital. J Gynecol Obstet Biol Reprod 1998; 27:150-160.
93. Abvad A. Cost-effectiveness on antenatal screening for syphilis. Health Care Women Inti 1995; 16:323-328.
94. Cable RG. Evaluation of syphilis testing of blood donors. Transfusion Med Rev 1996; p:296-302.
95. Ταμπακούδης Π, Τζεβελέκης Φ, Ρώσιου Κ, Καλαχάνης Ι, Μπιζίμης Π, Αναγνώστου Ε, και συν. Μητρική και συγγενής σύφιλη. Ελληνική Μαιευτική και Γυναικολογία 1999; 11(2):197-202.
96. Martens P, Hall L. Malaria on the move: human population movement and malaria transmission. Emerging Infectious Disease 2000; 6:103-109.
97. Heltberg O, Skov F, Gerner-Smidt P, et al. Nosocomial epidemic of Serratia marcescens septicemia ascribed to contaminated blood transfusion bags. Transfusion 1993; 33:221-227.
98. Blajchman MA. Bacterial contamination and proliferation during the storage of cellular blood products. Vox Sang 1998; 74:155-159.
99. Morduchowicz G, Pitlik SD, Huminer D, Alkan M, et al. Transfusion reactions due to bacterial contamination of blood and blood products. Rev Infect Dis 1991; 13:307-314.
100. Evatt B, Austin H, Barhart E, et al. Surveillance of Creutzfeldt-Jakob disease among persons with hemophilia. Transfusion 1998; 38:817-820.
101. Budka H. Prions and Transfusion Medicine, Vox Sang 2000; 78:231-238.