Διαγνωστική προσέγγιση
της ενδομητρίωσης
Δ. Τσολακίδης
Γ. Πάντος
Τ. Τσαλίκης
Ι. Μπόντης
A' Μαιευτική-Γυναικολογική
Κλινική
Α.Π.Θ.
Νοσοκομείο «Παπαγεωργίου»
Θεσσαλονίκη
Aλληλογραφία:
Δημήτριος Χ. Τσολακίδης
Ι. Πασσαλίδη 155
Θεσσαλονίκη 55133
Tηλ: 2310-432845
e-mail: dtsolakidis@hol.gr
Κατατέθηκε: 27/4/2004
Εγκρίθηκε: 21/6/2004
Περίληψη
Η ενδομητρίωση αποτελεί συχνή γυναικολογική πάθηση, κυρίως της αναπαραγωγικής
ηλικίας. Η οριστική διάγνωσή της βασίζεται στην ιστολογική ανεύρεση έκτοπου
ενδομητρίου με παρουσία αδένων και στρώματος. Όμως τόσο η κλινική, όσο και η
εργαστηριακή διερεύνηση εξακολουθεί να είναι προβληματική. Αυτό το άρθρο ανασκοπεί
τον βαθμό προόδου στη διαγνωστική προσέγγιση με μη επεμβατικές μεθόδους, όπως
η διακολπική υπερηχογραφία, η Doppler υπερηχογραφία, η μαγνητική τομογραφία
και οι ορολογικοί δείκτες CA-125, κυτοκίνες και αρωματάση Ρ450 για τη βελτίωση
της διάγνωσης της ενδομητρίωσης τόσο σε ασυμπτωματικές, όσο και σε γυναίκες
με χρόνιο πυελικό άλγος και υπογονιμότητα. Τέλος, παρουσιάζονται οι τελευταίες
εξελίξεις της επιστήμης στην ανεύρεση γονιδίων, πρωτεϊνών και αντισωμάτων για
τη διάγνωση αλλά και τη θεραπεία της ενδομητρίωσης.
Όροι ευρετηρίου:
Eνδομητρίωση, υπερηχογραφία, Doppler, μαγνητική τομογραφία, CA-125, κυτοκίνες.
ΕΙΣΑΓΩΓΗ
Η ενδομητρίωση ορίζεται ως η παρουσία έκτοπου ενδομητρικού ιστού από αδένες
και στρώμα εκτός της ενδομητρικής κοιλότητας. Αν και το 75-90% των γυναικών
παρουσιάζουν παλινδρόμηση εμμηνορυσιακού υλικού στην περιτοναϊκή κοιλότητα,
ωστόσο μόνο το 2-10% των γυναικών της αναπαραγωγικής ηλικίας θα εμφανίσουν ενδομητρίωση.(1)
Κατά τον Verkauf η ενδομητρίωση ανευρίσκεται στο 5,2% των γόνιμων γυναικών και
στο 38,5% των υπογόνιμων.(2) Όμως η ακριβής συχνότητα της νόσου είναι δύσκολο
να καθορισθεί, διότι, αν και η λαπαροσκόπηση είναι η μέθοδος εκλογής για τη
διάγνωση και τη σταδιοποίηση της ενδομητρίωσης, η ιστολογική εξέταση από τις
ύποπτες βλάβες είναι αρνητική σε ποσοστό 24% ακόμη και με τη λαπαροσκόπηση.
Αντίθετα, είναι δυνατόν κατά τη διαγνωστική λαπαροσκόπηση της περιτοναϊκής κοιλότητας
κάτω από ένα μακροσκοπικά «φυσιολογικό» περιτόναιο να υπάρχει μικροσκοπική ιστολογική
βλάβη συμβατή με ενδομητρίωση.(3)
Το κλινικό φάσμα της ενδομητρίωσης είναι ευρύ και κανένα από τα συμπτώματα,
όπως η δυσμηνόρροια, η δυσπαρεύνια, το πυελικό άλγος και η υπογονιμότητα δεν
είναι παθογνωμονικό. Επίσης, το στάδιο της νόσου πολλές φορές δεν συσχετίζεται
με την ένταση και τη σοβαρότητα των συμπτωμάτων.
Η διακολπική υπερηχογραφία σε συνδυασμό με την Doppler υπερηχογραφία, καθώς
και η μαγνητική τομογραφία είναι χρήσιμες στη διάγνωση των ενδομητριωσικών κύστεων
των ωοθηκών (ενδομητριώματα). Πρόσφατα, η διορθική υπερηχογραφία και η μαγνητική
τομογραφία (MRI) βρέθηκε ότι συμβάλλουν σημαντικά στη διάγνωση τής εν τω βάθει
ενδομητρίωσης και ειδικότερα του ορθοκολπικού διαφράγματος.
Μέχρι σήμερα έχουν διεξαχθεί πολλές μελέτες για την ανακάλυψη ορολογικών δεικτών
που θα μπορούσαν να χρησιμοποιηθούν ως μέθοδος ανίχνευσης (screening) της ενδομητρίωσης
ακόμη και σε ασυμπτωματικές γυναίκες. Παρόλα αυτά, κανένας ορολογικός δείκτης,
συμπεριλαμβανομένου και του CA-125, δεν έχει την ευαισθησία και την ειδικότητα
για να χρησιμοποιηθεί ευρέως ως μέθοδος ανίχνευσης της συχνής αυτής πάθησης
σε γυναίκες αναπαραγωγικής ηλικίας. Τελευταία, οι έρευνες στρέφονται στη μοριακή
γενετική για την ανακάλυψη γονιδίων και συγκεκριμένων πρωτεϊνών για τη διάγνωση
και τη θεραπεία, δεδομένου ότι ολοένα και περισσότερες μελέτες συγκλίνουν στο
γεγονός πως η ενδομητρίωση αποτελεί πολυγονιδιακή και πολυπαραγοντική νόσο.
Σκοπός αυτού του άρθρου είναι να παρουσιάσει τις πρόσφατες ανακαλύψεις στις
απεικονιστικές τεχνικές και στους ορολογικούς δείκτες για τη διαγνωστική προσέγγιση
της ενδομητρίωσης.
Ι. ΑΠΕΙΚΟΝΙΣΤΙΚΕΣ ΤΕΧΝΙΚΕΣ
1. Υπερηχογραφία
Παρά το γεγονός ότι η υπερηχογραφία δεν μπορεί να ανιχνεύσει τις ενδομητριωσικές
εστίες στο περιτόναιο, η διακολπική υπερηχογραφία με τη χρήση κεφαλών 6.5ΜΗz
αποτελεί την πιο χρήσιμη και συχνή απεικονιστική μέθοδο για την ανίχνευση και
την παρακολούθηση των ενδομητριωσικών κύστεων των ωοθηκών με μέγεθος μεγαλύτερο
των 10mm. Σύμφωνα με μελέτες η ευαισθησία της μεθόδου στη διάγνωση των ενδομητριωμάτων
κυμαίνεται στο 76-90% και η ειδικότητα στο 89-100% (πίνακας 1).(4) Tο 95% των
ενδομητριωσικών κύστεων στη διακολπική υπερηχογραφία απεικονίζονται ως κύστεις
στρογγύλου σχήματος με υπερηχοϊκό ομαλό τοίχωμα στο 81% και με ομοιογενές πυκνό
υποηχοϊκό περιεχόμενο στο 63% των περιπτώσεων. Το περιεχόμενο αυτό αντιστοιχεί
στο σοκολατοειδές υγρό από την αποδόμηση των προϊόντων του αίματος που προέρχεται
από τις κυκλικές αλλαγές κατά τον καταμήνιο κύκλο. Σπανίως, οι ενδομητριωσικές
κύστεις απεικονίζονται υπερηχογραφικά με τη μορφή διαφραγμάτων με πολύ παχύ
τοίχωμα, ή οζιδίων τα οποία προσεκβάλλουν στο εσωτερικό τους και δημιουργούν
διαφοροδιαγνωστικά προβλήματα.(5)
Η διακολπική Doppler υπερηχογραφία κατά τον Guerriero συμβάλλει στη διαφοροδιάγνωση
των ενδομητριωσικών κύστεων από άλλες εξαρτηματικές βλάβες των ωοθηκών με αύξηση
της ευαισθησίας από 81% σε 90% και της ειδικότητας από 91% σε 97%. Συγκεκριμένα,
διαπιστώνεται λεπτή αιματική ροή περικυστικά και κυρίως στην πύλη της ωοθήκης
στο 69% των επιβεβαιωμένων ενδομητριωμάτων με μέτριες έως αυξημένες αγγειακές
αντιστάσεις κατά την παραγωγική φάση και συγκεκριμένα με μέση τιμή δείκτη παλμικότητας
(pulsatility index) 0.88 (0.36-2.28) και μέση τιμή δείκτη αντίστασης (resistance
index) 0.57 (0.33-0.96). Έτσι, η διακολπική Doppler υπερηχογραφία αυξάνει τη
διαγνωστική ακρίβεια της απλής διακολπικής υπερηχογραφίας, ιδιαίτερα στη διαφοροδιάγνωση
των ενδομητριωμάτων από άλλες καλοήθεις μη ενδομητριωσικές κύστεις των ωοθηκών,
όπως των κύστεων του ωχρού σωματίου που χαρακτηρίζονται από πλούσια αγγείωση
τόσο στο τοίχωμά τους όσο και στο εσωτερικό τους.
Επιπλέον, στις άτυπες υπερηχογραφικά ενδομητριωσικές κύστεις των ωοθηκών στρογγύλου
σχήματος με ομοιογενές υποηχοϊκό περιεχόμενο και με ένα υπερηχοϊκό μόρφωμα στο
εσωτερικό τους, η απουσία αιματικής ροής κατά την Doppler υπερηχογραφία στο
εσωτερικό της προσεκβολής τις διαχωρίζει από τις μη ενδομητριωσικές κύστεις.(6)
Αντίθετα, ο Αlcazar δεν διαπίστωσε πως η Doppler υπερηχογραφία υπερέχει της
απλής διακολπικής υπερηχογραφίας.(7) Διαπίστωσε, όμως, πως η εκτίμηση της αγγείωσης
των ενδομητριωμάτων με την Doppler υπερηχογραφία στους ασθενείς με πυελικό άλγος
είναι μεγαλύτερη (88.6%) σε σχέση με τους ασυμπτωματικούς ασθενείς (66.1%),
υποδηλώνοντας, έτσι, ότι στους συμπτωματικούς ασθενείς υπάρχει αυξημένη αγγειογένεση,
γεγονός που έχει αποδειχθεί και με άλλες μελέτες εκτίμησης της αγγειακής δραστηριότητας
βασιζόμενες σε ορολογικούς και σε αγγειογενετικούς δείκτες του περιτοναΐκού
υγρού.(8)
Η χρήση των 3D power Doppler στο μέλλον μπορεί να επιτρέψει την καλύτερη απεικόνιση
του τοιχώματος, του εσωτερικού περιεχομένου και της αγγείωσης των ενδομητριωσικών
κύστεων και να συμβάλει με μεγαλύτερη σαφήνεια και ακρίβεια στη διαφοροδιάγνωσή
τους από τις άλλες καλοήθεις και κακοήθεις κύστεις των ωοθηκών. Στην 3D power
Doppler υπερηχογραφία τα αγγεία των σοκολατοειδών κύστεων είναι συνήθως ευθέα,
ομαλά διακλαδιζόμενα που ξεκινούν από ένα αγγείο της πύλης και διατρέχουν κατά
μήκος της επιφάνειας του τοιχώματός τους (εικόνα 1).(9)
Μέχρι σήμερα έχουν γίνει λίγες υπερηχογραφικές μελέτες για την ανίχνευση και
τη διάγνωση της εν τω βάθει ενδομητρίωσης, η οποία στη διακολπική υπερηχογραφία
απεικονίζεται ως οζίδια συμπαγή υποηχοϊκά με μέγεθος 0.5 έως 4 εκατοστά. Τα
οζίδια αυτά είναι περισσότερο επώδυνα, όταν η υπερηχογραφική εξέταση πραγματοποιηθεί
κατά την εμμηνορρυσία. Aνάλογα με τη συχνότητα της κεφαλής των υπερήχων, η ευαισθησία
και η ειδικότητα της εξέτασης στην ανίχνευση της ενδομητρίωσης στους ιερομητρικούς
συνδέσμους είναι 75% και 83% αντίστοιχα. Στην περίπτωση της ενδομητρίωσης του
τοιχώματος του ορθού η ευαισθησία και η ειδικότητα της εξέτασης ανέρχονται στο
95% και 100% αντίστοιχα.
Το κύριο πλεονέκτημα της διακολπικής υπερηχογραφίας είναι ότι εξετάζεται ολόκληρη
η ελάσσονα πύελος συμπεριλαμβανομένης της ουροδόχου κύστεως, της μήτρας, των
ιερομητρικών συνδέσμων, του δουγλασείου, των ωοθηκών, του ορθοκολπικού διαφράγματος
και του ορθού σε μία μόνο εξέταση. Ωστόσο, η διακολπική υπερηχογραφία, ενώ μπορεί
να διαπιστώσει την απουσία διακριτών ορίων μεταξύ του οπισθίου τοιχώματος του
κόλπου και του προσθίου τοιχώματος του ορθού, στην ενδομητρίωση του ορθοκολπικού
διαφράγματος δεν μπορεί να καθορίσει την ακριβή απόσταση των ορθικών βλαβών
από τον πρωκτικό δακτύλιο και να εκτιμήσει την ύπαρξη και το βάθος διήθησης
του τοιχώματος του ορθού.(10)
Με τη διορθική υπερηχογραφία μπορούμε να εκτιμήσουμε το πάχος των ιερομητρικών
συνδέσμων και την παρουσία ανωμαλίας στο σχήμα τους με ευαισθησία 75%-80% και
ειδικότητα 67%-97%, καθώς επίσης την ύπαρξη διήθησης του τοιχώματος (βλεννογόνου,
υποβλεννογόνιου και μυικού χιτώνα) του ορθού και των γύρω ιστών με ευαισθησία
75%-97% και ειδικότητα 67%-96%. Συμπεραίνουμε, λοιπόν, πως η διακολπική και
η διορθική υπερηχογραφία έχουν την ίδια ακρίβεια στη διάγνωση της εν τω βάθει
ενδομητρίωσης στον οπίσθιο δουγλάσειο χώρο.
Γι' αυτό προτείνεται η χρήση της ως εξέταση εκλογής για την εκτίμηση της ενδομητρίωσης,
καθώς επιτρέπει την εκτεταμένη εξέταση ολόκληρης της ελάσσονος πυέλου, χωρίς
να γίνεται ιδιαίτερα ενοχλητική για την ασθενή. Eνώ η διορθική υπερηχογραφία
έχει ένδειξη μόνο όταν υποπτευόμαστε ενδομητρίωση του τοιχώματος του ορθού,
γιατί είναι πιο αξιόπιστη μέθοδος ως προς την εκτίμηση του βάθους και της έκτασης
της διήθησης, πληροφορίες αναγκαίες για τη σωστή χειρουργική αντιμετώπιση αυτής
της μορφής της εν τω βάθει ενδομητρίωσης.(11,12)
Στην ενδομητρίωση της ουροδόχου κύστεως η διακολπική υπερηχογραφία μπορεί να
αποκαλύψει ένα συμπαγές οζίδιο μέσα στο οπίσθιο τοίχωμα, έχοντας την ουροδόχο
κύστη ελαφρώς γεμάτη. Η έγχρωμη Doppler υπερηχογραφία ανιχνεύει μικρή έως μέτρια
αγγείωση στο οζίδιο, ενώ η ελαφρά πίεση με την κολπική κεφαλή συχνά εκλύει τοπικά
πόνο.(13)
Τέλος, σε επιλεγμένες περιπτώσεις, όπως η ενδομητρίωση του κοιλιακού τοιχώματος,
η χρήση της διακοιλιακής υπερηχογραφίας μπορεί να αποδειχθεί χρήσιμη.(14)

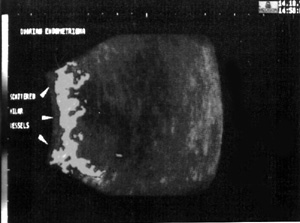
Εικόνα 1. Χαρακτηριστική
αγγείωση ενδομητριώματος στην 3D power υπερηχογραφία.
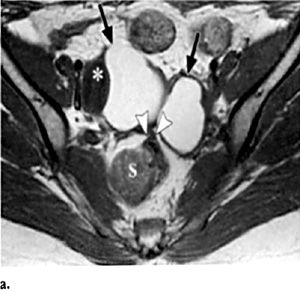
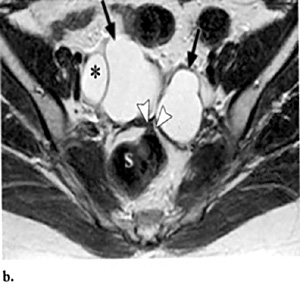
Εικόνα
2. Ωοθηκικά ενδομητριώματα. Εγκάρσιες Τ1(Α) και Τ2(Β) εικόνες μαγνητικής τομογραφίας
αμφοτερόπλευρων ωοθηκικών ενδομητριωμάτων. Υψηλής έντασης σήμα και στις δύο
ακολουθίες (βέλη), χαρακτηριστικό των ενδομητριωμάτων. Χαμηλής έντασης σήμα
μεταξύ των ωοθηκών (κεφαλή βέλους) και του σιγμοειδούς (S), που αντιστοιχεί
σε ινώδεις συμφύσεις. *=ωοθυλάκιο
2.
Μαγνητική τομογραφία
H μαγνητική τομογραφία (MRI) έχει αποδειχθεί ως ένα χρήσιμο μη επεμβατικό διαγνωστικό
μέσο της ενδομητρίωσης. H μαγνητική τομογραφία υπερέχει της υπερηχογραφίας στην
ενδομητρίωση του περιτοναίου, η οποία εμφανίζεται ως πολλαπλά μικρά οζίδια,
γιατί μπορεί να ανιχνεύσει την ύπαρξη ενδομητριωσικών εμφυτεύσεων στις Τ1 ακολουθίες
με ευαισθησία 11-27% και με σήμα το οποίο ποικίλει σε ένταση ανάλογα με την
ενεργό δραστηριότητα και τη χρονική διάρκεια της βλάβης. Στις Τ2 ακολουθίες
οι εμφυτεύσεις εμφανίζονται ως μάζες χαμηλού σήματος λόγω της αντιδραστικής
ίνωσης που περιβάλλει τις μικρές συλλογές ενδομητριωσικού υλικού, αν και κάποιες
φορές στο εσωτερικό των εμφυτεύσεων μπορεί να υπάρχει υψηλής έντασης σήμα λόγω
της κυκλικής αιμορραγίας (εικόνα 2). Όταν όμως οι λήψεις της μαγνητικής τομογραφίας
λαμβάνονται με καταστολή του λίπους, βελτιώνεται η ανίχνευση των ενδομητριωσικών
εμφυτεύσεων στο περιτόναιο, αυξάνοντας την ευαισθησία της μεθόδου στο 47-61%
και την ειδικότητα στο 87-97%.
Επιπλέον, στη μαγνητική τομογραφία οι συμφύσεις εμφανίζονται ως χαμηλής έντασης
σήματος νηματοειδείς σχηματισμοί, οι οποίοι καθιστούν ασαφείς τις διαχωριστικές
επιφάνειες δύο παρακείμενων οργάνων και μπορούν ενίοτε να προσλαμβάνουν σκιαστικό,
χωρίς ωστόσο να αυξάνουν την ευαισθησία ή την ειδικότητα της μαγνητικής τομογραφίας.
Σύμφωνα με μελέτη των Katayama και συν. εκτιμήθηκε η αξία της μαγνητικής τομογραφίας
στην εκτίμηση των πυελικών συμφύσεων χρησιμοποιώντας μια ειδική τεχνική και
διαπιστώθηκε πως η ευαισθησία και η ειδικότητα της μεθόδου είναι 72.5% και 87.4%
αντίστοιχα. Η οπίσθια κλίση και καθήλωση της μήτρας στον δουγλάσειο, η προσκόλληση
των ωοθηκών μεταξύ τους και στην οπίσθια επιφάνεια της μήτρας, η γωνίωση των
εντερικών ελίκων, η ανύψωση των οπίσθιων κολπικών θόλων, η εγκυστωμένη συλλογή
υγρού και η παρουσία υδροσαλπίγγων αποτελούν έμμεσα ευρήματα, ενδεικτικά συμφύσεων
(εικόνα 3).(15,16)
Η μαγνητική τομογραφία έχει αποδειχθεί χρήσιμη στη διάγνωση των ενδομητριωμάτων,
με ευαισθησία και ειδικότητα συγκρίσιμη, και σύμφωνα με κάποιους ερευνητές,
μεγαλύτερη της διακολπικής υπερηχογραφίας, αλλά σαφώς και με μεγαλύτερο κόστος
ως εξέταση. Συγκεκριμένα ο Takahashi διαπίστωσε πως τόσο η κλασική, όσο και
η μαγνητική τομογραφία με καταστολή του λίπους ανιχνεύει όλα σχεδόν τα ενδομητριώματα
με διάμετρο μεγαλύτερη των 10 χιλιοστών.(17) Ακόμη η νόσος μπορεί να βρίσκεται
σε αρχικό στάδιο, όταν η μαγνητική τομογραφία ανιχνεύει βλάβες μικρότερες των
6 χιλιοστών, ενώ βλάβες μεγαλύτερες των 15 χιλιοστών συσχετίζονται με προχωρημένο
στάδιο.(18) Στην κλασική μαγνητική τομογραφία τα ενδομητριώματα εμφανίζονται
ως πολλαπλές, ομοιογενείς, υψηλού σήματος μάζες στις Τ1 ακολουθίες και με χαμηλής
έντασης σήμα στις Τ2 ακολουθίες ως «σκιά» λόγω της αποδόμησης των προϊόντων
του αίματος και της δημιουργίας αιμοσιδηρίνης. Όμως σε περίπτωση πρόσφατου ενεργού
ενδομητριώματος η παρουσία αίματος και στις δύο, Τ1 και Τ2, ακολουθίες θα εκδηλώνεται
ως υψηλής έντασης σήμα, γεγονός που καθιστά δύσκολη τη διαφοροδιάγνωση από τις
αιμορραγικές κύστεις των ωοθηκών. Επίσης, το παχύ ινώδες τοίχωμα της ενδομητριωσικής
κύστης εμφανίζεται ως χαμηλής έντασης σήμα στις Τ2 ακολουθίες, με πρώιμη πρόσληψη
του σκιαστικού εξαιτίας της ύπαρξης αγγείωσης και μακροφάγων με αιμοσιδηρίνη.
Η εν τω βάθει ενδομητρίωση συνήθως απαντάται στη μαγνητική τομογραφία ως ανώμαλου
σχήματος οζίδια διαμέτρου έως 25 χιλιοστά με σήμα ίδιας έντασης με το μυομήτριο
και διάσπαρτες μικρές εστίες υψηλής έντασης στις Τ1 ακολουθίες, ορατές ακόμη
και με καταστολή του λίπους. Στις Τ2 ακολουθίες το σήμα των οζιδίων είναι ίδιας
ή μικρότερης έντασης σε σχέση με το σήμα του μυομητρίου, με διάσπαρτες υψηλής
έντασης εστίες στο εσωτερικό τους. Συνήθεις θέσεις εντόπισης των οζιδίων αποτελεί
το ορθοκολπικό διάφραγμα, με σπάνια επέκταση στα παραμήτρια και τους ουρητήρες,
στους ιερομητρικούς συνδέσμους, στην κυστεομητρική πτυχή, στο τοίχωμα του ορθοσιγμοειδούς
με χαρακτηριστική εστιακή υπερτροφία του έξω μυικού χιτώνα και εξέλκωση του
βλεννογόνου, χωρίς όμως ενδοαυλική επέκταση, σημείο διαφοροδιαγνωστικό από το
καρκίνωμα του εντέρου (πίνακας 2).(19)
Τελευταία, η διαγνωστική ακρίβεια της μαγνητικής τομογραφίας έχει βελτιωθεί
περισσότερο με τη χρήση πηνίων και την αρνητική λήψη σήματος προκειμένου να
αποφευχθεί η χρήση των σκιαστικών του εντέρου.(20)
Στην ενδομητρίωση της ουροδόχου κύστεως η μαγνητική τομογραφία υπερτερεί της
υπερηχογραφίας και αποτελεί τη διαγνωστική μέθοδο εκλογής, γιατί μπορεί να εντοπίσει
όλες τις ενδομητριωσικές βλάβες με διαγνωστική ακρίβεια 100% και να εκτιμήσει
το βάθος διήθησης του οπισθίου τοιχώματός της, πληροφορία πολύ σημαντική για
τη θεραπευτική στρατηγική που θα ακολουθηθεί.(13)
Επιπλέον, η μαγνητική τομογραφία κάποιες φορές συμπληρώνει τη διαγνωστική λαπαροσκόπηση,
γιατί μπορεί να εντοπίσει εξωπεριτοναϊκές ενδομητριωσικές βλάβες ή εστίες κρυμμένες
πίσω από στερρές και εκτεταμένες συμφύσεις, οι οποίες αποφράσσουν μερικώς ή
πλήρως τον οπίσθιο δουγλάσειο. Τέλος, αποτελεί μια χρήσιμη μη επεμβατική μέθοδο
παρακολούθησης των αποτελεσμάτων της φαρμακευτικής θεραπείας. Βρέθηκε πως η
ύπαρξη σκιάς χαμηλής έντασης στις Τ2 ακολουθίες, πριν την έναρξη ή κατά τη διάρκεια
της φαρμακευτικής θεραπείας των ενδομητριωμάτων, αποτελεί αρνητικό προγνωστικό
παράγοντα. Αυτό οφείλεται στο γεγονός ότι το επιθήλιο της ενδομητριωσικής κύστης
λεπτύνεται από την πίεση των προϊόντων του αίματος που συλλέγεται στο εσωτερικό
της και το πυκνό αυτό υλικό δεν μπορεί να απορροφηθεί (εικόνα 4).(15)
A.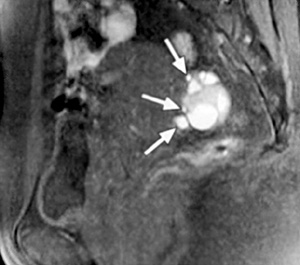 B.
B.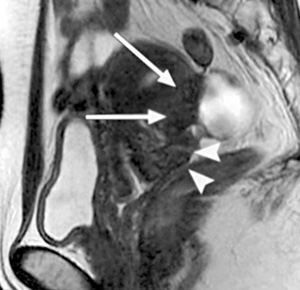
Εικόνα 3. Πυελική ενδομητρίωση
με σοβαρές συμφύσεις. Οβελιαία τομή με καταστολή του λίπους στην Τ1 ακολουθία
(Α) και κλασική Τ2 οβελιαία τομή (Β), όπου απεικονίζονται πολλαπλές ενδομητριωσικές
κύστεις στον δουγλάσειο. Μικρά ενδομητριώματα με υψηλής έντασης σήμα αναγνωρίζονται
στην Τ1 ακολουθία με καταστολή του λίπους (βέλη στη τομή Α). Οπίσθια κλίση της
μήτρας με ανύψωση του οπισθίου κολπικού θόλου (κεφαλή βέλους στη τομή Β), ενδεικτικά
παρουσίας σοβαρών συμφύσεων στον δουγλάσειο. Επιπλέον διαπιστώνεται αδενομύωση
στον ορογόνο της οπισθίας επιφάνειας του μυομητρίου (βέλη στην τομή Β).
Α. 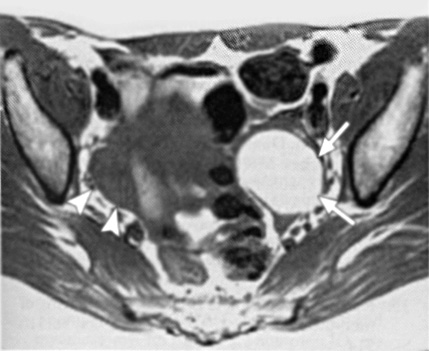 Β.
Β. 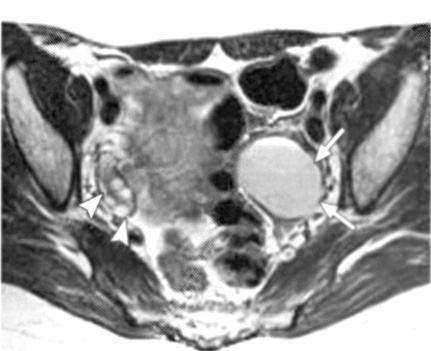
Γ. 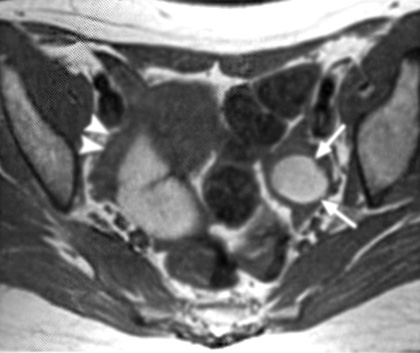 Δ.
Δ.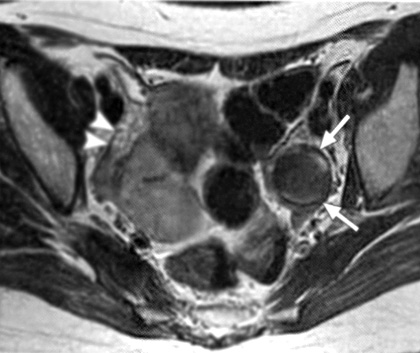
Εικόνα 4. Ωοθηκικά
ενδομητριώματα πριν και μετά τη θεραπεία με GnRH-a. Κεφαλή βέλους= δεξιά ωοθήκη
(Α,Β). Εγκάρσιες Τ1 (Α) και T2(Β) τομές πριν την έναρξη της θεραπείας, όπου
απεικονίζεται μια κύστη υψηλής έντασης (βέλη) που αντιπροσωπεύει ένα ενδομητρίωμα
αριστερής ωοθήκης (Γ,Δ). Εγκάρσιες Τ1 και Τ2 τομές μετά τη θεραπεία με GnRH-a.
Η κύστη είναι μικρότερη σε μέγεθος, αλλά έχει χαμηλής έντασης σήμα στις Τ2 τομές.
Συνεπώς η ορμονική θεραπεία πρέπει να διακοπεί, καθώς η σκιά στο εσωτερικό της
κύστης αποτελεί αρνητικό προγνωστικό δείκτη.
ΙΙ. ΟΡΟΛΟΓΙΚΟΙ ΔΕΙΚΤΕΣ
Τα τελευταία χρόνια διεξάγονται αρκετές μελέτες για την ανακάλυψη ορολογικών
δεικτών χρήσιμων τόσο στη διάγνωση της ενδομητρίωσης, όσο και στην παρακολούθηση
της ανταπόκρισης στη φαρμακευτική ή τη χειρουργική θεραπεία, καθώς επίσης και
στην έγκαιρη ανίχνευση της υποτροπής. Ο ιδανικός δείκτης για την ανίχνευση της
ενδομητρίωσης είναι εκείνος που θα χαρακτηρίζεται από υψηλή ευαισθησία, ειδικότητα,
προγνωστική αξία και καλή συσχέτιση των επιπέδων στον ορό με το στάδιο της νόσου.
Συνεπώς, η έγκαιρη διάγνωση της ενδομητρίωσης με τη χρήση των ορολογικών δεικτών
θα συμβάλλει στην αποφυγή άσκοπων εξετάσεων ή θεραπειών στις ασθενείς με υπογονιμότητα
ή πυελικό άλγος. Μέχρι σήμερα ένας τέτοιος ορολογικός δείκτης δεν έχει ανακαλυφθεί.
1. CA-125
To CA-125 αποτελεί μια υψηλού μοριακού βάρους γλυκοπρωτεΐνη στην επιφάνεια της
μεμβράνης των κυττάρων, η οποία προέρχεται από το σπλαγχνικό επιθήλιο και τους
πόρους του Muller, συμπεριλαμβάνοντας τον ενδοτράχηλο, το ενδομήτριο, τις σάλπιγγες,
το περιτόναιο, το περικάρδιο και τον υπεζωκότα.
Έχει βρεθεί πως η τιμή του CA-125 μεταβάλλεται κατά τη διάρκεια του καταμήνιου
κύκλου τόσο στις υγιείς όσο και στις γυναίκες με ενδομητρίωση, με τη χαμηλότερη
τιμή στη μέση παραγωγική και ωορρηκτική φάση, και την υψηλότερη τιμή κατά τη
διάρκεια της εμμηνορυσίας.(21) Σύμφωνα με μια προοπτική πολυκεντρική μελέτη,
η τιμή του CA-125 είναι πιο αξιόπιστη και ακριβής, όταν προσδιορίζεται στην
ωορρηκτική φάση του κύκλου.(22) Ο OΥShaughnessy προτείνει τη μέτρηση δύο τιμών
CA-125, μία στην εμμηνορρυσία και μία στην ωορρηκτική φάση, και εάν ο λόγος
τους είναι μεγαλύτερος ή ίσος του 1.5, τότε η ευαισθησία της εξέτασης στη διάγνωση
της ενδομητρίωσης αυξάνει στο 66%. Στα φυσιολογικά άτομα η τιμή του CA-125 κυμαίνεται
στα 8 έως 22U/ml, στην ελάχιστη και ήπια ενδομητρίωση η τιμή του CA-125 κυμαίνεται
στο 14 έως 31U/ml , ενώ στη μέτρια και σοβαρή ενδομητρίωση στο 13-95U/ml.(3)
Διαπιστώνουμε πως υπάρχει αλληλοεπικάλυψη των τιμών μεταξύ των φυσιολογικών
γυναικών και των γυναικών με ενδομητρίωση, και κυρίως αυτών με την ελάχιστη
και ήπια ενδομητρίωση.
Επίσης, η τιμή του CA-125 αυξάνεται όχι μόνο στην ενδομητρίωση, αλλά και σε
άλλες καλοήθεις και κακοήθεις γυναικολογικές και μη καταστάσεις, όπως στους
επιθηλιακούς καρκίνους κυρίως της ωοθήκης, στη σαλπιγγίτιδα, στην παγκρεατίτιδα,
στην περιτονίτιδα, στην εγκυμοσύνη και στο σύνδρομο υπερδιέγερσης των ωοθηκών.
Συνεπώς η μέτρηση του CA-125 στον ορό δεν είναι παθογνωμονική εξέταση για τη
διάγνωση της ενδομητρίωσης. Προτείνεται ως όριο η τιμή των 35U/ml στον ορό για
το CA-125, κάτω από την οποία η πιθανότητα να υπάρχει ενδομητρίωση είναι πολύ
μικρή. Σύμφωνα με μια μετα-ανάλυση 23 μελετών (1986-1997) που σύγκριναν τα προεγχειρητικά
επίπεδα του CA-125 στις περιπτώσεις ενδομητρίωσης, οι οποίες επιβεβαιώθηκαν
με τη λαπαροσκόπηση, διαπιστώθηκε πως η χρήση του CA-125 είναι εξέταση με πτωχή
διαγνωστική αξία. Για παράδειγμα, για ειδικότητα 90% η ευαισθησία της εξέτασης
είναι μόλις 28%, ενώ η βελτίωση της ευαισθησίας στο 50% συνοδεύεται με πτώση
της ειδικότητας στο 72%. Σύμφωνα με αυτήν τη μελέτη η μέτρηση του CA-125 στη
διάγνωση της ενδομητρίωσης σταδίου ΙΙΙ/ΙV είναι περισσότερο αξιόπιστη, διότι
για ειδικότητα 89% η ευαισθησία είναι 47%. Ακόμη η ευαισθησία στο στάδιο ΙΙΙ/ΙV
μπορεί να φθάσει στο 60%, με μια μικρή πτώση της ειδικότητας στο 81%.(23) Συνεπώς
η μέτρηση του CA-125 είναι μια περισσότερο αξιόπιστη μη επεμβατική μέθοδος ανίχνευσης
κυρίως της μέτριας και σοβαρής ενδομητρίωσης, στην οποία συνήθως είναι πιο αυξημένο,
διότι ο μεγαλύτερος αριθμός βλαβών περιέχουν αναλογικά μεγαλύτερη ποσότητα του
αντιγόνου και υπάρχει πιο αυξημένη απόπτωσή του. ΓιΥ αυτό η μέτρησή του ως ρουτίνα,
κυρίως στις υπογόνιμες γυναίκες, δικαιολογείται, αφού αυτές υποβάλλονται πιο
έγκαιρα σε λαπαροσκόπηση και αποφεύγουν άλλες άσκοπες εξετάσεις και θεραπείες.
Ο συνδυασμός των θετικών κλινικών ευρημάτων, με την ανίχνευση οζιδίων κατά την
εμμηρορρυσία, με τα επίπεδα του CA-125 αυξάνει την ευαισθησία της εξέτασης στο
87%.(24) Όμως ο συνδυασμός των επιπέδων του CA-125 με τα υπερηχογραφικά ευρήματα
δεν αποβαίνει σε βελτίωση της ευαισθησίας της διακολπικής υπερηχογραφίας. ΠαρΥ
όλα αυτά, η εκτίμηση του CA-125 συμβάλλει στη διαφοροδιάγνωση των ενδομητριωμάτων
από τις κύστεις ωχρού σωματίου που έχουν παρόμοια υπερηχογραφικά ευρήματα.
Τέλος, σε αρκετές μελέτες προτείνεται ο προσδιορισμός διαδοχικών τιμών του CA-125
για την ανταπόκριση στη θεραπεία, φαρμακευτική ή χειρουργική, καθώς και για
την έγκαιρη ανίχνευση της υποτροπής μετά τη θεραπεία.(3)

2. Κυτοκίνες
Οι κυτοκίνες αποτελούν μια μεγάλη οικογένεια χαμηλού μοριακού βάρους πρωτεϊνών,
οι οποίες σχετίζονται με τη ρύθμιση της κυτταρικής δραστηριότητας. Έχουν αυτοκρινή
αλλά και παρακρινή δράση μέσα στα πλαίσια του ανοσολογικού συστήματος του ανθρώπινου
οργανισμού και μαζί με τους αυξητικούς παράγοντες παίζουν σημαντικό ρόλο στη
ρύθμιση της χημειοταξίας, της μίτωσης, της αγγειογένεσης και της διαφοροποίησης.
Σύμφωνα με έρευνες που έχουν διεξαχθεί τα τελευταία χρόνια όσον αφορά στην ανακάλυψη
της παθογένειας της ενδομητρίωσης, βρέθηκε πως πιθανόν οι μεταβολές του ανοσοποιητικού
συστήματος να είναι υπεύθυνες για το ότι κάποιες γυναίκες εμφανίζουν ενδομητρίωση
ενώ άλλες όχι. Συγκεκριμένα το ανοσοποιητικό σύστημα των γυναικών με ενδομητρίωση
πρέπει να επιτρέπει την επιβίωση των ενδομητρικών κυττάρων στην περιτοναϊκή
κοιλότητα. Οι κυτοκίνες και οι αυξητικοί παράγοντες του περιτοναϊκού υγρού που
παράγονται από τα ενεργοποιημένα μακροφάγα και τα μεσοθηλιακά κύτταρα φαίνεται
να προωθούν την εμφύτευση και την ανάπτυξη του έκτοπου ενδομητρικού ιστού, προάγοντας
τον πολλαπλασιασμό και τη διαφοροποίησή του.(25)
Σύμφωνα με μια πρόσφατη μελέτη αλλά και με δικά μας αποτελέσματα(26) μετρήθηκαν
οι συγκεντρώσεις στον ορό και στο περιτοναϊκό υγρό της ΙL-1b, IL-6,IL-8, IL-12,
IL-13 και του TNF-a σε 130 γυναίκες, σε μια προσπάθεια ανακάλυψης ενός μη επεμβατικού
διαγνωστικού μέσου της ενδομητρίωσης. Βρέθηκε, λοιπόν, πως τα επίπεδα της IL-6
στον ορό και του TNF-a στο περιτοναϊκό υγρό με διακολπικά κατευθυνόμενη υπερηχογραφική
παρακέντηση του δουγλασείου μπορούν να χρησιμοποιηθούν, προκειμένου να διακρίνουμε
ποιες γυναίκες πάσχουν από ενδομητρίωση και ποιες όχι, με υψηλή ευαισθησία και
ειδικότητα. Το γεγονός πως οι μετρήσεις αυτών των δύο κυτοκινών δεν επηρεάζονται
σημαντικά κατά τις φάσεις του καταμήνιου κύκλου τις καθιστά αρκετά αξιόπιστες,
προκειμένου να εφαρμοστούν στην κλινική πράξη ως διαγνωστικά μέσα της ενδομητρίωσης.
Όμως τα επίπεδά τους δεν κατάφεραν να συσχετιστούν με το στάδιο βαρύτητας της
νόσου και γιΥ αυτό θα πρέπει να εκλαμβάνονται ως ποιοτικά και όχι ως ποσοτικά
διαγνωστικά μέσα της ενδομητρίωσης. Έτσι προτάθηκε το όριο των 2pg/ml στον ορό
του αίματος για την IL-6, για να διακρίνουμε με ευαισθησία 90% και ειδικότητα
67% οποιες γυναίκες πάσχουν από ενδομητρίωση. Για τον TNF-a προτάθηκε το όριο
των 15pg/ml στο περιτοναϊκό υγρό, πάνω από το οποίο ανιχνεύουμε με ευαισθησία
100% και ειδικότητα 87% τις γυναίκες που πάσχουν από ενδομητρίωση.(27) Απαιτούνται
περισσότερες μελέτες σε μεγαλύτερα δείγματα πληθυσμού, πριν αυτοί οι δείκτες
χρησιμοποιηθούν ευρέως στην κλινική πράξη ως μη επεμβατικό διαγνωστικό μέσο
της ενδομητρίωσης.
3. Λεπτίνη
Η λεπτίνη αποτελεί ορμόνη που παράγεται στο λιπώδη ιστό και έχει σημαντικό ρόλο
στον μεταβολισμό και την αναπαραγωγική λειτουργία. Σύμφωνα με μια πρόσφατη μελέτη
η συγκέντρωση της λεπτίνης αυξάνεται στατιστικά σημαντικά τόσο στον ορό, όσο
και στο περιτοναϊκό υγρό των γυναικών με ενδομητρίωση. Οι ερευνητές πιστεύουν
πως πιθανώς η λεπτίνη δια μέσου της προφλεγμονώδους και της νεοαγγειογενετικής
δραστηριότητάς της μπορεί να συμμετέχει στην παθογένεση της ενδομητρίωσης.(28)
Υψηλότερες συγκεντρώσεις της λεπτίνης διαπιστώθηκαν στην ενδομητρίωση του περιτοναίου
από ό,τι στην ωοθηκική ενδομητρίωση, γεγονός που υποδηλώνει πως διαφορετικοί
βιοχημικοί μηχανισμοί ευθύνονται για τις δύο μορφές ενδομητρίωσης.(29) Ωστόσο
σύμφωνα με μια άλλη μελέτη σε μεγαλύτερο αριθμό περιστατικών δεν κατέστη δυνατό
να συσχετισθούν τα επίπεδα της λεπτίνης με την ενδομητρίωση.(30) Συνεπώς χρειάζεται
να διεξαχθούν μεγαλύτερες προοπτικές μελέτες, προκειμένου να αποσαφηνιστεί ο
ρόλος της λεπτίνης στην ενδομητρίωση και να χρησιμοποιηθεί στην ευρύτερη κλινική
πράξη.
4. Metrio test
Πρόσφατα αναπτύχθηκε ένα μη επεμβατικό διαγνωστικό μέσο για την ενδομητρίωση,
βασιζόμενο στην ανίχνευση διαφόρων λευκοκυτταρικών υποτύπων στο ενδομήτριο και
στη συσχέτισή τους με το CA-125 του ορού. Συγκεκριμένα, διεξήχθη μια μελέτη
ελέγχου σε οκτώ κέντρα του Καναδά κατά το διάστημα 1997 έως 2001, στην οποία
συμμετείχαν 368 γυναίκες (173 με επιβεβαιωμένη χειρουργικά ή λαπαροσκοπικά ενδομητρίωση
και 195 ως ομάδα ελέγχου). Με τη χρήση της κυτταρομετρίας ροής διαπιστώθηκε
πως η αναλογία οχτώ λευκοκυτταρικών υποτύπων των CD3(+), CD16(+),CD3(-), HLADR(-),
CD3(-)CD45RA(-), CD3(+)CD16(-), CD3(+)CD56(-), CD56(-)CD16(+), CD16b(+) ήταν
στατιστικά σημαντικά διαφορετική στο ενδομήτριο των γυναικών με ενδομητρίωση
σε σχέση με τις γυναίκες της ομάδας ελέγχου. Το μοντέλο αυτό βασίστηκε στα επίπεδα
των συγκεκριμένων λευκοκυτταρικών υποτύπων στο ενδομήτριο και στη συσχέτισή
τους με τα επίπεδα του CA-125 και άλλων παραγόντων όπως ο τόκος, η υπογονιμότητα,
το πυελικό άλγος, η παρουσία ινομυωμάτων και η διάρκεια της εμμήνου ρύσεως.
Έτσι η ειδικότητα του Metrio test αγγίζει το 95% και η ευαισθησία του το 61%
για την ανίχνευση της ενδομητρίωσης όλων των σταδίων, με θετική προγνωστική
αξία 91% και αρνητική προγνωστική αξία 75%. Συνεπώς, ένα θετικό τεστ πρέπει
να ερμηνευτεί από τον κλινικό ιατρό ως ισχυρή ένδειξη ενδομητρίωσης. Με αυτό
τον τρόπο επισπεύδεται η οριστική διάγνωση και θεραπεία της ασθενούς με τη λαπαροσκόπηση.
Αντίθετα, ένα αρνητικό τεστ πρέπει να ερμηνευτεί πως η ασθενής έχει πολύ μικρή
πιθανότητα ενδομητρίωσης, η οποία ωστόσο δεν μπορεί να αποκλεισθεί 100%(31)
5. Αρωματάση Ρ450
Διάφορες μελέτες αναφέρουν πως το ένζυμο αρωματάση Ρ450 που καταλύει τη μετατροπή
των C19 στεροειδών (ανδροστενδιόνη & τεστοστερόνη) σε οιστρόνη, εκφράζεται
στο ενδομήτριο των γυναικών με ενδομητρίωση, αλλά όχι στο ενδομήτριο των υγιών
γυναικών. Επίσης η έκφραση της αρωματάσης είναι ανεξάρτητη από τη φάση του κύκλου,
γεγονός που την καθιστά ιδανικό δείκτη, αφού δεν απαιτεί προγραμματισμένη βιοψία.
Αυτό που αξιολογείται είναι η έκφραση του ενζύμου στο ενδομήτριο ως ποιοτική
εξέταση και όχι η συγκέντρωσή του, διότι διαπιστώθηκε πως αυτή δεν συσχετίζεται
με το στάδιο της νόσου, αλλά και ούτε με τα επίπεδα του CA-125 στον ορό του
αίματος. Συγκεκριμένα στην αναδρομική μελέτη του Κitawaki διαπιστώθηκε η παρουσία
του ενζύμου Ρ450 σε βιοψίες ενδομητρίου σε γυναίκες που έπασχαν από ενδομητρίωση,
αδενομύωση, λειομυώματα και καρκίνο του ενδομητρίου, ενώ ήταν αδύνατη η ανίχνευσή
του στο ενδομήτριο γυναικών που δεν έπασχαν από κάποιο άλλο γυναικολογικό ή
μη νόσημα. Η υψηλή ευαισθησία 91% και η ειδικότητα 100% αυτής της εξέτασης,
σύμφωνα τη συγκεκριμένη μελέτη, υποδηλώνουν πως η ανίχνευση της αρωματάσης Ρ450
μπορεί να βοηθήσει να διακρίνουμε σε επίπεδο εξωτερικού ιατρείου τις γυναίκες
που πάσχουν από οιστρογονοεξαρτώμενη πυελική νόσο. Ιδιαίτερα όταν αυτή η εξέταση
συσχετιστεί με διαγνωστικές απεικονιστικές τεχνικές, η παρουσία της αρωματάσης
Ρ450 βοηθά να διαγνώσουμε την ενδομητρίωση, την αδενομύωση και τα λειομυώματα
ποιο εύκολα και με μεγαλύτερη ακρίβεια. Έτσι, όταν η αδενομύωση, τα λειομυώματα,
οι νεοπλασματικές παθήσεις και η φλεγμονή αποκλεισθούν, τότε η διάγνωση της
ενδομητρίωσης είναι πιο πιθανή. Επιπλέον η αρωματάση Ρ450 στο ενδομήτριο μπορεί
να χρησιμοποιηθεί για τη διάγνωση της υποτροπής της νόσου.(32)
Σύμφωνα με μια άλλη προοπτική μελέτη, η Dheenadaaylu διαπίστωσε πως η έκφραση
της αρωματάσης Ρ450 στο ενδομήτριο με τη μέθοδο της RT-PCR, ως διαγνωστικός
δείκτης για όλα τα στάδια της ενδομητρίωσης, έχει ευαισθησία 82% και ειδικότητα
57%, με θετική προγνωστική αξία 76% και αρνητική προγνωστική αξία 67%. Όμως,
ως διαγνωστική εξέταση για την παρουσία πυελικής νόσου γενικότερα, η ευαισθησία
αυξάνεται στο 85%, η ειδικότητα στο 75% και η θετική προγνωστική αξία στο 89%,
χωρίς μεταβολή της αρνητικής προγνωστικής αξίας που παραμένει σταθερή στο 67%
και εμποδίζει την ευρύτερη εφαρμογή της στην κλινική πράξη.(33)
ΙΙΙ. ΠΡΩΤΟΠΟΡΙΑΚΕΣ ΣΤΡΑΤΗΓΙΚΕΣ ΣΤΗΝ ΕΡΕΥΝΑ ΤΩΝ ΔΕΙΚΤΩΝ ΓΙΑ ΤΗ ΔΙΑΓΝΩΣΗ ΤΗΣ ΕΝΔΟΜΗΤΡΙΩΣΗΣ
Τα τελευταία χρόνια έγινε τεράστια έρευνα για την καταγραφή των γονιδίων (genomics)
του ανθρώπινου DNA, τα οποία είναι περίπου 30.000 με 3 δισεκατομμύρια βάσεις.
Εκπληκτικό όμως είναι το γεγονός πως η διαφοροποίηση των χαρακτηριστικών μεταξύ
των ανθρώπων οφείλεται σε διαφορά 0.1% στην αλληλουχία του DNA. Σήμερα με τη
βοήθεια της μοριακής γενετικής κατέστη δυνατόν να διαπιστωθούν διαφορές στην
έκφραση των γονιδίων. Πρόσφατα ο Eyster ανακάλυψε διαφορές στην έκφραση 8 από
4133 γονίδια μεταξύ φυσιολογικού και έκτοπου ενδομητρίου, στο οποίο αυτά υπερεκφράζονταν.
Περισσότερες μελέτες των γονιδίων που υπερεκφράζονται θα μας οδηγήσουν στην
καλύτερη κατανόηση της φύσης της ενδομητρίωσης και θα ανοίξουν νέους ορίζοντες
στη διάγνωση αλλά και στη θεραπεία της.(34)
Από τη συγκριτική ανάλυση των mRNAs και των πρωτεϊνών βρέθηκε πως τα επίπεδα
των mRNAs δεν συσχετίζονται με τις πρωτεΐνες που τελικά κωδικοποιούν. Έτσι,
ένα γονίδιο μπορεί να κωδικοποιεί πολλές διαφορετικές πρωτεΐνες ανάλογα με τα
σήματα που λαμβάνει από άλλα γονίδια. Έτσι αναπτύχθηκε ο όρος "proteonomics",
ο οποίος αναφέρεται στη νέα βιοτεχνολογία που επιτρέπει την ανίχνευση μεγάλου
αριθμού πρωτεϊνών σε κύτταρα, ιστοτεμάχια ή υγρά του ανθρωπίνου σώματος. Πρόσφατα
αναπτύχθηκε ένα μοντέλο proteonomics με συγκεκριμένες πρωτεΐνες για την ανακάλυψη
του καρκίνου των ωοθηκών με ευαισθησία 100% και ειδικότητα 95%, βασισμένο σε
μια πρόσφατη μελέτη στον ορό 116 γυναικών. Υπάρχει η πεποίθηση πως η χρήση της
βιοτεχνολογίας για τον εντοπισμό συγκεκριμένων γονιδίων και πρωτεϊνών υπο τη
μορφή chips θα συμβάλλει στην έγκαιρη και ακριβή διάγνωση αλλά και θεραπεία
διαφόρων παθήσεων με μια απλή εξέταση αίματος.
Καταβάλλονται προσπάθειες προκειμένου να αναπτυχθούν μονοκλωνικά αντισώματα
συζευγμένα με παραμαγνητικά λιποσωμάτια έναντι συγκεκριμένων αντιγόνων των ενδομητριωσικών
εστιών, έτσι ώστε το σύμπλεγμα αντιγόνου-αντισώματος να είναι φωτοτοξικό, και
ο γυναικολόγος να πραγματοποιεί in situ κατευθυνόμενη καταστροφή των ενδομητριωσικών
εστιών. Δυστυχώς δεν επιτεύχθηκε μέχρι σήμερα η ανακάλυψη αντιγόνων αποκλειστικών
των ενδομητριωσικών κυττάρων.
ΣΥΜΠΕΡΑΣΜΑΤΑ
Η διάγνωση της ενδομητρίωσης εξακολουθεί να αποτελεί μια πρόκληση. Παρά τις
εκταμένες έρευνες για καινούργιες διαγνωστικές ορολογικές εξετάσεις και την
ύπαρξη προηγμένων απεικονιστικών μεθόδων, δεν υπάρχει προς το παρόν μια απλή
διαγνωστική μη επεμβατική εξέταση παθογνωμονική της ενδομητρίωσης με διαγνωστική
ακρίβεια 100%.
Summary
Tsolakidis D, Pados G, Tsalikis T, Bontis J.
Diagnostic approach of endometriosis.
Hellen Obstet Gynecol 16(4): 407-416, 2004
Endometriosis represents a common gynaecologic disorder of the reproductive
age. Its definite diagnosis is based on histologic identification of ectopic
endometrial glands and stroma. Both clinical diagnosis and noninvasive laboratory
investigations remain problematic. This article reviews the degree of progression
in noninvasive diagnostic procedures and particular in Doppler ultrasound, magnetic
resonance imaging (MRI) and serum markers like CA-125, cytokines and aromatase
P450, for the improved recognition of endometriosis in asymptomatic women and
in women with pelvic pain or infertility. Finally, emphasis is given in identification
of genes, protein patterns (proteonomics) and specific antibodies for the diagnosis
and treatment of endometriosis.
Key words:
Endometriosis, Doppler ultrasound, magnetic resonance imaging, CA-125, cytokines.
ΒΙΒΛΙΟΓΡΑΦΙΑ
1. Βαβίλης Δ. Ενδομητρίωση-Αδενομύωση. Μπόντης Ι. Βασικές γνώσεις Μαιευτικής
& Γυναικολογίας. 1η έκδ.University Studio Press 2002:261-266.
2. Verkauf B. The incidence, symptoms and signs of endometriosis in fertile
and infertile women. J Flu Med Assoc 1987; 74:671.
3. DΥHooghe T, Hill J. Endometriosis. In: Berek J. NovakΥs gynecology 13th ed.
Lippincott W&W 2002:931-972.
4. Brosens J, Timmerman D, Starzinski-Powitz A, et al. Noninvasive diagnosis
of endometriosis: the role of imaging and markers. Obstet Gynecol Clin N Am
2003; 30:95-114.
5. Allem F, Pennisi J, Zeitoun K, et al. The role of color Doppler in diagnosis
of endometriomas. Ultrasound Obstet Gynecol 1995; 5(1):51-54.
6. Guerriero S, Ajossa S, Mais, et al. The diagnosis of endometriomas using
colour Doppler energy imaging. Hum Reprod 1998; 13(6):1691-1695.
7. Alcazar Juan. Transvaginal colour Doppler in patients with ovarian endometriomas
and pelvic pain. Hum Reprod 2001; 16(12):2672-2675.
8. Alcazar J, Laparte C, Jurado M, et al. The role of transvaginal ultrasonography
combined with color velocity imaging and pulsed Doppler in the diagnosis of
endometrioma. Fertil Steril 1997; 67(3):487-491.
9. Κurjak A, Kupesic S. The assessment of ovarian lesions by 3D power Doppler.
In: color Doppler in obstetrics, gynaecology and infertility. Art Studio Azinovic-Medison
1999; 6:82-85.
10. Bazot M, Detchev R, Cortez A, et al. Transvaginal sonography and rectal
endoscopic sonography for the assessment of pelvic endometriosis: a preliminary
comparison. Hum Reprod 2003; 18(8):1686-1692.
11. Chapron C, Dumontier I, Dousset B, et al. Results and role of rectal endoscopic
ultrasonography for patients with deep pelvic endometriosis. Hum Reprod 1998;
13(8):2266-2270.
12. Fedele L, Bianchi S, Portuese A, et al. Transrectal ultrasonography in the
assessment of rectovaginal endometriosis. Obstet Gynecol 1998; 91(3):444-448.
13. Balleyguier C, Chapron C, Dubuisson J, et al. Comparison of magnetic resonance
imaging and transvaginal ultrasonography in diagnosing bladder endometriosis.
J Am Assoc Gynecol Laparosc 2002; 9(1):15-23.
14. Alexiadis G, Lambropoulou M, Deftereos S, et al. Abdominal wall endometriosis-ultrasound
research: a diagnostic problem. Clin Exp Obstet Gynecol 2001; 28:121-122.
15. Imaoka I, Wada A, Matsuo M, et al. MR imaging of disorders associated with
female infertility: use in diagnosis, treatment, and management. Radiographics
2003; 23(6):1401-1421.
16. Haimavici J, Tempany C. MR of the female pelvis: Benign disease. Applied
Radiology 1997:7-22.
17. Takahashi K, Okada M, Kitao M, et al. Studies on the detection of small
endometrial implants by magnetic resonance imaging using a fat saturation technique.
Gynecol Obstet Invest 1996; 41(3):203-206.
18. Ha H, Lim Y, Suh T, et al. Diagnosis of pelvic endometriosis: fat suppressed
T1-weighted vs conventional MR images. AJR Am J Roentgenol 1994; 163(1):127-131.
19. Βazot M, Darai E, Hourani R, et al. Deep pelvic endometriosis: MR imaging
for diagnosis and prediction of extension of disease. Radiology 2004.
20. Bis K, Vrachliotis T, Agrawal R, et al. Pelvic endometriosis: MR imaging
spectrum with laparoscopic correlation and diagnostic pitfalls. Radiographics
1997; 17(3):639-655.
21. Pittaway D, Fayez J. Serum CA-125 antigen levels increase during menses.
Am J Obstet Gynecol 1997; 156:75-76.
22. Hompes P, Koninckx P, Kennedy S, et al. Serum CA-125 concentrations during
midfollicular phase, a clinically useful and reproducible marker in diagnosis
of advanced endometriosis. Clin Chem 1996; 42:1871-1874.
23. Ben M, Neriman B, Jeroen G, et al. The performance of CA-125 measurement
in the detection of endometriosis: a meta analysis. Fertil Steril 1998; 70(6):1101-1108.
24. Koninckx P, Meuleman C, Oosterlynck D, et al. Diagnosis of deep endometriosis
by clinical examination during menstruation and plasma CA-125 concentration.
Fertil Steril 1996; 65:280-287.
25. Wu M, Ho H. The role of cytokines in endometriosis. Am J Reprod Immunol
2003; 49(5):285-296.
26. Pados G, Zournatzi V, Bontis J, et al. Interleukin-10 and interleukin-12
in the peritoneal fluid of women with endometriosis. Hum Reprod 1998; 13(1),
abstract No 255.
27. Bedaiwy M, Falcone T, Sharma R, et al. Prediction of endometriosis with
serum and peritoneal fluid markers: a prospective controlled trial. Hum Reprod
2002; 17(2):426-431
28. Matarese G, Alviggi C, Sanna V, et al. Increased leptin levels in serum
and peritoneal fluid of patients with pelvic endometriosis. Clin Endocrinol
Metab 2000; 85(7):2483-2487.
29. Placido G, Alviggi C, Carravetta C, et al. The peritoneal fluid concentration
of leptin is increased in women with peritoneal but not ovarian endometriosis.
Hum Reprod 2001; 16(6):1251-1254.
30. Vigano P, Somigliana E, Matrone R, et al. Serum leptin concentrations in
endometriosis.Clin Endocrinol Metab 2002; 87(3):1085-1087.
31. Gagne D, Rivard M, Page M, et al. Development of a non-surgical diagnostic
tool for endometriosis based on the detection of endometrial leukocyte subsets
and serum CA-125.
32. Kitawaki J, Kusuki I, Koshiba H, et al. Detection of aromatase cytochrome
P450 in endometrial biopsy specimens as a diagnostic test for endometriosis.
Fertil Steril 1999; 72(6):1100-1106.
33. Dheenadayalu K, Mak I, Gordts S, et al. Aromatase P450 messenger RNA expression
in eutopic endometrium is not a specific marker for pelvic endometriosis. Fertil
Steril 2002; 78(4):825-829.
34. Eyster K, Boles A, Brannian J, et al. DNA microarray analysis of gene expression
markers of endometriosis. Fertil Steril 2002; 77(1):38-42.