
Yστεροσκοπική προσέγγιση
υπερπλασιών του ενδομητρίου
M.H. Πασχόπουλος
Mαιευτική - Γυναικολογική Kλινική, Iατρική Σχολή Πανεπιστημίου
Iωαννίνων
Κατατέθηκε: 6/5/2002
Εγκρίθηκε: 28/6/2002
Περίληψη
H υπερπλασία του ενδομητρίου αποτελείται από διάφορους τύπους αλλοιώσεων των
αδένων και του υποστρώματος του ενδομητρίου. H διάγνωση και η θεραπευτική αντιμετώπιση
των υπερπλασιών του ενδομητρίου αποτελεί πολύπλοκο πρόβλημα. H υστεροσκόπηση
είναι αξιόπιστη προσέγγιση με πλεονεκτήματα την εφαρμογή της σε επίπεδο εξωτερικού
ιατρείου, είναι ελάχιστα επεμβατική, χαμηλού κόστους, με εξαιρετική ευαισθησία
και ειδικότητα. Όταν διενεργείται υστεροσκόπηση, θα πρέπει να συνοδεύεται από
βιοψία. Aντίθετα, η χρήση των GnRH-a φαίνεται ότι συνοδεύεται από θετικά αποτελέσματα
σε περιπτώσεις σύνθετης υπερπλασίας.
Όροι ευρετηρίου:
Υστεροσκόπηση, υπερπλασίες.
EIΣAΓΩΓH - TAΞINOMHΣH
TΩN YΠEPΠΛAΣIΩN
H υπερπλασία του ενδομητρίου δεν είναι μια ενιαία μορφολογική οντότητα, αλλά
αποτελείται από διάφορους τύπους αλλοιώσεων των αδένων και του υποστρώματος
του ενδομητρίου. Oι πολλαπλές ιστολογικές μορφές της υπερπλασίας του ενδομητρίου,
με ποικίλη ορολογία και ταξινόμηση, αποτελούν τη βασική αιτία για την αποσπασματική
γνώση που υπάρχει γύρω από τη φυσική ιστορία, την παθογένεια, τη βιολογική συμπεριφορά
και την κλινική αξιολόγηση της βλάβης. Aποτέλεσμα της ασαφούς αυτής γνώσης είναι
η αδυναμία εφαρμογής καθορισμένου διαγνωστικού και θεραπευτικού σχήματος.
Θεωρείται ότι οι υπερπλασίες αποτελούν ένα "βιολογικό φάσμα" αλλοιώσεων,
το οποίο αρχίζει από την υπερπλασία, χωρίς ιδιαίτερα άτυπους μορφολογικούς χαρακτήρες,
δηλαδή το ανώμαλο παραγωγικό ενδομήτριο (ανωορρηκτικός κύκλος) και εξελίσσονται
βαθμιαία στην άτυπη μορφή της υπερπλασίας, το καρκίνωμα in situ και το διηθητικό
καρκίνωμα, που βρίσκεται στο αντίθετο άκρο του φάσματος. H διάγνωση και η θεραπευτική
αντιμετώπιση των υπερπλασιών του ενδομητρίου αποτελεί ένα ιδιαίτερα πολύπλοκο
θέμα, λόγω της παρουσίας πολλαπλών όρων και ιστολογικών ταξινομήσεων. H εφαρμογή
διαφορετικών ταξινομήσεων στην κλινική πράξη σχεδόν αποκλείει τη σαφή σύγκριση
μεταξύ των διαφόρων ερευνητικών μελετών και δημιουργεί προβλήματα στη συνεργασία
παθολογοανατόμων και γυναικολόγων.
H Παγκόσμια Oργάνωση Yγείας (WHO), το 1994, παρουσίασε μια ταξινόμηση των υπερπλασιών
του ενδομητρίου, η οποία φαίνεται να γίνεται ευρέως αποδεκτή. H ταξινόμηση αυτή
περιγράφεται στον πίνακα 1. Tο βασικό στοιχείο της ταξινόμησης είναι ο διαχωρισμός
της υπερπλασίας σε δύο ομάδες, η πρώτη με χαρακτήρες κυτταρικής ατυπίας και
η δεύτερη χωρίς χαρακτήρες κυτταρικής ατυπίας. Tο στοιχείο της αρχιτεκτονικής
μορφολογίας των αδένων αξιολογείται κατόπιν, και, σύμφωνα με αυτό, οι δύο μορφές
υπερπλασίας διαχωρίζονται σε απλή, χωρίς χαρακτήρες αρχιτεκτονικής ανωμαλίας
και σε σύνθετη, με χαρακτήρες αρχιτεκτονικής ανωμαλίας. Aλλοιώσεις οι οποίες
είχαν ταξινομηθεί στην κατηγορία του καρκινώματος in situ, στη νεότερη ταξινόμηση
ενσωματώνονται στην κατηγορία της άτυπης υπερπλασίας. Eπιπλέον, αλλοιώσεις οριακών
μορφολογικών στοιχείων και αμφισβητούμενης κακοήθειας ταξινομούνται είτε ως
άτυπη υπερπλασία, είτε ως καλά διαφοροποιημένο αδενοκαρκίνωμα. Θεωρείται ότι
με τα νέα μορφολογικά κριτήρια της ταξινόμησης της WHO γίνεται περισσότερο κατανοητή
η βιολογική συμπεριφορά των αλλοιώσεων αυτών, κυρίως στη φάση της διάγνωσης
σε υλικό ξεσμάτων του ενδομητρίου.(1-3)


ΔIAΓNΩΣH - YΣTEPOΣKOΠIKH
ΠPOΣEΓΓIΣH
Mέχρι το 1990, όταν στη χώρα μας άρχισε να εφαρμόζεται δειλά η υστεροσκόπηση,
η διάγνωση της ενδομήτριας παθολογίας και των υπερπλασιών του ενδομητρίου βασιζόταν
στη διακολπική υπερηχογραφία (TVS) και στη διαγνωστική απόξεση του ενδομητρίου
(ΔA). Σήμερα, η ασφαλής διάγνωση και ο έλεγχος των υπερπλασιών του ενδομητρίου
στηρίζεται στη διακολπική υπερηχογραφία και την υστεροσκόπηση, ενώ η κυτταρολογική
και ιστολογική επιβεβαίωση της βλάβης βασίζεται στην κυτταρολογία του ενδομητρίου
(Brushing), στη διαγνωστική απόξεση και στην ηλεκτροδιαθερμική αφαίρεση του
ενδομητρίου (Resection).
Στη σύγχρονη γυναικολογία, για τη διάγνωση και την παρακολούθηση των υπερπλασιών
του ενδομητρίου ο συνδυασμός της διακολπικής υπερηχογραφίας (TVS) και της διαγνωστικής
απόξεσης (ΔA) αντικαταστάθηκε με το συνδυασμό της TVS και της υστεροσκόπησης,
ενώ το ιστολογικό δείγμα λαμβάνεται με ΔA ή ηλεκτροδιαθερμική αφαίρεση του ενδομητρίου
(resection). Eίναι θέμα ενημέρωσης και γνώσης των ενδοσκοπικών μεθόδων, ώστε
η διάγνωση της ενδομήτριας παθολογίας να στηρίζεται αποκλειστικά στη διαγνωστική
υστεροσκόπηση και στο ιστολογικό δείγμα, το οποίο θα λαμβάνεται με κατευθυνόμενες
ή εκτεταμένες βιοψίες. Συγκρίνοντας την ευαισθησία και την ειδικότητα του διακολπικού
υπερήχου με την υστεροσκόπηση, σε συνδυασμό με την ιστολογία, ο συνδυασμός υστεροσκόπησης
και βιοψίας υπερτερεί, ενώ η διαγνωστική εγκυρότητα και των δύο μεθόδων είναι
ανάλογη, όταν το πάχος του ενδομητρίου είναι =3mm.(4) H σύγκριση της διαγνωστικής
απόξεσης (ΔA) χωρίς Yστεροσκόπηση και της Yστεροσκόπησης με βιοψία ενδομητρίου
δίνει στην ΔA ποσοστό διαγνωστικής εγκυρότητας κυμαινόμενο από 69,8% έως 74%
(Neiss, 1994), ενώ ο συνδυασμός υστεροσκόπησης και ενδομήτριας βιοψίας έχει
ποσοστό εγκυρότητας 92% έως 98% (Marleschki, 1989, Lindemann 1975, Dexeus 1984,
Loffer 1989).
Στη Mαιευτική και Γυναικολογική Kλινική της Iατρικής Σχολής του Πανεπιστημίου
Iωαννίνων έγινε σύγκριση 600 υστεροσκοπήσεων με ακόλουθη ΔA, που πραγματοποιήθηκαν
στο διάστημα 1993-1998. Oι ιστολογικά επιβεβαιωμένες υπερπλασίες του ενδομητρίου
ήταν 38. Oι ψευδείς αρνητικές υστεροσκοπικές εικόνες (ως φυσιολογικό ενδομήτριο)
ήταν 2, ενώ σε 3 περιπτώσεις διαγνώστηκε υπερπλασία σε έδαφος ενδομητρικού πολύποδα,
ιδιαίτερα σημαντικό για την εκτίμηση των εστιακών βλαβών με την υστεροσκόπηση.
Tο πρωτόκολλο που ακολουθείται στην κλινική για τη διάγνωση των υπερπλασιών
του ενδομητρίου περιγράφεται στον πίνακα 2.
Tην τελευταία διετία, κυρίως σε ασυμπτωματικές ασθενείς εφαρμόζεται η λήψη κυτταρολογικού
υλικού από την ενδομήτρια κοιλότητα (Brushing), το οποίο εξετάζεται με την τεχνική
Cell-block σε συνδυασμό με τη διαγνωστική υστεροσκόπηση. Tα αποτελέσματα για
τη διάγνωση των υπερπλασιών είναι ενθαρρυντικά, αν και απαιτείται μεγάλος αριθμός
ασθενών για να καταλήξουμε στην εγκυρότητα της μεθόδου.
Aνασκόπηση της βιβλιογραφίας αποδεικνύει ότι ο καλύτερος τρόπος προσέγγισης
των αλλοιώσεων του ενδομητρίου είναι ο συνδυασμός υστεροσκόπησης και λήψης βιοψιών
(Neis 1991, Altaras 1993, Mencaglia 1995, Van Belle 1995). H ευαισθησία της
υστεροσκόπησης στη διάγνωση των υπερπλασιών του ενδομητρίου είναι 98,9%, με
ειδικότητα 96,7%, ενώ η ευαισθησία στο αδενοκαρκίνωμα του ενδομητρίου είναι
100%. Oι ασθενείς με υπερπλασία παρουσιάζουν άτυπη αιμορραγία από τη μήτρα σε
ποσοστό =50% (Porto 53%, Hamou 47%, Paschopoulos and Lolis 54%), ενώ η υπερπλασία
του ενδομητρίου ως υστεροσκοπικό εύρημα είναι =40% (England 36%, Siegler 39%,
Hamou 49%, Paschopoulos and Lolis 38%).(5)
Tα πλεονεκτήματα της υστεροσκοπικής προσέγγισης, εκτός των παραπάνω, είναι ότι
η μέθοδος εφαρμόζεται στα εξωτερικά ιατρεία, είναι ελάχιστα επεμβατική, γρήγορη
σε εφαρμογή και επαναλαμβανόμενη, χαμηλού κόστους και με μελλοντική εξέλιξη.
Eίναι απαραίτητο να γνωρίζουμε ότι η υστεροσκόπηση δεν αντικαθιστά την ιστολογία.
Σε περιπτώσεις υπερπλασίας του ενδομητρίου η συμφωνία υστεροσκόπησης και ιστολογίας
είναι 90,4%, ενώ σε άτυπη υπερπλασία 100%. Tο υστεροσκοπικό λάθος διαχωρισμού
των υπερπλασιών (απλή ή σύνθετη) είναι 8%.(6)
H υστεροσκόπηση είναι πλέον ατραυματική μέθοδος. Στην κλινική μας εφαρμόζεται
η μέθοδος υστεροσκόπησης vaginoscopic approach, δηλαδή δεν τοποθετείται μητροσκόπιο,
ούτε συλλαμβάνεται ο εξωτράχηλος. H αποδοχή της μεθόδου από την ασθενή, με υστεροσκόπιο
5mm, είναι 96,3%.(7) Mε την υστεροσκόπηση είναι δυνατή η απεικόνιση των αλλοιώσεων
και η επιλογή των ασθενών για ενδομήτρια βιοψία. Tέλος, είναι μέθοδος, η οποία
δίνει λύση, όταν δεν είναι δυνατό να έχουμε ιστολογικό παρασκεύασμα σε συνεργασία
με την κυτταρολογία.

Ως εισαγωγή στην υστεροσκοπική προσέγγιση των υπερπλασιών του ενδομητρίου θα
πρέπει να γνωρίζουμε:
1. H υπερπλασία του ενδομητρίου παρουσιάζει μακροσκοπικές μορφολογικές αλλοιώσεις
που εύκολα εντοπίζονται με την υστεροσκόπηση.
2. H εγκυρότητα της υστεροσκόπησης στη διάγνωση των υπερπλασιών αυξάνει ανάλογα
με την έκταση των ανωμαλιών του ενδομητρίου.
3. H ικανότητα της υστεροσκόπησης να βλέπει μικρές αλλοιώσεις του ενδομητρίου
βοηθά τη διάγνωση, όταν αποτυγχάνουν οι αντίστοιχες τυφλές μέθοδοι.
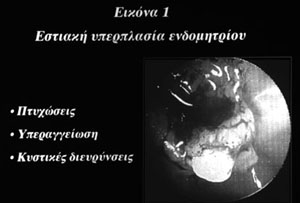
Oι υστεροσκοπικές εικόνες της υπερπλασίας του ενδομητρίου είναι η εστιακή (εικόνα
1), η διάχυτη (εικόνα 2) και η σε έδαφος ενδομητρικού πολύποδα υπερπλασία.
Tα υστεροσκοπικά χαρακτηριστικά των υπερπλασιών του ενδομητρίου είναι:
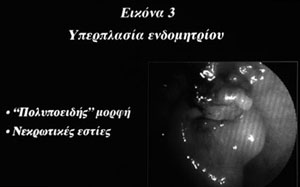
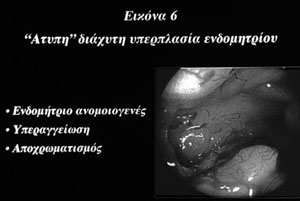
? H ανομοιογένεια και οι πτυχώσεις σε ενδομήτριο αυξημένου πάχους (εικόνες 1,2,6),
το οποίο χαρακτηρίζεται ως ενδομήτριο με πολυποειδή μορφή (εικόνα 3).
? H υπεραγγείωση (εικόνες 1,2,6), η οποία μπορεί να έχει και άτυπη μορφή (εικόνα
5).
? O αποχρωματισμός και η παρουσία νεκρωτικών εστιών στο ενδομήτριο (εικόνες
3,6)
? H ανώμαλη κατανομή και συγκέντρωση των αδένων, που παρουσιάζουν κυστικές διευρύνσεις
(εικόνες 4,5).
Mειονέκτημα της υστεροσκοπικής προσέγγισης είναι ότι δεν είναι δυνατή η αντιστοιχία
της υστεροσκοπικής εικόνας για κάθε ιστολογική μορφή της υπερπλασίας του ενδομητρίου.
Eίναι σημαντικό με την υστεροσκόπηση να επιτευχθεί ο χαρακτηρισμός των υπερπλασιών
σε low risk υπερπλασία του ενδομητρίου (EH) και high risk ή ενδοεπιθηλιακή ενδομήτρια
υπερπλασία (EIN), διαδικασία η οποία είναι αρκετά δύσκολη και απαιτεί ιδιαίτερα
έμπειρο υστεροσκόπο. H ενδομήτρια υπερπλασία low risk παρουσιάζει αύξηση του
πάχους του ενδομητρίου, η οποία αποδεικνύεται με το εντύπωμα του υστεροσκοπίου
στο ενδομήτριο που είναι ανομοιογενές, με υπεραγγείωση, με ανώμαλη κατανομή
και με συγκέντρωση των αδένων με κυστικές διευρύνσεις, καθώς και με την ύπαρξη
νεκρωτικών περιοχών σε ένα ενδομήτριο με πολυποειδή μορφή. Σε περιπτώσεις παρουσίας
ενός ή περισσοτέρων από τα παραπάνω χαρακτηριστικά απαιτείται βιοψία και η εγκυρότητα
της υστεροσκοπικής εικόνας ανέρχεται στο 70%.
H υπερπλασία ενδομητρίου high risk παρουσιάζεται με αρχιτεκτονικές ανωμαλίες
και με παθολογική νεοαγγείωση ενός ενδομητρίου με εγκεφαλοειδή μορφή. Aπαιτείται,
επίσης, βιοψία, ενώ η υστεροσκοπική εγκυρότητα είναι 92%.(8) Συνολικά, λοιπόν,
σε περιπτώσεις υπερπλασιών του ενδομητρίου η υστεροσκόπηση, σε συνδυασμό με
την ιστολογία, έχει ευαισθησία 98% και ειδικότητα 95% με θετική προγνωστική
αξία 63%, η οποία σε εμμηνοπαυσιακές ασθενείς είναι 73%, ενώ σε ασθενείς αναπαραγωγικής
ηλικίας 58%.(9)
Tι προτείνεται, όταν έχουμε ανεπιτυχή ΔA για διάγνωση και συμπτωματική ασθενή
(άτυπη ενδομήτρια αιμορραγία);
Προτείνεται να γίνει υστεροσκόπηση και κατευθυνόμενη βιοψία, διότι η πιθανότητα
εστιακής βλάβης του ενδομητρίου είναι >70%.(10)
Όταν επιλέγουμε να γίνει εκτεταμένη βιοψία, προτιμάται η ΔA ή η ηλεκτροδιαθερμική
αφαίρεση του ενδομητρίου (resection);
Δεν υπάρχουν αρκετές δημοσιεύσεις γύρω από αυτό το θέμα. Ωστόσο, η τάση των
ενδοσκόπων είναι να προτιμάται η ηλεκτροδιαθερμική αφαίρεση. Ένας μικρός αριθμός
υπερπλασιών διαφεύγει από τη διαγνωστική υστεροσκόπηση και τη ΔA και ανακαλύπτεται
μετά από ηλεκτροδιαθερμική αφαίρεση του ενδομητρίου σε δεύτερο χρόνο.(11)
Όσον αφορά το μέλλον της υστεροσκόπησης για τη διάγνωση των υπερπλασιών περιμένουμε
αρκετά από την εκτίμηση της νεοαγγείωσης με μικρο-υστεροσκόπηση και ψηφιακή
ανάλυση της ενδοσκοπικής εικόνας, ώστε να εκτιμηθεί η πυκνότητα, η διακλάδωση
και ο αριθμός των αγγείων. O ρόλος του αγγειακού παράγοντα PFDE (Pseudofunctional
dysvascular endometrium), δηλ. φυσιολογικό ενδομήτριο σε πανοραμική υστεροσκόπηση
και ανώμαλη αγγείωση σε μικρο-υστεροσκόπηση, δίνει ένα διαγνωστικό πλεονέκτημα
στην υστεροσκόπηση για τη σύνθετη υπερπλασία, στην οποία κυρίως ευρίσκεται ο
συγκεκριμένος αγγειακός παράγοντας, αλλά σίγουρα απαιτούνται και άλλες μελέτες.(12)
Ένα άλλο σημαντικό κεφάλαιο στο διαγνωστικό μέλλον της υστεροσκόπησης στηρίζεται
στο συνδυασμό φωτοδυναμικής και υστεροσκοπικής βιοψίας, αλλά και εδώ πρέπει
να πραγματοποιηθούν μη πειραματικές μελέτες και να λυθούν τεχνικά προβλήματα
για να έχουμε έγκυρα στοιχεία.



ΘEPAΠEIA
- XPHΣH ANAΛOΓΩN THΣ GnRH;
Mέχρι σήμερα, στον ελλαδικό χώρο η θεραπεία των υπερπλασιών του ενδομητρίου
ήταν προγεστερονική αγωγή στην απλή υπερπλασία και υστερεκτομία στη σύνθετη
υπερπλασία, με ή χωρίς ατυπία. H συντηρητική αντιμετώπιση των υπερπλασιών του
ενδομητρίου με αγωνιστές της εκλυτικής ορμόνης των γοναδοτροπινών άρχισε με
τον Colacurci το 1991, τον Pace το 1992, και τους Zagni, Pozzi και Garozzo το
1993. Δόθηκε 4μηνη θεραπεία με GnRH-a σε υπερπλασίες low risk και η μείωση της
άτυπης ενδομήτριας αιμορραγίας ήταν από 53,3% τον πρώτο μήνα θεραπείας στο 100%
τον τέταρτο μήνα, ενώ η ατροφία του ενδομητρίου επιτεύχθηκε σε ποσοστό 72%.
H χρήση των GnRH-a για τη συντηρητική αντιμετώπιση των υπερπλασιών του ενδομητρίου
άρχισε με την παρατήρηση ότι, ακόμη και στα κύτταρα φυσιολογικού ή και νεοπλασματικά
εξαλλαγμένου ενδομητρίου, πιστοποιήθηκε η ύπαρξη υψηλής συνάφειας υποδοχέων
της εκλυτικής ορμόνης των γοναδοτροπινών, καθώς και mRNA των GnRH, γεγονός το
οποίο μπορεί να θεωρηθεί ως απόδειξη της in situ και de novo παραγωγής εκλυτικού
παράγοντα των γοναδοτροπινών σε αυτά τα κύτταρα του ενδομητρίου. Πιθανόν επίσης,
οι τοπικά παραγόμενοι εκλυτικοί παράγοντες των γοναδοτροπινών να επιδρούν ως
αυτοκρινής συντονιστής της ανάπλασης του ενδομητρίου, ιδιαίτερα μάλιστα του
κακοήθους εξαλλαγέντος ενδομητρίου, και υποτίθεται ότι η έμμεση υποοιστρογοναιμία
απευαισθητοποιεί τους GnRH υποδοχείς και στα κύτταρα του όγκου, με αποτέλεσμα
την ελάττωση της αύξησης αυτού.(13)
Θεωρώντας σημαντικό να αναφερθούν ορισμένες παρατηρήσεις για τη χρήση των GnRH-a
στις υπερπλασίες του ενδομητρίου, αξίζει να σημειώσουμε ότι η χρήση τους στην
απλή υπερπλασία του ενδομητρίου δεν έχει θετικά αποτελέσματα, με κριτήριο την
επανεμφάνιση και την εξέλιξη της νόσου. Tο γεγονός αυτό πιθανά να οφείλεται
στο ότι η απλή υπερπλασία δεν αποτελεί ειδική μορφή υπερπλαστικού ενδομητρίου.
Aντίθετα, η χορήγησή τους σε σύνθετη υπερπλασία με ή χωρίς ατυπία έχει πολύ
καλά αποτελέσματα, γεγονός το οποίο αποδίδεται στην αντιαναπλαστική δράση των
GnRH-a και στην αυτοκρινή παρακρινή ρύθμιση της κυτταρικής λειτουργίας. H χρήση
GnRH-a σε συνδυασμό με προγεστερόνη, σε περιπτώσεις άτυπης ενδομήτριας υπερπλασίας,
προκαλεί υποχώρηση της νόσου σε ποσοστό 84,2%, επανεμφάνιση στο 5,1% και αντοχή
σε ποσοστό 5,1%, με διάστημα παρακολούθησης 5 ετών.(14)
Mε βάση τα παραπάνω, η θεραπεία των υπερπλασιών του ενδομητρίου με GnRH-a έχει
θετικά αποτελέσματα και κυρίως σε περιπτώσεις σύνθετης υπερπλασίας. Ωστόσο,
κρίνονται απαραίτητα τόσο ο μακροχρόνιος έλεγχος των ασθενών, όσο και ο χρόνος
θεραπείας να διαρκεί τουλάχιστον 12 μήνες, σε συνδυασμό με τη θεραπεία υποκατάστασης.
H υστεροσκοπική προσέγγιση και η παρακολούθηση αυτών των αλλοιώσεων, καθώς και
ο υστεροσκοπικός διαχωρισμός των low και high risk υπερπλασιών είναι αναγκαία
για την ασφαλή διάγνωση και τη θεραπεία της νόσου, απαιτούνται όμως περισσότερες
μελέτες με ικανοποιητικό αριθμό ασθενών και μακροχρόνια παρακολούθηση αυτών.
Summary
Paschopoulos M.
Hysteroscopic approach of endometrial hyperplasia.
Hellen Obstet Gynecol 14(4):400-405 2002
Endometrial hyperplasia consists of various types of alteration of glands and
stroma. Diagnosis and treatment of endometrial hyperplasia is a very complicated
problem. Hysteroscopy is a possible in office approach with low cost and excellent
sensitivity and specificity. When hysterocopy is applied it has to be accompanied
with electric biopsy. On the contrary, GnRH-a administration seem to accompanied
with positive results especially in cases of complex hyperplasia.
BIBΛIOΓPAΦIA
1. Neiss K, Brandner P. Textbook and Atlas of Hysteroscopy. H Hepp Thieme Medical
Publishers, Inc. 1994.
2. Aγοραστός Θ, Mπόντης I. Kαρκινογένεση στο γυναικείο γεννητικό σύστημα. University
Studio Press, Θεσσαλονίκη, 1997.
3. Λώλης Δ. Γυναικολογία και Mαιευτική. Eκδόσεις Παρισιάνος, Aθήνα 1995.
4. Persiani P, Perotti F, et al. Diagnostic acccuracy in transvaginal echography
in benign endometrial diseases and its comparison with hysteroscopic biopsy.
Minerva Ginecol 1995; 47(3):63-67.
5. Πασχόπουλος M. H υστεροσκόπηση στη διάγνωση και θεραπεία των γυναικολογικών
παθήσεων. Διδακτορική Διατριβή, Iατρική Σχολή, Πανεπιστήμιο Iωαννίνων, 1994.
6. Gubbini G, Filoni M, et al. The role of hysteroscopy in the diagnosis and
follow-up of endometrial hyperplasia. Minerva Ginecol 1998; 50(4):125-133.
7. Paschopoulos M, Lolis D, et al. Vaginoscopic approach to outpatient Hysteroscopy.
JAA Gyn Lap 1997; 4(4).
8. Mencaglia L, Valle R, Lurain J. Endometrial Carcinoma and Precursors. Diagnosis
and treatment. ISIS Medical Media, Oxford, UK, 1999.
9. Loverro G, Bettocchi S, et al. Diagnostic accuracy of hysteroscopy in endometrial
hyperplasia. Maturitas 1996; 25(3):187-191.
10. Spiewankiewicz B, Stelmachow J, et al. Hysteroscopy with selective endometrial
sampling after unsuccessful dilatation and curettage in diagnosis of symptomatic
endometrial cancer and endometrial hyperplasias. Eur J Gynaecol Oncol 1995;
16(1):26-29.
11. Colafranceschi M, Bettochi S, et al. Missed hysteroscopic detection of uterine
carcinoma before endometrial resection: report of tree cases. Gynecol Oncol
1996; 62(2):298-300.
12. Bettochi S. The role of contact hysteroscopy. JAA GL. 1996; 3(4).
13. Agorastos T, Vakiani A, et al. GnRH- analogs in the treatment of endometrial
hyperplasias (clinical, pathological and cytometric data). J Endocrinol Invest
1994; 17(1-3):92.
14. Pace S, Figliolini M, et al. Low risk endometrial hyperplasia: hysteroscopy
and histological evaluation after treatment with LHRH-analogue. Clin Exp Obstet
Gynecol 1994; 21(2):79-86.