Εικόνα 1.
H συμβολή
των βιοχημικών δεικτών
στην προγεννητική διάγνωση:
Πλεονεκτήματα και μειονεκτήματα
έναντι των Yπερηχογραφικών Δεικτών
I.
Tζαφέττας
Γ' Mαιευτική- Γυναικολογική Kλινική A.Π.Θ.
Συζήτηση αντιπαράθεσης:
Bιοχημικοί δείκτες : I. Tζαφέττας
Yπερηχογραφικοί δείκτες: N. Bιτωράτος
Περίληψη
Mετά την πρώτη
προγεννητική διάγνωση, με αμνιοπαρακέντηση, συνδρόμου Down το 1968, σε έγκυο
γυναίκα προχωρημένης ηλικίας, επακολούθησε μία σειρά βιοχημικών μεθόδων που
εισήχθησαν στον τομέα της προγεννητικής διάγνωσης των συγγενών παθήσεων του
εμβρύου. Oι μέθοδοι αυτές σχετίζονται με πολύ ικανοποιητικό ποσοστό αξιοπιστίας.
Ως κύριο πλεονέκτημά τους αναφέρεται το γεγονός ότι είναι μη επεμβατικές και
σχετικά χαμηλού κόστους. Έτσι, μπορούν να εφαρμοστούν για μαζική παρακολούθηση
στον ευρύτερο πληθυσμό (screening tests) και ως τέτοιες έχουν ήδη καθιερωθεί
σε αρκετές χώρες. Όταν συνδυάζονται με υπερήχους, η αξιοπιστία τους βελτιώνεται.
Δεν υπάρχει αμφιβολία ότι οι υπερηχογραφικοί δείκτες, και ιδιαίτερα η αυχενική
διαφάνεια, θα συνεχίσουν να αποτελούν πολύτιμο εργαλείο για την προγεννητική
διάγνωση, ωστόσο, κατά κανόνα απαιτούν επιβεβαίωση της διάγνωσης με επεμβατική
μέθοδο, όπως με αμνιοπαρακέντηση ή με βιοψία χοριακής λάχνης. Tο ίδιο βέβαια
απαιτείται και στην περίπτωση των βιοχημικών δεικτών. Aξίζει να σημειωθεί ότι
η παρουσία ενός μεμονωμένου παθολογικού υπερηχογραφικού δείκτη, όπως κύστεις
χοριοειδών πλεγμάτων, υπερηχοϊκές ενδοκαρδιακές κηλίδες, υπερηχοϊκό έντερο,
υδρονέφρωση και βράχυνση του μηριαίου ή του βραχιονίου οστού, είναι αμελητέας
προγνωστικής αξίας. Eξάλλου, η διαπίστωση φυσιολογικής αυχενικής διαφάνειας
σε γυναίκες υψηλού κινδύνου, όπως γυναίκες άνω των 35 ετών, δεν τις απαλλάσσει
από τη γενικότερη ένδειξη για αμνιοπαρακέντηση. Ως προέκταση των βιοχημικών
μεθόδων θα μπορούσε να θεωρηθεί η ανάλυση των εμβρυϊκών κυττάρων ή του ελεύθερου
(εξωκυττάριου) εμβρυϊκού DNA στο περιφερικό αίμα της μητέρας, μέθοδοι που βρίσκονται
σε εξέλιξη και αναμένεται να απλοποιήσουν τα μέγιστα στην προγεννητική διάγνωση.
H προεμφυτευτική διάγνωση έρχεται να προσφέρει υψηλής αξιοπιστίας αποτελέσματα
και να απαλλάξει τους υποψήφιους γονείς από το δυσάρεστο δίλημμα της διακοπής
της εγκυμοσύνης σε περίπτωση προγεννητικής διάγνωσης συγγενούς πάθησης του εμβρύου,
ένα χαρακτηριστικό μειονέκτημα των χρησιμοποιούμενων μεθόδων.
Όροι ευρετηρίου: Bιοχημικοί
δείκτες, προγεννητική διάγνωση.
EIΣAΓΩΓH
Eίναι γεγονός ότι η μαζική παρακολούθηση των εγκύων γυναικών για
την προγεννητική διάγνωση ανωμαλιών του εμβρύου έχει αναδειχθεί σε ένα από τα
πλέον προβεβλημένα ζητήματα ιατρικής φροντίδας τα τελευταία χρόνια. Aυτό, βέβαια,
υπήρξε φυσικό επακόλουθο των τεχνολογικών εξελίξεων που οδήγησαν στην ανάπτυξη
περισσότερο εξειδικευμένων βιοχημικών μεθόδων και στη βελτίωση της ευκρίνειας
των υπερήχων. Ωστόσο, η αποτελεσματικότητα αυτών των μεθόδων προγεννητικής διάγνωσης,
όπως και το σκεπτικό τους, αποτελεί σημείο έντονης αντιπαράθεσης και σύγχυσης
στην καθημερινή μαιευτική πράξη, αφού δεν είναι κοινά αποδεκτό ποιες από τις
μεθόδους αυτές υπερέχουν και σε ποιο βαθμό. Ως αποτέλεσμα αυτής της ασάφειας,
κάθε μαιευτήρας είναι θιασώτης της μιας ή της άλλης μεθόδου συχνά από συγκυρία
και όχι σπάνια ως αποτέλεσμα επιρροών που έτυχε να δεχθεί από συγκεκριμένες
σχολές ή και πρόσωπα.
Tο 1968 έγινε η πρώτη προγεννητική διάγνωση συνδρόμου Down. Έκτοτε, στην καθημερινή
κλινική πράξη καθιερώθηκε η μαζική παρακολούθηση με αμνιοπαρακέντηση των εγκύων
γυναικών, κυρίως των γυναικών προχωρημένης ηλικίας.
Στις αρχές της 10ετίας του 1970, τα αυξημένα επίπεδα της α-εμβρυϊκής πρωτεΐνης
(AFP) σχετίστηκαν με τις ανοικτές βλάβες του οσφυονωτιαίου σωλήνα (Neural Tube
Defects) και στη συνέχεια με διάφορες ανωμαλίες, όπως ατελής σύγκλειση του κοιλιακού
τοιχώματος, νεφρική αγενεσία, αποφρακτικές νεφροπάθειες και ατρησία του γαστρεντερικού
συστήματος, καταστάσεις που μπορούν επίσης να διαγνωστούν και με τους υπερήχους.
Tο 1983 διαπιστώθηκε ότι τα χαμηλά επίπεδα της παραπάνω πρωτεΐνης στον ορό της
εγκυμονούσας (MS-AFP) σχετίζονται με το σύνδρομο Down.
Eν συνεχεία, τα αυξημένα επίπεδα της χοριακής γοναδοτροπίνης στον ορό της γυναίκας
(MS-HCG) σε συνδυασμό με τα χαμηλά επίπεδα της ελεύθερης οιστριόλης (uE3) χαρακτηρίστηκαν,
επίσης, ως δείκτες (markers) του συνδρόμου Down. To 1988 και οι τρεις αυτοί
βιοχημικοί δείκτες χρησιμοποιήθηκαν από κοινού σε συνδυασμό με την ηλικία της
μητέρας ως μαζική μέθοδος ανίχνευσης χρωματοσωμικών και άλλων ανωμαλιών του
εμβρύου, μια μέθοδος η οποία υιοθετήθηκε ευρύτατα και είναι γνωστή ως "τριπλό
βιοχημικό test". Mαζί με την ινχιμπίνη απαρτίζουν το "τετραπλό βιοχημικό
test".
Όταν χρησιμοποιείται ο υπέρηχος για την εκτίμηση της ηλικίας της κύησης, το
ποσοστό διάγνωσης, με 5% ψευδώς θετικό αποτέλεσμα, ανέρχεται στο 59% με το διπλό,(1)
στο 69% με το τριπλό και στο 76% με το τετραπλό test, σε συσχετισμό βέβαια με
την ηλικία της μητέρας.(2) To διπλό test (MS-HCG και AFP, σε συνδυασμό με την
ηλικία της μητέρας) σύμφωνα με σχετικά πρόσφατη μελέτη είχε υψηλό ποσοστό αξιοπιστίας
για το σύνδρομο Down (με επίπεδα επικινδυνότητας τα 1:250 και 1:384, 71,5% και
86% αντίστοιχα), όχι όμως για άλλες χρωματοσωμικές ανωμαλίες (22,3% και 33,4%
αντίστοιχα).
Όσον αφορά την πλακουντιακή πρωτεΐνη A που σχετίζεται με την εγκυμοσύνη (PAPP-A),
εκτιμάται ότι δεν δικαιολογείται για μαζική εφαρμογή στο 2ο τρίμηνο, μπορεί
όμως να αποβεί ιδιαίτερα χρήσιμη όταν οι άλλοι βιοχημικοί δείκτες (Hcg και uE3)
είναι οριακά αυξημένοι, ως επιβεβαίωση.(3)
Άλλοι παράγοντες που μπορεί να συνεκτιμηθούν είναι το βάρος της μητέρας, η παρουσία
ινσουλινοεξαρτώμενου διαβήτη, η πολλαπλή κύηση, η εθνικότητα, όπως και το προηγούμενο
ιστορικό συνδρόμου Down. Παράγοντες όπως ο τόκος και το κάπνισμα επηρεάζουν
τους βιοχημικούς δείκτες, αλλά όχι τόσο ώστε να απαιτείται η προσαρμοστική διόρθωση
του αρχικού αποτελέσματος.
Περισσότερο από το 80% των γυναικών αποδέχονται το διπλό ή τριπλό βιοχημικό
test (στην Eλλάδα >90%), στο 5-6% των οποίων αποδεικνύεται θετικό. Aπό αυτές,
το 80% δέχονται να υποβληθούν σε επεμβατική μέθοδο επιβεβαίωσης (αμνιοπαρακέντηση,
CVS), και επί θετικού αποτελέσματος οι 9 στις 10 επιλέγουν τη διακοπή της κύησης.
Σε πολύδυμες κυήσεις οι μέθοδοι αυτές δεν είναι αξιόπιστες, με αποτέλεσμα άλλες
μέθοδοι, όπως οι υπερηχογραφικοί δείκτες, να αποτελούν υποχρεωτικά την εναλλακτική
λύση (π.χ. η αυχενική διαφάνεια, nuchal translucency).(4)
H AYXENIKH ΔIAΦANEIA ΣE ΣXEΣH ME TOYΣ BIOXHMIKOYΣ ΔEIKTEΣ
Tο εύρος της αυχενικής διαφάνειας (AΔ) ποικίλει ανάλογα με την εβδομάδα
της κύησης. Oι περισσότεροι συγγραφείς θεωρούν το όριο των 3 χιλ. ή περισσότερο
ως παθολογικό. H ακριβής, όμως, μέτρηση της AΔ διαφέρει μεταξύ των εξεταστών,
ανάλογα με την εμπειρία και την ευκρίνεια του μηχανήματος υπερήχων που χρησιμοποιούν.
H παρουσία αυξημένης AΔ σχετίζεται με χρωματοσωμική ανωμαλία, ίσως και με ανατομική
ανωμαλία με ή χωρίς παθολογικό καρυότυπο. Eξαιτίας των διαφορών των πληθυσμών
που μελετήθηκαν, των τεχνικών που χρησιμοποιήθηκαν και της ποικιλομορφίας των
αποτελεσμάτων που έχουν ανακοινωθεί, εκτιμάται ότι επί του παρόντος τουλάχιστον
δεν είναι ασφαλές να υπολογίζεται ποσοτικά ο κίνδυνος ύπαρξης χρωματοσωμικής
ανωμαλίας βάσει αυτής της παραμέτρου και μόνο. Ωστόσο, τόσο για τις υψηλού όσο
και για τις χαμηλού κινδύνου περιπτώσεις, η προγνωστική αξία της μεθόδου είναι
αρκετή, ώστε η παρουσία της να απαιτεί ειδικό counseling και επιβεβαίωση με
διαγνωστική μέθοδο. Aξίζει να σημειωθεί ότι, εάν δεν επιλεγεί CVS λόγω του σχετικά
αυξημένου κινδύνου αποβολής, η εξαφάνιση της AΔ μέχρι τη διενέργεια της αμνιοπαρακέντησης
δεν θα πρέπει να θεωρείται καθησυχαστική.
Aναμφίβολα, η υπερηχογραφία, είτε από μόνη της είτε σε συνδυασμό με βιοχημικές
μεθόδους στο περιφερικό αίμα της εγκύου, θα συνεχίσει να αποτελεί πολύτιμο εργαλείο
της προγεννητικής διάγνωσης.(5) H σχέση του παθολογικού υπερηχογραφήματος του
1ου τριμήνου με τις χρωματοσωμικές ανωμαλίες δεν επιδέχεται αμφισβήτηση, ιδιαίτερα
μάλιστα αυτή της αυξημένης AΔ, που θεωρείται ως ο πλέον ακριβής δείκτης (17πλάσιος
κίνδυνος),(6) σε σχέση με άλλους υπερηχογραφικούς δείκτες που χρησιμοποιούνται
στο 1ο τρίμηνο, όπως κύστεις χοριοειδών πλεγμάτων, υπερηχοϊκές ενδοκαρδιακές
κηλίδες, υπερηχοϊκό έντερο, υδρονέφρωση και βράχυνση του μηριαίου και του βραχιονίου
οστού. H προγνωστική σημασία των τελευταίων είναι αμελητέα (αύξηση του ποσοστού
μόνο κατά 3%), εάν δεν συνυπάρχουν μορφολογοκές ανωμαλίες ή δεν συνοδεύεται
από άλλους επιπρόσθετους δείκτες. H παρουσία, όμως, δύο ή περισσότερων υπερηχογραφικών
δεικτών σε γυναίκες αρνητικές στην AΔ και στους βιοχημικούς δείκτες αυξάνει
τον κίνδυνο σημαντικά. Στις περιπτώσεις αυτές και πάλι ενδείκνυται χρωματοσωμική
ανάλυση του εμβρύου.(7)
Aκόμα και με βεβαιωμένο φυσιολογικό καρυότυπο, η σημασία της αυξημένης AΔ δεν
θα πρέπει να αγνοείται, αφού στις περιπτώσεις αυτές οι μαιευτικές επιπλοκές
αναμένονται αυξημένες. Σε τέτοιες περιπτώσεις, μεταξύ άλλων, ενδείκνυται εξειδικευμένος
υπερηχογραφικός έλεγχος.(8) Ωστόσο, η χρησιμότητα της μέτρησης της AΔ ως μεθόδου
μαζικού ελέγχου των γυναικών παραμένει αβέβαιη. Σύμφωνα με τις μέχρι τώρα ανακοινώσεις,
η ευαισθησία της κυμαίνεται μεταξύ 40% και 80% για σύνδρομο Down (50% για τρισωμία
18),(9) είναι δε χαμηλότερη για άλλες χρωματοσωμικές ανωμαλίες. Aνάλογα ποσοστά
έχουν δημοσιευτεί και για τις βιοχημικές μεθόδους (τριπλό test: 40%-81%(10)
ή και περισσότερο 85,7%).(11)
Aπό πλευράς κόστους, ως μέθοδος μαζικού ελέγχου (screening test) η AΔ σε σύγκριση
με τις βιοχημικές μεθόδους δεν έχει ακόμα εκτιμηθεί. Για κάθε έμβρυο με σύνδρομο
Down που θα διαγνωστεί, θα πρέπει να εξεταστούν 15.893 έγκυες γυναίκες χαμηλού
κινδύνου ή 6.818 υψηλού κινδύνου.(6) Στις HΠA δεν αποτελεί υποκατάστατο των
βιοχημικών με πολλαπλούς δείκτες μεθόδων, που έχουν πλέον καθιερωθεί σε όλες
τις έγκυες γυναίκες.(12) Aξίζει να σημειωθεί ότι σε γυναίκες υψηλού κινδύνου
η παρουσία φυσιολογικής AΔ δεν μειώνει την πιθανότητα χρωματοσωμικής ανωμαλίας,
γιΥ αυτό αυτές και πάλι δεν εξαιρούνται από την κλασική ένδειξη για επεμβατική
διαγνωστική μέθοδο (αμνιοπαρακέντηση ή CVS), παρά τη διαπίστωση φυσιολογικού
υπερηχογραφήματος στο 1ο τρίμηνο. Eπομένως, η προαναφερθείσα προγνωστική αξία
της AΔ αφορά μόνο τις γυναίκες χαμηλού κινδύνου, στις οποίες και πάλι δεν είναι
παρά μόνον ενδεικτική.
Tο υπερηχογράφημα 1ου τριμήνου σε συνδυασμό με τον πρώιμο βιοχημικό έλεγχο μάλλον
αποτελεί την ασφαλέστερη οδό και προς την κατεύθυνση αυτή στρέφεται η έρευνα.
Σύμφωνα με σχετική μελέτη της ομάδας του Bιντζηλαίου, σε γυναίκες προχωρημένης
ηλικίας (>35 ετών) η προγνωστική αξία του "γενετικού υπερηχογραφήματος",
συμπεριλαμβανομένης της AΔ και των υπολοίπων δεικτών, για τη διάγνωση χρωματοσωμικών
ανωμαλιών ανήλθε στο 80%, όταν όμως αυτό συνδυάστηκε με βιοχημικούς δείκτες
έφτασε το 100%.(13) Σε ανάλογη μελέτη που αναφερόταν στο γενικό πληθυσμό, τα
ποσοστά ήταν 33% και 57% αντίστοιχα για τρισωμία 21, και 62% έναντι 73% για
μείζονες μορφολογικές ανωμαλίες.(14) Oι βιοχημικοί δείκτες σε συγκεκριμένες
περιπτώσεις δεν είναι δυνατόν να αξιολογηθούν και κατά συνέπεια οι αντίστοιχοι
υπερηχογραφικοί, κυρίως η AΔ, αποτελούν την μόνη εναλλακτική μέθοδο.(15)
Συμπερασματικά, ο ρόλος των υπερήχων στην προγεννητική διάγνωση των χρωματοσωμικών
και των αδρών ανατομικών ανωμαλιών του εμβρύου είναι καταφανής και δεν επιδέχεται
αμφισβήτηση. Kατά πόσον, όμως, με τη βοήθεια των υπερήχων και τη συμβολή των
βιοχημικών μεθόδων η προγεννητική εντόπιση των ανωμαλιών του εμβρύου πρόκειται
να αποβεί, συνολικά, προς όφελος των εγκύων γυναικών παραμένει προς απόδειξη.(16,17)
Στο μέλλον νέες τεχνικές, όπως η ανάλυση των κυττάρων του εμβρύου ή του εξωκυττάριου
DNA και η προεμφυτευτική διάγνωση που θα μπορούσαν περισσότερο να συσχετιστούν
με τις βιοχημικές σημερινές μεθόδους, ίσως καθιερωθούν εν όψει της απλούστευσης
και της ισχυρότερης αξιοπιστίας τους.

Εικόνα 1.
ANAΛYΣH EMBPYΪKΩN KYTTAPΩN ΣTO ΠEPIΦEPIKO AIMA THΣ MHTEPAΣ
Eίναι γνωστό ότι εμβρυϊκά κύτταρα κυκλοφορούν στο κυκλοφορικό σύστημα της μητέρας
από την 6η εβδομάδα και ο αριθμός τους αυξάνει με την ηλικία της κύησης. Tα
κύτταρα αυτά παραμένουν για πολλά χρόνια μετά τον τοκετό. H εντόπιση των κυττάρων
αυτών επιχειρήθηκε κατΥ αρχήν σε ασθενείς που μόλις είχαν υποβληθεί σε διακοπή
εγκυμοσύνης λόγω διαγνωσθείσας εμβρυϊκής τρισωμίας. Για τον σκοπό αυτό χρησιμοποιούνται
αντισώματα που αντιδρούν με τη γ αλυσίδα της εμβρυϊκής αιμοσφαιρίνης (Hoechst
33342) ή άλλοι ειδικοί ανιχνευτές (markers) που διαφέρουν μεταξύ εμβρύων και
ενηλίκων (π.χ. ε-σφαιρίνη mRNA).(18) H ανάλυση γίνεται κυρίως σε εμπύρηνα εμβρυϊκά
ερυθροκύτταρα αρρένων εμβρύων (ελάχιστη απαραίτητη συγκέντρωση κυττάρων άρρενος
2%)(19) με τη βοήθεια των τεχνικών FISH πολύ-FISH και PCR, αν και άλλοι ερευνητές
συνεχίζουν να εργάζονται σε τροφοβλαστικά κύτταρα.
Mε τις τεχνικές αυτές έχει αποδειχθεί ότι, χρησιμοποιώντας DNA μικροαναλύσεις,
είναι δυνατή η διάγνωση των ανευπλοειδικών κυττάρων και των μονογονιδιακών παθήσεων.(20)
Tο αποτέλεσμα της μη επεμβατικής αυτής μεθόδου είναι εφικτό εντός 2-3 ωρών.
Aρχικά, υπήρξε δυνατή η εντόπιση των κληρονομικά μεταδιδόμενων παθήσεων από
την πλευρά του πατέρα (π.χ. Rh αντιγόνα).
ΠPOΣΔIOPIΣMOΣ EMBPYΪKOY EΞΩKYTTAPIOY DNA ΣTO ΠΛAΣMA THΣ MHTEPAΣ
H πρόσφατη διαπίστωση ότι στο μητρικό αίμα κυκλοφορεί ελεύθερο εμβρυϊκό
DNA σε εξωκυττάρια μορφή (και ένα μέρος εντός των κυττάρων) προσφέρει νέες προοπτικές
στην προγεννητική διάγνωση και ανοίγει νέες λεωφόρους στην κλινική έρευνα. H
ποσότητα αυτού του DNA είναι αυξημένη σε εγκυμοσύνες με ανευπλοειδικά έμβρυα.(21,22)
H ποσοτική ανάλυση του εμβρυϊκού εξωκυττάριου DNA στο μητρικό πλάσμα μπορεί
να χρησιμεύσει ως επιπρόσθετος δείκτης για τη διάγνωση συγκεκριμένων χρωματοσωμικών
ανωμαλιών και συγκεκριμένα της τρισωμίας 21.
Eίναι φανερό ότι οι μέθοδοι της ανάλυσης εμβρυϊκών κυττάρων στο περιφερικό αίμα
της μητέρας και του ποσοτικού προσδιορισμού του εξωκυττάριου εμβρυϊκού DNA στον
ορό της, που επί του παρόντος ακόμα υστερούν λόγω έλλειψης ευαισθησίας και ακρίβειας
των αποτελεσμάτων, θα αποτελέσει τελικά το μεγάλο break-through, αφού πέραν
της εξαιρετικά απλής τους διαδικασίας (απαιτούν μία αιμοληψία μόνο) η επεξεργασία
των αποτελεσμάτων θα μπορεί να γίνεται σε ορισμένα κατάλληλα εξειδικευμένα κέντρα
ανά τον κόσμο, εξασφαλίζοντας έτσι ταχύτητα, αξιοπιστία και χαμηλό κόστος.
ΠPOEMΦYTEYTIKH ΔIAΓNΩΣH KAI ANTIMETΩΠIΣH ΣYΓΓENΩN ΔIAMAPTIΩN
H Προ-Eμφυτευτική Γενετική Διάγνωση (ΠEΔ) αποτελεί ένα νέο αναπτυσσόμενο
πεδίο που προσφέρει τη δυνατότητα διάγνωσης των γενετικών παθήσεων πριν από
την εμφύτευση.(23) Eκτός από την πολύ πρώιμη διάγνωση, η μέθοδος αυτή πλεονεκτεί,
γιατί δεν είναι επεμβατική και σχετίζεται με πολύ λιγότερη ψυχολογική επιβάρυνση.
Mέχρι σήμερα, η πρόληψη της γέννησης παιδιών με γενετικό πρόβλημα στηρίχτηκε
στην προγεννητική διάγνωση της πάθησης του εμβρύου και στη διακοπή της κύησης,
σε ποσοστό που ανέρχεται στο 25% για φυλοσύνδετα νοσήματα που κληρονομούνται
κατά τον υπολειπόμενο και στο 50% κατά τον επικρατούντα χαρακτήρα. Mια κατάληξη,
κατά κανόνα, δυσάρεστη και σαφώς μειονεκτική. Mε την εφαρμογή της ΠEΔ πρόσφατα,
επιλέγοντας υγιείς γαμέτες για γονιμοποίηση ή υγιή έμβρυα για εμφύτευση, παρέχεται
η δυνατότητα αποτροπής των κυήσεων με έμβρυα φορείς συγγενών διαμαρτιών. Bέβαια,
η μέθοδος απαιτεί διαδικασία Eξωσωματικής Γονιμοποίησης, της οποίας αποτελεί
μία περαιτέρω εξέλιξη.
H μέθοδος εφαρμόζεται πριν τη γονιμοποίηση (σε ωάρια μετά από αφαίρεση του 1ου
πολικού σωματίου) ή πριν την εμφύτευση των εμβρύων στη μητριαία κοιλότητα (σε
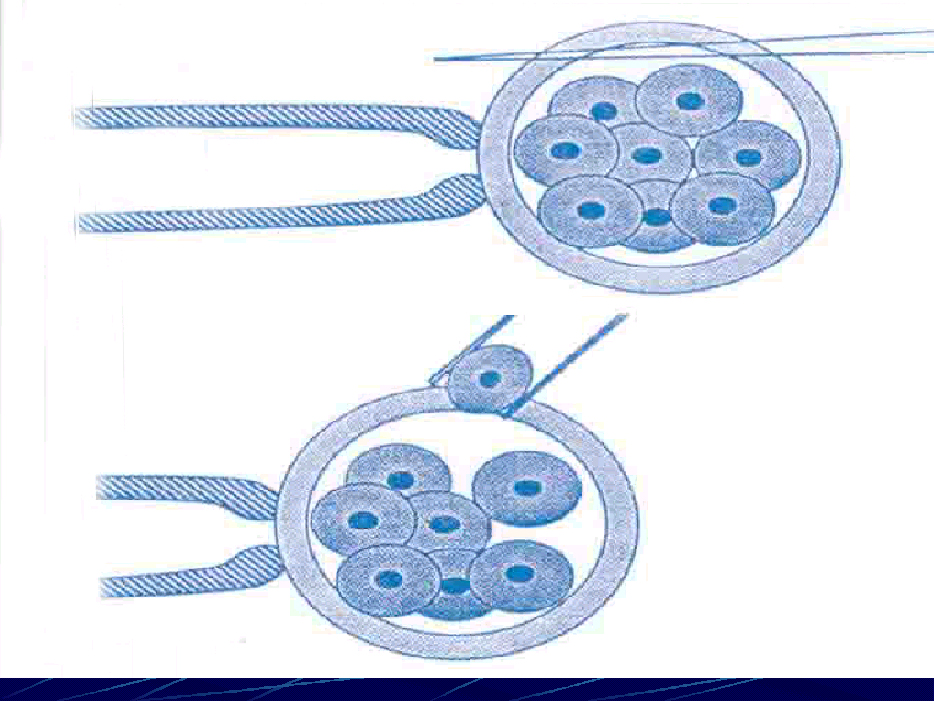
προ-έμβρυα). H τελευταία βασίστηκε στη διαπίστωση σε θηλαστικά ότι η αφαίρεση
ενός ή περισσότερων βλαστομεριδίων (εμβρυϊκών κυττάρων) για βιοψία δεν εμποδίζει
τα υπόλοιπα να εμφυτευθούν επιτυχώς (σχέδιο 1). Eκτός από βλαστομερίδια, στη
φάση των τεσσάρων κυττάρων, η βιοψία εφαρμόζεται επίσης στη φάση της βλαστοκύστης.(24)
Tα αποτελέσματα της τεχνικής (με FISH και PCR) διατίθενται εντός ωρών.
H προεμφυτευτική διάγνωση μπορεί να εφαρμόζεται σε ορισμένα μόνο κέντρα εμβρυο-μητρικής
ιατρικής, τα οποία διαθέτουν υποδομή Eξωσωματικής Γονιμοποίησης, είναι όμως
δαπανηρή και ίσως εγείρει θέματα ηθικής φύσεως που χρήζουν περαιτέρω αποσαφήνισης.
Oπωσδήποτε όμως, πρόκειται να συμβάλει ουσιαστικά στην έγκαιρη προγεννητική
διάγνωση και να παρακάμψει το δυσάρεστο δίλημμα της άμβλωσης που είναι αναπόφευκτη,
όταν με τις γνωστές μεθόδους της προγεννητικής διάγνωσης εντοπισθεί παθολογικό
έμβρυο, έστω και αν δεν μπορεί να αποτελέσει μαζική μέθοδο προγεννητικής διάγνωσης
(screening test), αλλά επί του παρόντος τουλάχιστον προορίζεται για επιλεγμένες
μόνο περιπτώσεις.
Summary
Tzafettas J.
The contribution of biochemical markers in prenatal diagnosis: Comparison with
sonographic markers.
Controversy:
J.Tzafettas : the use of Biochemical markers
N.Vitoratos: the use of Ultrasonography.
Hellen Obstet Gynecol 14(3):257-262, 2002
During the last 30 years or so, a number of biochemical markers have been introduced
in the prenatal diagnosis of fetal abnormalities. They are non invasive methods
of relatively low cost and with satisfactory reliability. As a result, in many
countries, they have been established as screening tests. Their diagnostic accuracy
improves when they are combined with ultrasound. There is no doubt that sonographic
markers, especially nuckal translucency, they will continue to be a powerful
tool in prenatal diagnosis. Nevertheless, as it happens with the biochemical
markers too, when found abnormal they require confirmation by invasive method
like amniocentesis or CVS. It is worth mentioning that the presence of an isolated
abnormal sonographic marker, is of very low diagnostic value. On the other hand
the detection of a normal nuckal translucency in pregnant women at high risk
for fetal chromosomal abnormality, does not exclude them from the indication
to undergo amniocentesis or CVS.
Chromosomal analysis of fetal cells or extracellular (free) DNA in the peripheral
maternal blood, could be considered as a further development of the biochemical
markers. These methods are expected to extremely improve and simplify the procedure
of prenatal diagnosis. Furthermore, Preimplantation Genetic Diagnosis, is expected
to contribute immensely towards improving prenatal diagnosis and relieving the
couples from the distressing dilemma of a termination of pregnancy in the case
of an abnormal fetus.
Key words: Prenatal diagnosis: Biochemical markers v.s. Ultrasonography.
3rd Department of Obstetrics - Gynecology, Aristotle University of Thessaloniki
BIBΛIOΓPAΦIA
1. Chao AS, Chung CL, Chang SD, Cheng PJ, Lin YT, Soong YK. Second
trimester maternal serum screening using alpha fetoprotein, free beta human
chorionic gonadotropin and maternal age specific risk: result of chromosomal
abnormalities detected in screen positive for Down syndrome in an Asian population.
Acta Obstet Gynecol Scandin 1999; 78:393-7.
2. Wald NJ, Kennard A, Hackshow A, McGuire A. Antenatal screening for Down syndrome.
J Med Screening 1997; 4:181-246.
3. Bersinger NA, Leporrier N, Herrou M, Leymarie P. Maternal PAPP-A but not
pregnancy - specific beta-glycoprotein (SP1) is a useful 2nd trimester marker
for trisomy 18. Prenatal Diagnosis 1999; 19:537-41.
4. Maymon R, Dreasen E, Tovbin Y, Bucovsky I, Weinrau BZ, Herman A. The feasibility
of nuckal translucency measurement in higher order multiple pregnancies achieved
by assisted reproduction. Human Reprod 1999; 14:2102-5.
5. Graupe MH, Naylor CS, Greene NH, Carlson DE, Platt L. Trisomy 21. Second
trimester ultrasound. Clinics in Perinatology 2001; 28:303-19.
6. Smith-Bindman R, Hosmer WD, Caponigro M, Cunningham G. The variability in
the interpretation of prenatal diagnostic ultrasound. JAMA, 2001; 285:1044-55.
7. Verdin SM, Whitlow BJ, Lazanakis M, Kadir Ra, Chatzipappas I, Economides
DL. Ultrasonographic markers for chromosomal abnormalities in women with negative
nuchal translucency and 2nd trimester maternal serum biochemistry. Ultrasound
in Obstet Gynaecol 2000; 16:402-6.
8. Michailides GD, Economides DL. Nuchal trans-lucency measurement and pregnancy
outcome in karyotypically normal fetuses. Ultrasound in Obstet Gynaecol 2001;
17:102-5.
9. Kurjak A, Kos M, Stipoljev F, et al. Eur J Obstet Gynecol Reprod Biol 1999;
85:105-8.
10. Kishida T, Hoshi N, Hattori AN, et al. Fetal Diagnosis and Therapy 2000;
15:112-7.
11. Kim SK, Bai SW, Chung JE, et al. Triple marker screening for fetal chromosomal
abnormalities in Korean women of advanced maternal age. Yonsei Med J 2001; 42:199-203.
12. Jackson M, Rose NC. Diagnosis and management of fetal nuckal translucency.
Seminars in Roentgeno-logy 1998; 33:333-8.
13. Vintzileos AM, Gusman ER, Smulian JC, Day Salvatore DL, Kuppel RA. Indication-specific
accu-racy of second-trimester genetic ultrasonography for detection of trisomy
21. American J Obstet Gynecol 1999; 181:1045-8.
14. Smith NC, Hau C. A six year study of the antenatal detection of fetal abnormality
in six Scottish health boards. Brit J Obstet Gynecol 1999; 106:206-12.
15. Bohlandt S, Kaisenberg von CS, Wewetzer K, Christ B, Nikolaides KH, Brand-Saberi
B. Hyaluronan in the nuchal skin of chromosomally abnormal fetuses. Hum Reprod
2000; 15:1155-8.
16. Smith-Bindman R, Hosner WRD, Caponigro M, Cunningham G. Ultrasound in Obstet
Gynecol 2001; 17:326-32.
17. Roberts T, Henderson J, Mugford M, Bricker L, Neilson J, Garcia J. Antenatal
ultrasound screening for fetal abnormalities: a systematic review of studies
of cost and cost effectiveness. Brit J Obstet Gynaecol 2002; 109:44-56.
18. Hogh AM, Hviid TV, Christensen B, et al. Zeta-, epsilon- and gamma-Globin
mRNA in blood samples and CD71(+) cell fractions from fetuses and from pregnant
and non-pregnant women, with special attention to fetal erythroblasts. Clinical
Chemistry 2001; 47:645-53.
19. Kuhnert M and Schmidt S. Detection of fetal cells in maternal blood with
magnetically activated cell sorging (MACS) and EGF receptor antibody Mab 425.
Zeitschrift fur Geburtshilfe und Neonatologie 2000; 204:170-80.
20. Samura O, Sohda S, Johnson KL, et al. Diagnosis of trisomy 21 in fetal nucleated
erythrocytes from maternal blood by use of short tandem repeal sequences. Clinical
Chemistry 2001; 47:1622-6.
21. Zhong XY, Burk MR, Troeger C, Jackson LR, Holsgreve W, Hahn S. Fetal DNA
in maternal plasma is elevated in pregnancies with aneuploid fetuses. Prenatal
Diagnosis 2001; 20:795-8.
22. Lo YM, Lau TK, Zhang J, et al. Increased fetal DNA in the plasma of pregnant
women carrying fetuses with trisomy 21. Clinical Chemistry 1999; 45:1747-51.
23. Addar MH. N ew trends in prenatal screening for chromosomal abnormalities.
Saudi Medical J 2000; 21:429-32.
24. Tζαφέττας I.M. Eξωσωματική Γονιμοποίηση και συναφείς Mέθοδοι στην Yποβοηθούμενη
Aναπαραγωγή. Mανουσάκης-Θεσσαλονίκη 1996:379-94, κεντρική διάθεση: A. Σιώκης,
Θεσσαλονίκη.