Τοξική ηπατίτιδα μετά
από διαδοχική χορήγηση φλουταμίδης
και οξικής κυπροτερόνης
Η θέση του ουρσοδεοξυχολικού οξέος
Σ.
ΜΑΝΩΛΑΚΟΠΟΥΛΟΣ[1], Σ. ΜΠΕΘΑΝΗΣ[1], Α. ΑΡΜΟΝΗΣ[1],
Ε. ΑΝΔΡΙΚΟΠΟΥΛΟΣ[1], A. ΑΥΓΕΡΙΝΟΣ[2], Δ. ΤΖΟΥΡΜΑΚΛΙΩΤΗΣ[1]
[1] Γαστρεντερολογικό Τμήμα ΓΝΑ "Πολυκλινική",
[2] Β΄ Γαστρεντερολογική Κλινική ΓΝΑ "Ο Ευαγγελισμός"
Η φλουταμίδη και η οξική
κυπροτερόνη αποτελούν εκπροσώπους δύο διαφορετικών τάξεων αντιανδρογόνων: των
επονομαζόμενων αμιγών, μη στεροειδικών, αντιανδρογόνων και των στεροειδικών
αντιανδρογόνων αντίστοιχα, που χρησιμοποιούνται ευρύτατα στην καθημερινή κλινική
πράξη στην αντιμετώπιση του καρκίνου του προστάτη. Τόσο η φλουταμίδη, όσο και
η οξική κυπροτερόνη, έχουν ενοχοποιηθεί για ένα μεγάλο εύρος τοξικών επιδράσεων
στο ήπαρ [5-16].
Ο ι αντίστοιχες κλινικές
εκδηλώσεις κυμαίνονται από την ανορεξία, το αίσθημα ναυτίας και τον ασυμπτωματικό
ίκτερο, μέχρι τα συμπτώματα και τα σημεία της κεραυνοβόλου ηπατικής νέκρωσης.
Τα εργαστηριακά ευρήματα επίσης καταλαμβάνουν ένα μεγάλο εύρος εκδηλώσεων, από
την ήπια ανύψωση των τρανσαμινασών, ως τα βιοχημικά χαρακτηριστικά του χολοστατικού
ικτέρου, της ηπατικής νέκρωσης ή ακόμα και της ηπατικής ανεπάρκειας.
Η περίπτωση που περιγράφεται στη συνέχεια είναι η πρώτη, σύμφωνα με τη γνώμη
των συγγραφέων, αναφορά, αφενός τοξικής ηπατίτιδας μετά από διαδοχική ηπατοτοξική
δράση τόσο ενός στεροειδικού όσο και ενός μη στεροειδικού αντιανδρογόνου, και
αφετέρου η πρώτη αναφορά επιτυχούς αντιμετώπισής της. Πρόκειται για έναν ασθενή
που εμφάνισε ηπατίτιδα συνοδευόμενη από ίκτερο μετά τη χορήγηση αρχικά φλουταμίδης
και στη συνέχεια οξικής κυπροτερόνης. Η χορήγηση ουρσοδεοξυχολικού οξέος ξεκίνησε
αμέσως μετά την εισαγωγή του ασθενούς στην κλινική μας, παράλληλα με τη διακοπή
λήψης της ενεχόμενης ουσίας (οξική κυπροτερόνη). Σημειώθηκε σημαντική κλινική
βελτίωση του ασθενούς, με σαφή και ταχεία βελτίωση των βιοχημικών του δεικτών,
ήδη μετά τις τρεις πρώτες εβδομάδες της θεραπείας.
Περιγραφή της
περίπτωσης
Πρόκειται για έναν άνδρα ηλικίας 76 ετών, ο οποίος προσήλθε στις 9/2/2002 στην
κλινική μας προς διερεύνηση - αντιμετώπιση ικτερικού επεισοδίου, χρονολογουμένου
από μηνός προ της εισαγωγής του.
Το κληρονομικό ιστορικό του ασθενούς ήταν ελεύθερο για την ύπαρξη ηπατικού νοσήματος.
Από το ατομικό αναμνηστικό του ασθενούς δεν αναφέρονται μεταγγίσεις αίματος,
χρήση ναρκωτικών ουσιών, υπερβολική κατανάλωση αλκοόλ, έκθεση σε τοξικές ουσίες,
ενασχόληση με τον ιατρικό - παραϊατρικό χώρο, ενώ ο ασθενής δεν είχε υποβληθεί
σε δερματοστιξία.
Ο ασθενής είχε υποβληθεί σε σκωληκοειδεκτομή προ πεντηκονταετίας, σε χειρουργική
θεραπεία τριχοφωλεακού συριγγίου προ τριακονταετίας και σε νευροχειρουργική
επέμβαση αποκατάστασης δύο εγκεφαλικών ανευρυσμάτων προ εξαετίας, τα οποία ανακαλύφθηκαν
μετά από πτώση του ασθενούς.
Ο ασθενής λαμβάνει από πενταετίας ένα β-αδρενεργικό αποκλειστή, την ατενολόλη
(Neocardon, Gap) στη δοσολογία των 50mg μία φορά την ημέρα, λόγω ήπιας υπέρτασης.
Δεκαπέντε μήνες πριν από την εισαγωγή του στην κλινική μας, ο ασθενής είχε υποβληθεί
σε διουρηθρική εκτομή του προστάτη λόγω αδενοκαρκινώματος. Η ηπατική λειτουργία
του ασθενούς την περίοδο αυτή της ουρολογικής επεμβάσεως, ήταν μέσα στα φυσιολογικά
όρια.
Ένα μήνα περίπου μετά την επέμβαση, ο ασθενής ξεκίνησε τη λήψη φλουταμίδης (Flucinom,
Schering AG) σε δόση 250mg δύο φορές την ημέρα και ενός αναλόγου της LHRH, της
οξικής λευπρορελίδης (Elityran, Vianex), με χορήγηση μίας ενδομυικής ένεσης
των 3,75mg μία φορά κάθε τριάντα ημέρες. Έξι μήνες μετά την έναρξη της αγωγής
με φλουταμίδη, ο ασθενής νοσηλεύθηκε λόγω ικτερικού επεισοδίου σε νοσοκομείο
της Αθήνας. Τα εργαστηριακά ευρήματα του ασθενούς εκείνη την περίοδο ήταν τα
εξής (εντός παρενθέσεως αναφέρονται οι φυσιολογικές τιμές): τρανφεράση της αλανίνης
164IU/l (5-40), ασπαρτική τρανσφεράση 260IU/l (5-40), ολική χολερυθρίνη 23,6mg/dl
(0,1-1,3), άμεση χολερυθρίνη 17,7mg/dl (<0,4), αλκαλική φωσφατάση 132IU/l
(98-279) και γάμμα-γλουταμυλοτρανσπεπτιδάση 170IU/l (9-61).
Ο ασθενής υπεβλήθη κατά την τότε νοσηλεία του σε υπολογιστική τομογραφία άνω
και κάτω κοιλίας και σε ανάστροφη ενδοσκοπική χολαγγειοπαγκρεατογραφία, που
δεν ανέδειξαν παθολογικά ευρήματα. Το ικτερικό επεισόδιο θεωρήθηκε φαρμακευτικής
αιτιολογίας και διεκόπη η χορήγηση φλουταμίδης. Συνεστήθη η τροποποίηση της
φαρμακευτικής αγωγής με τη λήψη οξικής κυπροτερόνης (Androcur, Schering AG)
σε δόση 50mg τρεις φορές την ημέρα και συνέχιση της αγωγής με οξική λευπρορελίδη
και ατενολόλη, όπως και πριν από τη νοσηλεία του ασθενούς. Εδόθησαν επίσης οδηγίες
στον ασθενή για τακτική μέτρηση των τιμών της ολικής χολερυθρίνης.
Στο σχήμα 1 φαίνεται η πορεία των τιμών της ολικής και άμεσης χολερυθρίνης του
ασθενούς μετά τη διακοπή της λήψης φλουταμίδης και υπό τη χορήγηση οξικής κυπροτερόνης,
μέχρι την εισαγωγή του στην κλινικής μας προς διερεύνηση νέου ικτερικού επεισοδίου.
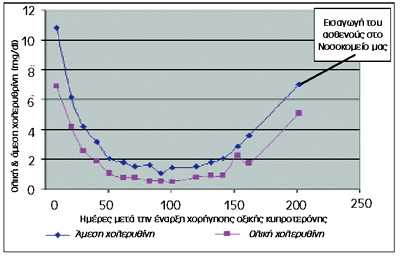
Σχήμα 1. Τιμές ολικής & άμεσης χολερυθρίνης υπό τη χορήγηση οξικής κυπροτερόνης
(διακοπή φλουταμίδης).
Από την αντικειμενική εξέταση
του ασθενούς κατά την εισαγωγή του στην κλινική μας, σημειώθηκε ικτερική χροιά
δέρματος και σκληρών, καθώς και ηπατομεγαλία. Δεν υπήρχε πυρετός, απώλεια βάρους,
ούτε αραχνοειδείς τηλεαγγειεκτασίες, παλαμιαίο ερύθημα ή σπληνομεγαλία. Ο ασθενής
ανέφερε αίσθημα κνησμού ήπιας εντάσεως.
Από τον εργαστηριακό έλεγχο προέκυψε φυσιολογική γενική εξέταση αίματος (WBC
8.67K/μl, RBC 3.53M/μl, Hgb 12.2g/dl, Hct 36.2%, PLT 166K/μl), ενώ οι ακραίες
τιμές των βιοχημικών παραμέτρων του ασθενούς σημειώθηκαν τη δεύτερη ημέρα εισαγωγής
του και ήταν οι ακόλουθες: ALT 162IU/l, AST 265IU/l, TBIL 6,8mg/dl, DBIL 4,88mg/dl,
γ-GT 118IU/l και ALP 302IU/l.Ο χρόνος προθρομβίνης του ασθενούς ήταν 15.3sec
(χρόνος μάρτυρα 10.7sec). Η ηλεκτροφόρηση των λευκωμάτων του ασθενούς έδωσε
τα παρακάτω αποτελέσματα: αλβουμίνη 48% (52-68), α-1 σφαιρίνες 3,4% (2-5), α-2
σφαιρίνες 6,7% (6,6-13,5), β-σφαιρίνες 14% (8,5-14,5) και γ-σφαιρίνες 27,9%
(11-21).
Ο έλεγχος για ηπατίτιδα Α, Β, C ήταν αρνητικός, όπως και ο έλεγχος για πρόσφατες
λοιμώξεις από κυτταρομεγαλοϊό, ιό Epstein-Barr και τους ιούς του απλού έρπητα.
Δεν ανευρέθησαν αντιπυρηνικά, αντιμιτοχονδριακά ή αντισώματα έναντι των λείων
μυικών ινών.
Σε γενόμενο υπερηχογραφικό έλεγχο παρατηρήθηκε αυξημένη ηχογένεια του ήπατος,
πολλαπλή χολολιθιασική σκίαση με φυσιολογικό εύρος του χοληδόχου πόρου, ενώ
η ηχογένεια νεφρών, σπληνός και παγκρέατος ήταν φυσιολογική.
Ο ασθενής υποβλήθηκε και σε υπολογιστική τομογραφία άνω και κάτω κοιλίας όπου
δεν παρατηρήθηκε εικόνα εστιακής βλάβης εντός του ήπατος, ούτε διάταση των ενδοηπατικών
χοληφόρων, ενώ ο υπόλοιπος έλεγχος της άνω και κάτω κοιλίας ήταν αρνητικός για
παθολογικά ευρήματα, πλην μιας σχετικά ευμεγέθους διαφραγματοκήλης. Επίσης,
πραγματοποιήθηκε έγχρωμο υπερηχογράφημα triplex σπληνοπυλαίου άξονα, χωρίς παθολογικά
ευρήματα.
Δεν πραγματοποιήθηκε βιοψία ήπατος λόγω άρνησης του ασθενούς.
Λόγω της υποψίας της φαρμακευτικής ηπατίτιδας, διεκόπη η χορήγηση οξικής κυπροτερόνης
κατά την εισαγωγή του ασθενούς. Ετέθη αγωγή με ουρσοδεoξυχολικό οξύ (Ursofalk,
Galenica), στη δοσολογία των 250 mg ανά δωδεκάωρο. Το υπόλοιπο διάστημα της
νοσηλείας του, τόσο η γενική κατάστασή του, όσο και οι βιοχημικές του παράμετροι
βελτιώθηκαν, με αποτέλεσμα την έξοδό του ένδεκα ημέρες μετά την εισαγωγή του.
Οι βιοχημικοί δείκτες κατά την έξοδό του ήταν οι εξής: ALT 124IU/l, AST 69IU/l,
TBIL 2,97mg/dl, DBIL 2,43mg/dl, γ-GT 89IU/l και ALP 239IU/l, ενώ υπήρχε σαφής
βελτίωση του ικτέρου και του κνησμού.
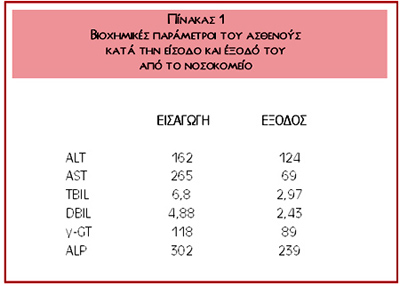
Στον πίνακα 1 καταγράφονται οι βιοχημικές παράμετροι του ασθενούς κατά την προσέλευσή
του στο νοσοκομείο μας και κατά την έξοδό του.
Μετά την έξοδό του, ο ασθενής παρακολουθείται σε εξωτερική βάση στο Ηπατολογικό
Ιατρείο του νοσοκομείου μας και περίπου δύο χρόνια μετά, βρίσκεται σε πολύ καλή
γενική κατάσταση, με φυσιολογικούς όλους τους ηπατικούς βιοχημικούς δείκτες
(σχήμα 2).

Σχήμα 2. Εξέλιξη των ηπατικών
βιοχημικών δεικτών του ασθενούς μετά την εισαγωγή του.
Συζήτηση
Η ηπατοκυτταρικού τύπου ηπατική βλάβη που περιγράφηκε προηγουμένως, πιθανότατα
προκλήθηκε αρχικά από τη χορήγηση φλουταμίδης και στη συνέχεια, μετά τη διακοπή
της φλουταμίδης, από τη χορήγηση οξικής κυπροτερόνης.
Υπήρχε μια σαφής χρονική συσχέτιση μεταξύ της έναρξης της λήψης των ενεχομένων
ουσιών και της εγκατάστασης της ηπατικής βλάβης. Το χρονικό διάστημα των 180
περίπου ημερών από την έναρξη της θεραπείας με φλουταμίδη και της διαπίστωσης
της ηπατοτοξικής της δράσης, συμπίπτει με τα αποτελέσματα που έχουν ανακοινώσει
και άλλοι ερευνητές στο παρελθόν (π.χ. Wysowski et al: χρονική απόσταση από
5-270 ημέρες μεταξύ της εκκίνησης της λήψης φλουταμίδης και της ηπατοτοξικής
της δράσης [7]). Επίσης, οι 150 κατά προσέγγιση ημέρες που μεσολάβησαν από την
έναρξη χορήγησης της οξικής κυπροτερόνης και της πρόκλησης της τοξικής ηπατίτιδας,
συμπίπτουν με τα αποτελέσματα προηγουμένων μελετών (π.χ. σύμφωνα με τον Friedman
και τους συνεργάτες του, το αντίστοιχο χρονικό διάστημα είναι 2-15 μήνες [16]).
Ο ασθενής δεν είχε ιστορικό ηπατικού νοσήματος ή νοσήματος των χοληφόρων, ενώ
με τον κατάλληλο έλεγχο αποκλείστηκαν όλες οι άλλες πιθανές αιτίες οξείας ηπατίτιδας.
Η ατενολόλη, όπως και η οξική λευπρορελίδη (ανάλογο της LHRH), που συγχορηγήθηκαν
στον ασθενή τόσο με τη φλουταμίδη όσο και με την οξική κυπροτερόνη, δεν χαρακτηρίζονται
από ανεπιθύμητες εκδηλώσεις από το ήπαρ [1-4], ενώ η ανάρρωση του ασθενούς επιτεύχθηκε
χωρίς καμία μεταβολή της αγωγής του με τις προαναφερθείσες ουσίες.
Υπό το φως αυτών των δεδομένων, φαίνεται πιθανότατη η αιτιολογική συσχέτιση
της τοξικής ηπατίτιδας που εμφάνισε ο ασθενής με τη χορήγηση αρχικά φλουταμίδης
και στη συνέχεια οξικής κυπροτερόνης, αλλά από τη στιγμή που για λόγους ηθικής
δεοντολογίας δεν δοκιμάστηκε η επαναχορήγηση των ενεχομένων ουσιών μετά τη βελτίωση
του ασθενούς, δεν έχουμε δικαίωμα να κάνουμε λόγο για απόδειξη της σύνδεσης
μεταξύ των προαναφερθεισών ουσιών και της τοξικής βλάβης του ήπατος. Στην κλινική
πράξη όμως, η διάγνωση της φαρμακευτικής ηπατοπάθειας συνήθως βασίζεται στον
αποκλεισμό άλλων αιτιών ηπατικής δυσλειτουργίας και στη χρονική συσχέτιση μεταξύ
της έναρξης της χορήγησης του φαρμάκου και της διάγνωσης της ηπατικής βλάβης.
Η φλουταμίδη και η οξική κυπροτερόνη αποτελούν εκπροσώπους των δύο διαφορετικών
κατηγοριών αντιανδρογόνων που υπάρχουν στις ημέρες μας. Η μεν φλουταμίδη υπάγεται
στα ονομαζόμενα αμιγή, μη στεροειδικά αντιανδρογόνα, ενώ η οξική κυπροτερόνη
στα στεροειδικά ανδρογόνα.
Όσον αφορά τη φλουταμίδη, έχουν περιγραφεί στο παρελθόν διάφορες ηπατοτοξικές
δράσεις του φαρμάκου. Σύμφωνα με τον Gomez και τους συνεργάτες του[6], η φλουταμίδη
έχει ενοχοποιηθεί για ασυμπτωματική αύξηση των τρανσαμινασών σε ποσοστό 0,36%,
ενώ μόνο 0,18% του δείγματος των 1.091 ασθενών που εξετάστηκαν (δηλαδή μόνο
2 ασθενείς) εμφάνισαν κλινικές εκδηλώσεις ηπατικής νόσου.
Σύμφωνα με άλλες μελέτες, το ποσοστό της τοξικής ηπατίτιδας μετά από χορήγηση
φλουταμίδης ανέρχεται από 1-5% [7,8]. Στις ΗΠΑ, μόνο τα πρώτα πέντε χρόνια κυκλοφορίας
του φαρμάκου αναφέρθηκαν 20 περιπτώσεις θανατηφόρου ηπατοτοξικής δράσης της
φλουταμίδης [7], για να ακολουθήσουν και άλλες καταγραφές περιπτώσεων ηπατικής
ανεπάρκειας με θανατηφόρα έκβαση μετά τη χορήγηση φλουταμίδης [8-10].
Η οξική κυπροτερόνη έχει υπερβεί τις δύο δεκαετίες χρησιμοποίησής της. Είναι
ένα γενικά καλώς ανεκτό φάρμακο, υπάρχουν όμως στη βιβλιογραφία συγκεκριμένες
αναφορές ηπατοτοξικής δράσης της, λιγότερες όμως σε συχνότητα και ηπιότερες
σε ένταση από αυτές της φλουταμίδης [11]. Το 1989 περιγράφτηκε για πρώτη φορά
η περίπτωση κεραυνοβόλου ηπατίτιδας που κατέληξε σε θάνατο [12], ενώ μέχρι σήμερα
έχουν περιγραφεί άλλες έξι περιπτώσεις θανατηφόρου ηπατίτιδας [13-16].
Η ηπατοτοξικότητα από τη λήψη οξικής κυπροτερόνης είναι αμελητέα σύμφωνα με
τον Hinkel και τους συνεργάτες του, όπως συμπέραναν μετά την αναδρομική μελέτη
89 ασθενών που λάμβαναν το συγκεκριμένο αντιανδρογόνο για χρονικό διάστημα μεγαλύτερο
των τεσσάρων ετών [11].
Ο μηχανισμός της τοξικής δράσης τόσο της φλουταμίδης, όσο και της οξικής κυπροτερόνης
στο ήπαρ, δεν έχει πλήρως αποσαφηνιστεί. Αν και η απευθείας ηπατοτοξική δράση
τόσο της φλουταμίδης όσο και της οξικής κυπροτερόνης δεν μπορεί να αποκλειστεί,
τα περισσότερα χαρακτηριστικά αυτής της ηπατοτοξικής δράσης οδηγούν στο συμπέρασμα
της ιδιοσυγκρασιακής αντίδρασης απέναντι στις ίδιες τις ουσίες ή κάποιους μεταβολίτες
τους [6-10,16,17]. Στην περίπτωση που περιγράψαμε δεν παρατηρήθηκε πυρετός,
εξάνθημα, αρθραλγίες και ηωσινοφιλία στο περιφερικό αίμα και συνεπώς η πιθανότητα
μεσολάβησης ανοσολογικού μηχανισμού είναι μικρή.
Από την αναδρομή που πραγματοποιήσαμε στη βιβλιογραφία προέκυψε πως η έγκαιρη
διάγνωση της ηπατικής βλάβης και η διακοπή της ενεχόμενης φαρμακευτικής ουσίας
αποτελούσαν τη μοναδική αποτελεσματική θεραπεία περιπτώσεων φαρμακευτικής ηπατίτιδας
ιδιοσυγκρασιακού τύπου. Υπήρχαν όμως πολλές αναφορές για την ευεργετική επίδραση
του ουρσοδεοξυχολικού οξέος, σε συνδυασμό με τη διακοπή της ενεχόμενης φαρμακευτικής
ουσίας, σε περιπτώσεις επιδείνωσης της ηπατικής λειτουργίας από λήψη φαρμακευτικής
αγωγής. Το ουρσοδεοξυχολικό οξύ είναι ένα μη τοξικό, υδρόφιλο χολικό οξύ, που
χρησιμοποιείται κυρίως σε χολοστατικού τύπου ηπατικές διαταραχές [18].
Πρώτος ο Kalliowski και οι συνεργάτες του το 1991 χρησιμοποίησαν με επιτυχία
το ουρσοδεοξυχολικό οξύ, σε περιπτώσεις ασθενών που εμφάνισαν φαρμακευτική ηπατίτιδα
χολοστατικού τύπου μετά από λήψη κυκλοσπορίνης [19]. Στη συνέχεια ακολούθησαν
και άλλες αναφορές ευεργετικών επιδράσεων του ουρσοδεοξυχολικού οξέος στην αντιμετώπιση
χολοστατικών συνδρόμων μετά από λήψη φαρμακευτικών ουσιών, όπως ο συνδυασμός
αμοξυκιλλίνης - κλαβουλανικού οξέος ή αναβολικών στεροειδών [21-25], όπως αναφέρεται
και η περίπτωση επιτυχούς αντιμετώπισης τοξικής ηπατίτιδας μετά από λήψη φλουταμίδης
[20] από την Cicognanni και τους συνεργάτες της.
Στην περίπτωση του ασθενούς που περιγράψαμε, η χορήγηση του ουρσοδεοξυχολικού
οξέος σχετίστηκε με τη βελτίωση της συμπτωματολογίας του ασθενούς (ύφεση ικτέρου
και κνησμού) και τη σημαντική βελτίωση της ηπατικής του βιοχημείας. Σύμφωνα
με τη γνώμη των συγγραφέων, αυτή είναι η πρώτη αναφορά στη διεθνή βιβλιογραφία
τοξικής ηπατίτιδας που προκλήθηκε από τη διαδοχική χορήγηση αρχικά φλουταμίδης
και στη συνέχεια οξικής κυπροτερόνης, εκπροσώπων δηλαδή των δύο διαφορετικών
τάξεων αντιανδρογόνων που χρησιμοποιούνται σήμερα. Η χορήγηση δε του ουρσοδεοξυχολικού
οξέος είχε ευεργετικά αποτελέσματα στην ηπατική βλάβη που προκλήθηκε από τη
χορήγηση των συγκεκριμένων αντιανδρογόνων.
Δεδομένων των δυνητικά θανατηφόρων ηπατοτοξικών επιδράσεων από τη χορήγηση αντιανδρογόνων,
η χορήγησή τους είναι επιβεβλημένο να συνοδεύεται από τακτική μέτρηση των ηπατικών
ενζύμων. Σε περίπτωση εμφάνισης ηπατικών διαταραχών, η διακοπή λήψης των ενεχόμενων
ουσιών και η χορήγηση ουρσοδεοξυχολικού οξέος φαίνεται, με τα μέχρι τώρα δεδομένα,
μια δοκιμασμένη και λογική επιλογή, αν και απαιτούνται παραπάνω στοιχεία για
την καθιέρωση του ουρσοδεοξυχολικού οξέος ως θεραπευτικού μέσου για την αντιμετώπιση
τοξικής ηπατίτιδας από χορήγηση αντιανδρογόνων.
Βιβλιογραφία
1. Ridell JG, Harron DW, Shanks RG. Clinical pharmakokinetics of beta - adrenoreceptor
antagonists. An update. Clin Pharmacokinet 1987 May; 12(5):305-20.
2.Borchard U. Pharmakokinetics of beta - adrenoreceptor blocking agents: clinical
significance of hepatic and / or renal clearance. Clin Phys Biochem 1990; 8(2):28-34.
3. Crawford ED, Eisenberger MA, Mc Leod DG et al. A controlled trial of leuprorelide
with and without flutamide in prostatic carcinoma. N Engl J Med 1989; 321:419-24.
4. Friedman A, Narcross MJ, Rein M. Adverse effects of leuprorelide acetate
depot treatment. Fertil Steril 1993; 59:448-450.
5. Migliari R, Muscas G, Murru M et al. Antiandrogens: a summary review of pharmacodynamic
properties and tolerability in prostate cancer therapy. Arch Ital Urol Androl
1999 Dec; 71(5):293-302.
6. Gomez JL, Dupont A, Cusan L et al. Incidence of liver toxicity associated
with the use of flutamide in prostate cancer patients. Is J Med 1992; 92:465-70.
7. Wysowski D, Freiman JP, Tourtelot JP et al. Fatal and nonfatal hepatotoxicity
associated with flutamide. Ann Intern Med 1992; 118:860-864.
8. Garcia Cortes M, Andrade RJ, Lucena MI et al. Flutamide - induced hepatotoxicity:
report of a case series. Rev ESP Enferm Dig 2001 July; 93(7):419-22.
9. Dourakis S, Alexopoulou A, Hadziyannis S. Fulminant hepatitis after flutamide
treatment. Journal of Hepatology 1994; 20:350-53.
10. Cetin M, Demirci D, Unal A et al. Frequency of flutamide induced hepatotoxicity
in patients with prostate carcinoma. Hum Exp Toxically 1999 Mar; 18(3):137-140.
11. Hinkel A, Berges RR, Pannek J et al. Cyproterone acetate in the treatment
of advanced prostatic cancer: retrospective analysis of liver toxicity in the
long - term follows up of 89 patients. Eur Urol 1996; 30(4):464-70.
12. Levesque H, Trivalle C, Manchon ND et al. Fulminant hepatitis due to cyproterone
acetate. Lancet 1989; I 215-16.
13. Parys BT, Hamid S, Thomson RGN. Severe hepatocellular dysfunction following
cyproterone acetate therapy. Br J Urol 1991; 67:312-13.
14. Hirsch D, Kovatz S, Bernheim J et al. Fatal fulminant hepatitis from cyproterone
acetate. Sir J Med Sci 1994; 30:238-242.
15. Bressolette L, Dubois A, Carlhant D et al. Fatal hepatitis caused by cyproterone
acetate. Therapie 1994; 49(2):153.
16. Friedman G, Lamoureux E, Sherker A. Fatal fulminant hepatic failure due
to cyproterone acetate. Dig Dis Sci Vol 44 No 7 Jul 1999; 1362-63.
17. Scheuer PJ. Liver biopsy interpretation. 4th ed Philadelphia. Baillie Tidal,
1988; 99-112.
18. Trauner M, Graziadei IW. Review article: mechanisms of action and therapeutic
applications of ursodeoxycholic acid in chronic liver diseases. Aliment Pharmacol
Ther 1999 Aug; 13(8):979-96.
19. Kallinowski B, Theilmann L, Zimmermann R et al. Effective treatment of cyclosporine
- induced cholostasis in heart - transplanted patients treated with ursodeoxycholic
acid. Transplantation 1991; 51:1.128-1.129.
20. Cicognani C, Malavolti M, Morselli - Labate A et al. Flutamide - induced
toxic hepatitis. Potential utility of ursodeoxycholic acid administration in
toxic hepatitis. Dig Dis Sci 1996 Nov; 41(11):2.219-2.221.
21. Soza A, Riquelme F, Alvarez M et al. Hepatotoxicity by amoxicillin / clavulanic
acid: case report. Rev ESP Enferm Dig 1998 Jul; 90(7):523-6.
22. Barrio J, Castiella A, Lobo C et al. Cholestatic acute hepatitis induced
by amoxycillin - clavulanic acid combination. Role of ursodeoxycholic acid in
drug - induced cholestasis. Rev ESP Enferm Dig 1998 Jul; 90(7):523-6.
23. Katsinelos P, Vasiliadis T, Xiarchos P et al. Ursodeoxycholic acid (UDCA)
for the treatment of amoxycillin - clavulanate potassium (Augmentin) - induced
intra - hepatic cholestasis: report of two cases. Eur J Gastroenterol Hepatol
2000 Mar; 12(3):365-8.
24. Habscheid W, Abele U, Dahm HH. Severe cholestasis with kidney failure from
anabolic steroids in a body builder. Dtsch Med Wochenschr 1999 Sep 10; 124(36):1.029-32.
25. Salmon L, Montet JC, Oddoze C et al. Ursodeoxycholic acid and prevention
of terrine - induced hepatotoxicity: a pilot study. Therapie 2001 Jan-Feb; 56(1):29-34.