
Oι επιπτώσεις του καπνίσματος
στο καρδιοαναπνευστικό σύστημα
ΒΡΥΩΝΗ ΙOΥΛΙΑ[1],
ΠΑΜΠOΥΚOΣ ΣΤΑΥΡOΣ[2]
[1]Πνευμονολόγος, Επιμ. Β', Πνευμονολογική Κλινική, Νοσοκομείο «Αμαλία Φλέμιγκ»
[2]Ειδικευόμενος Πνευμονολόγος, 6η Πνευμονολογική Κλινική ΝΝΘΑ
Από το 1964, όπου δημοσιεύθηκε
η πρώτη αναφορά των Surgeon General των ΗΠΑ πάνω στο θέμα «Κάπνισμα και Υγεία»,
το κάπνισμα τσιγάρων σταθερά αποδεικνύεται σημαντικός παράγοντας κινδύνου ανάπτυξης
αναπνευστικών και καρδιαγγειακών νόσων. Στο άρθρο αυτό ανακεφαλαιώνεται η εκτεταμένη
βιβλιογραφία που υπάρχει, πάνω στις δυσμενείς επιδράσεις του καπνίσματος στο
αναπνευστικό και στο καρδιαγγειακό σύστημα.
Παθολογοανατομικές
επιδράσεις του καπνίσματος στο αναπνευστικό σύστημα
1) Επίδραση στους αεραγωγούς
α) Στους μεγάλους αεραγωγούς προκαλεί
μέτρια αύξηση των τραχειοβρογχικών αδένων, αύξηση της βλεννώδους έκκρισης και
αύξηση του αριθμού των κυττάρων goblet. Οι αλλοιώσεις αυτές έχουν ως αποτέλεσμα
παραγωγικό βήχα και αύξηση της απόχρεμψης των καπνιστών.
β) Στους μικρούς αεραγωγούς (δ=2-3mm και μικρότερη) προκαλεί αρχικά φλεγμονή,
δημιουργία μικρών ελκών και πλακώδη μετάπλαση και στη συνέχεια αύξηση της μυϊκής
μάζας, στένωση των αεραγωγών και αύξηση των κυττάρων goblet.
2) Επίδραση στη βλεννοκροσσωτή
κάθαρση
Όπως είναι γνωστό, ο καπνός του τσιγάρου
προκαλεί δομικές και λειτουργικές ανωμαλίες στο βλεννοκροσσωτό σύστημα των αεραγωγών.
Βραχύχρονη έκθεση στον καπνό προκαλεί στάση των κροσσών in vitro, ενώ μακροχρόνια
έκθεση προκαλεί βλάβες στο επιθήλιο, υπερέκκριση βλέννης και δυσκινησία των
κροσσών. Η χρόνια βρογχίτις των καπνιστών και των πρώην καπνιστών χαρακτηρίζεται
από βλάβη της βλεννοκροσσωτής κάθαρσης. Τόσο η σωματιδιακή όσο και η αεριώδης
φάση του καπνού του τσιγάρου, είναι τοξική για τους κροσσούς.
3) Επίδραση στο πνευμονικό
παρέγχυμα
Ανευρίσκεται αυξημένος αριθμός φλεγμονωδών
κυττάρων (μακροφάγων, ουδετεροφίλων) στους πνεύμονες των καπνιστών, με αποτέλεσμα
απελευθέρωση ελαστάσης.
4) Επίδραση στα πνευμονικά
αγγεία
Δεν είναι ξεκάθαρο αν οι αλλαγές που
παρατηρούνται στα αγγεία των καπνιστών είναι πρωτοπαθείς ή δευτεροπαθείς λόγω
της υποξίας.
α) Ελαστικά αγγεία: αν και είναι λογικό στις μεγάλες ελαστικές αρτηρίες να βρίσκουμε
αθηρώματα (αφού το κάπνισμα είναι παράγοντας αθηρογένεσης), δεν υπάρχουν επαρκή
παθολογοανατομικά ευρήματα που να δείχνουν συσχέτιση.
β) Μυϊκά αγγεία: πολλές μελέτες έχουν ασχοληθεί με τις μυϊκές αρτηρίες καπνιστών,
πασχόντων ή μη από χρόνια βρογχίτιδα, εμφύσημα ή πνευμονική υπέρταση. Έχει παρατηρηθεί
αύξηση των μυϊκών ινών, οι οποίες περιβάλλονται από παχιές ελαστικές ίνες, που
διαταράσσουν τη δομή των αγγείων. Επίσης, έχει παρατηρηθεί αύξηση των CD8 και
Τ-λεμφοκυττάρων στα αγγεία, ευρήματα που συμβαδίζουν με την πάχυνση του τοιχώματός
τους και τις λειτουργικές μεταβολές. Τα αρτηριόλια είναι τα μικρά αγγεία που
εφάπτονται με τους κυψελιδικούς πόρους και αποτελούνται από ένα απλό στρώμα
ελαστικών ινών (lamina) και ατελές μυϊκό στρώμα. Στα αρτηριόλια των καπνιστών
παρατηρείται αύξηση των μυϊκών και ελαστικών ινών.
Εναπόθεση
του καπνού του τσιγάρου στο αναπνευστικό σύστημα
Ο καπνός που παράγεται κατά το κάπνισμα
διακρίνεται σε δύο κατηγορίες:
1) στον μη εισπνεόμενο (sidestream smoke-SSS), που παράγεται κατά τα μεσοδιαστήματα
της εισπνοής του καπνού και
2) στον εισπνεόμενο (mainstream smoke-MSS), ο οποίος διέρχεται από το καιόμενο
τσιγάρο και υφίσταται ορισμένες μεταβολές ως προς τη σύνθεσή του.
Από άποψη σύνθεσης, ο καπνός εμφανίζει 2 μορφές (φάσεις):
α) την αεριώδη (92% χημικά συστατικά σε αέρια μορφή) και
β) τη μορφή μικρών σωματιδίων διαλυμένων στο αέριο -aerosol (8%)- (πίνακας 1).
Κάθε εισπνοή καπνού από τον καπνιστή (puff), έχει όγκο 30-80ml και η συγκέντρωση
των σωματιδίων σε αυτήν ανέρχεται περίπου σε 0,3-3.109/ml. H εναπόθεση των σωματιδίων
του καπνού στον πνεύμονα εξαρτάται από:
α) το μέγεθός τους,
β) τον τύπο της αναπνοής και
γ) τη σχέση δομής - λειτουργίας του πνεύμονα.
Εντός του αναπνευστικού τα σωματίδια μπορούν να υποστούν υγροσκοπική μεγέθυνση,
λόγω απορρόφησης υγρασίας. Τα μεγάλα σωματίδια του εισπνεόμενου καπνού, εναποτίθενται
στο αναπνευστικό δένδρο με πρόσκρουση (λόγω ανικανότητας των μεγάλων μορίων
να αλλάζουν κατεύθυνση στις διακλαδώσεις) ή με καθίζηση, σε περιοχές μικρότερης
ροής π.χ. αναπνευστικά βρογχιόλια. Η εναπόθεση των σωματιδίων αυξάνει με την
αργή και βαθιά αναπνοή ή με το κράτημα της αναπνοής. Οι καπνιστές αναπνέουν
συνήθως βαθιά και γρήγορα, προξενώντας αυξημένη εναπόθεση κολλοειδών σωματιδίων
καπνού στις κορυφές του πνεύμονα. Επίσης, οι σχέσεις V/Q του όρθιου πνεύμονα
επηρεάζουν την κατανομή του καπνού. Η εναπόθεση των σωματιδίων του καπνού δεν
ακολουθεί την κλίση του αερισμού στα κατώτερα πνευμονικά πεδία και, θεωρητικά,
το υψηλότερο V/Q των πνευμονικών κορυφών οδηγεί σε αυξημένη εναπόθεση καπνού
στις ανώτερες πνευμονικές ζώνες, όπου έχουμε και χαμηλότερα επίπεδα πρωτεάσης,
η οποία δρα προστατευτικά. Η κατανομή αυτή εξηγεί τη δημιουργία κεντρολοβιώδους
εμφυσήματος στους άνω λοβούς και τη δημιουργία αναπνευστικής βρογχιολίτιδας
στις περιοχές όπου η ταχύτητα καθίζησης είναι μεγαλύτερη.

Μη νεοπλασματικές
νόσοι που συνδέονται με το κάπνισμα
- Χρόνια αποφρακτική πνευμονοπάθεια
(ΧΑΠ). Εμφύσημα, χρόνια βρογχιολίτιδα.
- Πνευμονική υπέρταση.
- Διάμεσες πνευμονικές νόσοι:
Αναπνευστική βρογχιολίτιδα - συνοδευόμενη με διάμεση πνευμονική νόσο (Respiratory
bronchiolitis - associated interstitial lung disease, RB-ILD). Αποφολιδωτική
διάμεση πνευμονία (Desquamative interstitial pneumonia, DIP). Ηωσινόφιλο κοκκίωμα
(Eosinophilic granuloma, EG).
Κάπνισμα και
ΧΑΠ
Το κάπνισμα αποτελεί το σημαντικότερο
παράγοντα κινδύνου ανάπτυξης ΧΑΠ (πίνακας 2). Στις ανεπτυγμένες χώρες 80-85%
των περιπτώσεων της νόσου αποδίδεται στο κάπνισμα, όμως μόνο 15-20% των καπνιστών
αναπτύσσει κλινικά εμφανή ΧΑΠ. Πρέπει όμως να τονιστεί ότι, ένα μεγάλο ποσοστό
καπνιστών αναπτύσσει αποφρακτική συνδρομή, χωρίς κλινικά εμφανή συμπτωματολογία.
Ένα ακόμη μεγαλύτερο ποσοστό καπνιστών παρουσιάζει βήχα και απόχρεμψη, χωρίς
την παρουσία αποφρακτικής συνδρομής. Μία από τις επικρατέστερες θεωρίες παθογένεσης
της ΧΑΠ από το κάπνισμα, είναι η θεωρία της πρωτεάσης - αντιπρωτεάσης, σύμφωνα
με την οποία το κάπνισμα:
α) παράγει οξειδωτικές ουσίες και ελεύθερες ρίζες οξυγόνου, που αναστέλλουν
απευθείας τη δράση της αντιθρυψίνης και
β) προκαλεί ενεργοποίηση και συνάθροιση κυψελιδικών μακροφάγων, τα οποία αφενός
αυξάνουν την παραγωγή ελαστάσης και αφετέρου εκκρίνουν μεταβιβαστές, οι οποίοι
κινητοποιούν, ενεργοποιούν και έλκουν πολυμορφοπύρηνα στον πνεύμονα. Τα πολυμορφοπύρηνα
παράγουν μεγάλα ποσά ελαστάσης. Η μειωμένη και αδρανής αντιθρυψίνη (αντιπρωτεάση)
δεν επαρκεί για την καταστροφή της ελαστάσης, η περίσσεια της οποίας «κατατρώγει»
τις αναπνευστικές μονάδες (τοιχώματα κυψελίδων, συνδετικό ιστό, τριχοειδικό
δίκτυο κ.λπ.). Το κάπνισμα είναι ο μόνος στατιστικά σημαντικός παράγοντας πρόβλεψης
της μείωσης της FEV1, λαμβανομένων υπόψη των διορθωτικών παραγόντων ηλικίας,
φύλου κ.λπ. (σχήμα 1). Παρόλο που είναι γνωστά τα συστατικά του καπνού του τσιγάρου
που ενέχονται στον καρκίνο του πνεύμονα, δεν έχουν εντοπιστεί τα συστατικά εκείνα
που είναι υπεύθυνα για την πρόκληση της ΧΑΠ. Η επίδραση του καπνίσματος στη
λειτουργικότητα του πνεύμονα, συνίσταται σε δημιουργία αποφρακτικού συνδρόμου,
μείωση της διαχυτικής ικανότητας, αύξηση της διατασιμότητας του πνεύμονα και
προοδευτική παγίδευση αέρα (air-trapping), με αποτέλεσμα την υπερδιάτασή του.

Κάπνισμα
και καρκίνος του πνεύμονα
Αποτελεί ένα έξοχο μοντέλο καρκίνου,
που προκαλείται από περιβαλλοντική έκθεση. Είναι ιδιαίτερα σύνθετη νόσος και
απαιτεί μεταλλάξεις για τουλάχιστον 10-20 χρόνια. Ως καρκινογόνες ουσίες στον
καπνό του τσιγάρου ενοχοποιούνται οι πολυαρωματικές αμίνες, οι νιτροζαμίνες,
οι πτητικοί οργανικοί παράγοντες (βενζένιο, φορμαλδεϋδη), καθώς και ραδιενεργά
στοιχεία όπως το πολώνιο 210. Οι καρκινογόνες αυτές ουσίες δρουν μέσω των P450
ενζύμων και οδηγούν στην καρκινογένεση. Η συσχέτιση του καπνίσματος με την ανάπτυξη
καρκίνου του πνεύμονα, είναι ιδιαίτερα ισχυρή για το καρκίνωμα εκ πλακωδών κυττάρων
και για το μικροκυτταρικό καρκίνωμα.
Διάμεσοι
νόσοι του πνεύμονα και κάπνισμα
1. Αναπνευστική βρογχιολίτιδα
- συνοδευόμενη με διάμεση πνευμονική νόσο (Respiratory bronchiolitis - associated
interstitial lung disease, RB-ILD)
Προσβάλλει βαρείς καπνιστές, στην
4η-5η δεκαετία της ζωής τους. Εμφανίζεται με αιφνίδια δύσπνοια, ήπιο περιοριστικό
σύνδρομο και μείωση της διαχυτικής ικανότητας του πνεύμονα. Η ακτινογραφία θώρακα
είναι παθολογική στο 70-80% των ασθενών και εμφανίζει διάχυτες αμφοτερόπλευρες
δικτυοζώδεις σκιάσεις. Η αξονική τομογραφία υψηλής ευκρίνειας παρουσιάζει σκιάσεις
τύπου θολής υάλου (ground glass), στα άνω πνευμονικά πεδία και μικροοζίδια μη
καλώς σχηματισμένα. Παθολογοανατομικά, η νόσος χαρακτηρίζεται από την παρουσία
κεχρωσμένων ενδοαυλικών μακροφάγων στα αναπνευστικά βρογχιόλια και η πρόγνωση
της νόσου είναι άριστη, κατόπιν διακοπής του καπνίσματος και χρήσης κορτικοειδών.
2. Αποφολιδωτική διάμεση
πνευμονία (Desquamative interstitial pneumonia, DIP)
Εμφανίζεται κατά την 5η δεκαετία της
ζωής και προσβάλλει κατά 90% καπνιστές. Εκδηλώνεται συνήθως με αιφνίδια έναρξη
δύσπνοιας και ξηρό βήχα. Προκαλεί περιοριστικού τύπου διαταραχές και μείωση
της διαχυτικής ικανότητας. Στην ακτινογραφία θώρακα παρουσιάζεται με βλάβες
θολής υάλου, ενώ στην αξονική τομογραφία υψηλής ευκρίνειας με εικόνα θολής υάλου
(ground glass) και σπάνια με βλάβες μελικηρύθρας. Η πρόγνωση της νόσου είναι
καλή. Τα 2/3 των ασθενών επιβιώνουν και βελτιώνονται (αυτόματη βελτίωση ή μετά
από χορήγηση ανοσοκατασταλτικών). Η κύρια ιστολογική βλάβη είναι η παρουσία
κεχρωσμένων μακροφάγων εντός των κυψελίδων.
3. Ηωσινόφιλο κοκκίωμα
(Eosinophilic granuloma, EG)
Εμφανίζεται συνήθως την 4η ή 5η δεκαετία
της ζωής σε καπνιστές ή πρώην καπνιστές. Το 70% των ασθενών παρουσιάζει σαν
αρχικό σύμπτωμα βήχα και δύσπνοια, το 25% αυτόματο πνευμοθώρακα και λιγότερο
από το 1/3 των ασθενών εμφανίζει γενικευμένα συμπτώματα (πυρετό, κακουχία, απώλεια
βάρους). Στην ακτινογραφία θώρακα παρατηρούνται συνήθως διάχυτες αμφοτερόπλευρες
διάμεσες σκιάσεις, με δικτυοοζώδη χαρακτήρα, σπάνια δε μπορεί να εμφανισθεί
ως μονήρης όζος ή ως ενδοβρογχικός όγκος, με συνοδό δευτεροπαθή ατελεκτασία
ή με προσβολή των μεσοθωρακίων λεμφαδένων. Στα αρχικά στάδια στην αξονική τομογραφία
θώρακα υψηλής ευκρίνειας, παρουσιάζεται με τη μορφή πολλαπλών οζιδίων ή λεπτοτοιχωματικών
κύστεων, στην περιοχή των άνω πνευμονικών πεδίων, μετέπειτα δε ελαττώνονται
τα οζίδια και αυξάνονται οι κύστεις. Η πρόγνωση είναι σχετικά καλή και λιγότερο
από το 10% των ασθενών έχουν προοδευτική μοιραία πορεία. Το ηωσινόφιλο κοκκίωμα
μπορεί να προηγηθεί, να συνυπάρχει ή να ακολουθήσει κακοήθεια ή νόσο του Ηοgkin.
Η ιστολογική διάγνωση γίνεται με βιοψία πνευμονικού τμήματος από θωρακοτομή
ή θωρακοσκόπηση. Η διαβρογχική βιοψία συνήθως δεν είναι διαγνωστική. Τα κύτταρα
Langerhans που συγκεντρώνονται στο διάμεσο χώρο, είναι διαγνωστικά για το ηωσινόφιλο
κοκκίωμα.
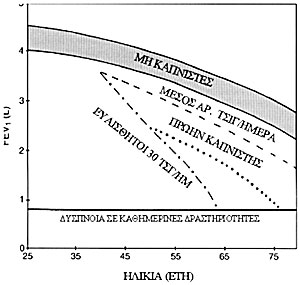
Σχήμα
1. Επίδραση του καπνίσματος στη φυσιολογική εξέλιξη του αναπνευστικού
συστήματος. Φυσιολογικά η FEV1 φθάνει το peak μεταξύ 15-25 χρόνων. Από 25-35
χρόνων διατηρείται σε plateau και από την ηλικία των 35 ετών και μετά ελαττώνεται,
με ρυθμό 30ml/χρόνο στους μη καπνιστές. Καπνιστές κατά μέσον όρο 30 τσιγάρων/ημέρα
έχουν ελαφρά μεγαλύτερο ρυθμό μείωσης της FEV1 και τιμές λίγο μικρότερες του
μέσου όρου των φυσιολογικών, μέχρι την ηλικία των 40 ετών. Σε ένα μικρό ποσοστό
ευαίσθητων καπνιστών (10-15%) η FEV1 ελαττώνεται ταχύτερα με ρυθμό 150ml/χρόνο,
με αποτέλεσμα να έχουν FEV1 0,8ml στην ηλικία των 65 ετών, ποσοστό τόσο χαμηλό
ώστε να εκδηλώνουν δύσπνοια σε καθημερινές δραστηριότητες. Ένας ευαίσθητος καπνιστής
που σταματάει το κάπνισμα στην ηλικία των 50 ετών, δεν ξανακερδίζει τη χαμένη
λειτουργικότητα, αλλά τα επόμενα χρόνια η απώλεια της πνευμονικής λειτουργίας
είναι ίδια με των μη καπνιστών. Η εμφάνιση δύσπνοιας κατά την εκτέλεση καθημερινών
δραστηριοτήτων θα εκδηλωθεί, σύμφωνα με τους μαθηματικούς υπολογισμούς, στην
ηλικία των 76 ετών, δηλαδή 11 χρόνια αργότερα από ό,τι αν συνέχιζαν να καπνίζουν.
Επίδραση του
καπνίσματος σε άλλες πνευμονικές νόσους
-
Κοινό κρυολόγημα: οι καπνιστές παθαίνουν περισσότερα κρυολογήματα
στη διάρκεια του έτους, πιο σοβαρά, με συχνότερες επιπλοκές από το κατώτερο
αναπνευστικό, σε σύγκριση με τους μη καπνιστές.
- Γρίππη: σαφής η σχέση της με το κάπνισμα, βαρύτερη η πρόγνωσή της
στους καπνιστές.
- Φυματίωση:
το κάπνισμα επιδρά στην αντιδραστικότητα της δοκιμασίας φυματίνης (Mantoux),
στη μετατροπή της, ακόμη και στην εμφάνιση ενεργού φυματίωσης. Σε μεγάλη έρευνα
που πραγματοποιήθηκε στο San Francisco στις ΗΠΑ το 1996, σε μετανάστες από την
Ανατολική Ασία, βρέθηκε συσχέτιση μεταξύ παθητικού καπνίσματος και εμφάνισης
ενεργού νόσου μετά από έκθεση στο μυκοβακτηρίδιο, ιδιαίτερα στα μικρά παιδιά,
εξαρτώμενη μάλιστα από το ποσοστό έκθεσης στο κάπνισμα.
- Βακτηριδιακή πνευμονία:
το ενεργητικό και το παθητικό κάπνισμα αποτελούν παράγοντες κινδύνου για βακτηριδιακή
πνευμονία, διότι αυξάνουν τον αποικισμό του αναπνευστικού συστήματος με βακτηρίδια
και μεταβάλλουν τη μικροβιολογία της πνευμονίας της κοινότητας. Γι' αυτό και
σε καπνιστές με πνευμονία απαιτείται θεραπεία με αντιβιοτικά ευρύτερου φάσματος.
- Πνευμονία από ανεμοβλογιά:
έχει βαρύτερη εικόνα στους ενήλικες και μάλιστα στους καπνιστές. Η από του στόματος
χορήγηση acyclovir ελαττώνει τη βαρύτητα της νόσου σε ενήλικες και παιδιά. Επειδή
οι καπνιστές έχουν αυξημένη συχνότητα εμφάνισης πνευμονίτιδας, συνιστάται η
από του στόματος χορήγηση acyclovir σε όλους τους ενήλικες καπνιστές με ανεμοβλογιά.
Σε όσους μάλιστα εκδηλώνεται πνευμονίτιδα, συνιστάται η ενδοφλέβια χορήγηση
acyclovir.
- Κάπνισμα και πνευμονική
αιμορραγία: το κάπνισμα φαίνεται να παίζει ρόλο στην προσβολή των
πνευμόνων στο σύνδρομο Goodpasture. Ερευνητικά πρωτόκολλα δείχνουν πιθανή σύνδεση
μεταξύ καπνίσματος και ιδιοπαθούς πνευμονικής αιμοσιδήρωσης. Γι' αυτό σε αρρώστους
με πνευμονική αιμορραγία συνιστάται η αποφυγή έκθεσης στις εισπνεόμενες τοξίνες
του καπνού.
- Κάπνισμα και πνευμονική
μεταστατική νόσος: έρευνες εισηγούνται ότι το κάπνισμα αυξάνει τη
συχνότητα των πνευμονικών μεταστάσεων στον καρκίνο του μαστού. Σε γενικές γραμμές,
σύμφωνα με τα αποτελέσματα ερευνών, ασθενείς που καπνίζουν και πάσχουν από οποιονδήποτε
καρκίνο, έχουν μεγαλύτερη συχνότητα πνευμονικών μεταστάσεων.
- Κάπνισμα και αυτόματος
πνευμοθώρακας: το κάπνισμα είναι μεγάλος παράγοντας κινδύνου για
την εμφάνιση αυτόματου πνευμοθώρακα, διότι προκαλεί παγίδευση αέρα και φλεγμονή
των βρογχιολίων, με αποτέλεσμα υπερδιάταση και ρήξη των κυψελίδων.
- Κάπνισμα και αμιάντωση:
αμιάντωση είναι η χρόνια προοδευτική πνευμονική νόσος, που προκαλείται από την
εισπνοή ινών αμιάντου. Για την εμφάνισή της απαιτείται περίοδος έκθεσης 20-30
χρόνια. Έχει αποδειχθεί ότι, η έκθεση σε ίνες αμιάντου σε καπνιστές συνοδεύεται
από αυξημένη συχνότητα καρκίνου πνεύμονα. Πιθανός μηχανισμός πρόκλησης είναι
η επίδραση του καπνίσματος στην κάθαρση των εισπνεόμενων ινών αμιάντου, επειδή
διευκολύνει τη διαπερατότητά τους σε απομακρυσμένες περιοχές του πνεύμονα. Οι
μελέτες του ΒAL ασθενών με αμιάντωση δείχνουν ενεργό κυψελιδίτιδα, με αυξημένο
αριθμό ενεργοποιημένων ουδετεροφίλων και μακροφάγων.
Νόσοι
των οποίων η συχνότητα ή η βαρύτητα ελαττώνεται με το κάπνισμα
- Σαρκοείδωση:
από μελέτες έχει βρεθεί ότι η σαρκοείδωση είναι συχνότερη στους μη καπνιστές
και αυτό πιθανόν οφείλεται στις μεταβολές, οι οποίες προκαλούνται με το κάπνισμα
στη δραστηριότητα των κυψελιδικών μακροφάγων και στους πνευμονικούς υποπληθυσμούς
και οι οποίες δρουν προστατευτικά στην εμφάνιση πνευμονικής σαρκοείδωσης.
-Πνευμονίτιδα εξ υπερευαισθησίας:
έχει επίσης παρατηρηθεί ότι είναι λιγότερο συχνή στους καπνιστές, αλλά όταν
εμφανιστεί έχει χειρότερη πρόγνωση και βαρύτερη πορεία.
Περαιτέρω έλεγχοι απαιτούνται, πάντως, για τεκμηρίωση της ευνοϊκής συσχέτισης
των δυο αυτών νοσημάτων με το κάπνισμα.
Κάπνισμα
και μετεγχειρητικές επιπλοκές στους πνεύμονες
- Μετεγχειρητική πνευμονία:
σε έρευνες που έγιναν διαπιστώθηκε μεγαλύτερος κίνδυνος, εξαρτώμενος από τον
αριθμό τσιγάρων ανά ημέρα, εμφάνισης μετεγχειρητικής πνευμονίας σε καπνιστές,
λόγω υπερέκκρισης βλέννης και απόφραξης αεραγωγών.
Το κάπνισμα συνδέεται επίσης με αυξημένο κίνδυνο παρατεταμένου μηχανικού αερισμού
μετεγχειρητικά. Έρευνες έχουν δείξει ότι, η διάρκεια του μετεγχειρητικού μηχανικού
αερισμού εξαρτάται από τα πακέτα/έτη καπνίσματος, το προεγχειρητικό ΡαΟ2 και
την αυξημένη απώλεια αίματος. Ο καλύτερος χρόνος για τη διακοπή του καπνίσματος,
έχει αποδειχθεί ότι είναι 6-8 εβδομάδες πριν από την επέμβαση. Δεν είναι ξεκαθαρισμένο
αν η διακοπή του καπνίσματος σε χρονικό διάστημα πλησιέστερο στην επέμβαση (πιθανόν
λόγω υπερέκκρισης βλέννης και συμπτωμάτων απόσυρσης νικοτίνης), αυξάνει τον
κίνδυνο επιπλοκών από το αναπνευστικό.
Επιπλοκές
του καπνίσματος στους ανώτερους αεραγωγούς
- Οι λευκοπλακίες είναι οι συνηθέστερες
προκαρκινικές βλάβες της στοματικής κοιλότητας και συνδέονται άμεσα με τη χρήση
του καπνού. Ορίζονται κλινικά ως λευκές πλάκες μη κερατινοποιημένου βλεννογόνου,
που στερούνται παθολογοανατομικών χαρακτήρων άλλης νόσου. Δυσπλασία μπορεί να
υπάρχει στο 3-15% των ασθενών με λευκοπλακία. Κάθε άτομο με λευκοπλακία θα πρέπει
να ενημερώνεται για τα οφέλη της διακοπής του καπνίσματος και να παρακολουθείται
τακτικά για τυχόν εξέλιξη της βλάβης.
- Οι ερυθροπλακίες είναι βλάβες του στοματικού βλεννογόνου, που εμφανίζονται
ως ερυθρές πλάκες, σύστασης βελούδου, με λευκές ή κίτρινες κηλίδες, που αιμορραγούν
όταν πιεσθούν με γάζα. Μικροσκοπικά εμφανίζουν επιθηλιακή ατροφία και άλλοτε
άλλου βαθμού δυσπλασίες. Είναι σπανιότερες από τις λευκοπλακίες, αλλά έχουν
5-7 φορές μεγαλύτερο κίνδυνο εξαλλαγής.
- Ο καρκίνος της στοματικής κοιλότητας αντιπροσωπεύει το 30% των καρκίνων κεφαλής
- τραχήλου και το 4-5% όλων των κακοήθων όγκων. Το 90% των κακοηθειών της στοματικής
κοιλότητας είναι καρκινώματα πλακώδους τύπου, συμβαίνουν συνήθως σε άτομα ηλικίας
40-80 ετών, αλλά επιθετικά νεοπλάσματα έχουν αναφερθεί και σε άτομα ηλικίας
μικρότερης των 40 ετών. Η χρήση αιθυλικής αλκοόλης είναι συχνά συνηγορητικός
παράγοντας. Κατά σειρά συχνότητας προσβάλλονται τα χείλη, η γλώσσα και το έδαφος
του στόματος.
- Ο καρκίνος του στοματοφάρυγγα και υποφάρυγγα, παρουσιάζεται συνήθως σαν παρατεινόμενη
φαρυγγαλγία ή αίσθηση ξένου σώματος. Τρισμός, δυσφαγία και δυσαρθρία, εκδηλώνονται
όταν η νόσος διηθεί τους παρακείμενους ιστούς. Συχνά εμφανίζονται με εικόνα
τραχηλικής μάζας και έχουν πτωχή πρόγνωση. Γενικά, κάθε ασθενής με ιστορικό
επίμονου άλγους κατά τη σίτιση ή ανεξήγητης ωταλγίας διαρκείας μεγαλύτερης των
4 εβδομάδων, χρήζει πληρέστερης διερεύνησης κεφαλής - τραχήλου.
- Ο καρκίνος του λάρυγγα συνδέεται επιδημιολογικά με τον καρκίνο του πνεύμονα
και έχει άμεση σχέση με το κάπνισμα. Οι ασθενείς εμφανίζονται συνήθως με παρατεινόμενο
βράγχος φωνής. Η πρώιμη διάγνωση και θεραπεία έχει άριστη πρόγνωση. Ασθενείς
καπνιστές με επίμονο βράγχος φωνής, πρέπει να υποβάλλονται σε λεπτομερή εξέταση
λάρυγγα.
- Οι όγκοι των σιελογόνων αδένων είναι σπανιότεροι. Ο όγκος του Warthin είναι
σχετικά σπάνια καλοήθης νεοπλασία των σιελογόνων αδένων, που συμβαίνει κατά
80-90% σε πρώην καπνιστές. Έχει διατυπωθεί η υπόθεση ότι, οι εισπνεόμενες ερεθιστικές
ουσίες του καπνού έρχονται σε επαφή με την παρωτίδα και προκαλούν μετάπλαση
και υπερπλασία των κυστικών, αδενικών και λεμφοειδών στοιχείων. Η θεραπεία είναι
η χειρουργική αφαίρεση.
- Άλλη μη κακοήθης διαταραχή των ανώτερων αεραγωγών, που συνδέεται με το κάπνισμα,
είναι η περιοδοντική νόσος. Επίσης, η επίδραση της έκθεσης στον καπνό του βλεννογόνου
των παραρρινίων κόλπων, δεν είναι απολύτως γνωστή. Θεωρείται ότι η έκθεση στον
καπνό επηρεάζει τη βλεννοκροσσωτή κάθαρση, καθώς και την ποιότητα και την ποσότητα
της βλέννης, γι αυτό ενήλικες καπνιστές έχουν υψηλά ποσοστά επεμβάσεων για
χρόνια παραρρινοκολπίτιδα. Επίσης, ρινοφαρυγγική λεμφοειδής υπερπλασία έχει
περιγραφεί στους βαρείς καπνιστές. Ο μηχανισμός πρόκλησής της δεν είναι απόλυτα
κατανοητός. Παρόλα αυτά, διακοπή του καπνίσματος σε συνδυασμό με προοδευτικά
μειούμενες δόσεις κορτικοστεροειδών, βοηθά στην αντιμετώπιση των αδενοειδών
και λεμφοειδών εκβλαστήσεων. Το κάπνισμα, επίσης, ενέχεται για το ροχαλητό και
την πρόκληση υπνοαπνοϊκού συνδρόμου, λόγω μεταβολών στην ανατομία των λεμφαδενικών
ιστών του ανώτερου αναπνευστικού. Η μέση ωτίτιδα έχει βρεθεί, από έρευνες, ότι
είναι συχνότερη σε παιδιά ηλικίας μικρότερης των 5 ετών, που η μητέρα τους καπνίζει.
Στους ενήλικες με μέση ωτίτιδα, πιθανοί μηχανισμοί δράσης του καπνού είναι η
επίδραση στη βλεννοκροσσωτή κάθαρση, ο έμμεσος ερεθισμός του βλεννογόνου των
ευσταχιανών σαλπίγγων και η ανοσοκαταστολή. Το οίδημα Reinke είναι καλοήθης
πάθηση των φωνητικών χορδών, που χαρακτηρίζεται από συλλογή υγρού στο χώρο του
Reinke, στην πτυχή της φωνητικής χορδής. Εκδηλώνεται με βαθιά, βραχνή και μονότονη
φωνή και συνδέεται με το κάπνισμα και την υπέρχρηση φωνής. Αντιμετωπίζεται με
χειρουργική αποφλοίωση ή με μικροχειρουργική με λέιζερ.
Kάπνισμα
και καρδιαγγειακά νοσήματα
Υπάρχει μεγάλη επιδημιολογική συσχέτιση
μεταξύ καπνίσματος και καρδιαγγειακών νόσων. Οι αυτοψίες και οι αγγειογραφικές
μελέτες δείχνουν επίσης ότι, το κάπνισμα σχετίζεται με αρτηριοσκλήρυνση των
αγγείων, σε δοσοεξαρτώμενη μάλιστα σχέση. Τις τελευταίες δεκαετίες διενεργούνται
πολλές έρευνες για την κατανόηση της παθοφυσιολογίας των νοσημάτων, τα οποία
συνδέονται με το κάπνισμα και έχουν επιτευχθεί μεγάλα άλματα στη διαλεύκανση
των μηχανισμών, δια των οποίων ο καπνός προκαλεί βλάβες στο καρδιαγγειακό σύστημα.
Σύμφωνα με στατιστικά δεδομένα, οι καπνιστές πεθαίνουν 7 χρόνια νωρίτερα από
τους μη καπνιστές.
Επίδραση του
καπνίσματος στο αίμα
Συστατικά του αίματος όπως τα λευκά
αιμοσφαίρια, τα αιμοπετάλια, οι παράγοντες πήξης, επηρεάζονται τόσο από τον
ΜSS όσο και από τον SSS καπνό. Η έκθεση στον ΜSS και SSS καπνό προκαλεί αύξηση
των λευκών αιμοσφαιρίων, κυρίως λόγω αύξησης των ουδετεροφίλων του περιφερικού
αίματος. Κάπνισμα έστω και δύο τσιγάρων, οδηγεί σε ενεργοποίηση των λευκοκυττάρων.
Η ενεργοποίηση των ουδετεροφίλων από τον καπνό μπορεί να συμβάλλει στην εμφάνιση
καρδιαγγειακής νόσου. Τα ουδετερόφιλα παράγουν αυξημένα ποσά ελευθέρων ριζών
οξυγόνου και ελαστάσης, που μπορούν να προξενήσουν βλάβες στο επιθήλιο των αγγείων
και να επιταχύνουν την εμφάνιση αθηροσκλήρυνσης. Η χρόνια έκθεση σε ΜSS οδηγεί
σε ελάττωση του αριθμού των κυκλοφορούντων λεμφοκυττάρων, καταστολή της λειτουργίας
των Τ και Β κυττάρων και πολλαπλασιασμό των Τ κυττάρων. Ο ΜSS προκαλεί σημαντική
αύξηση των μονοκυττάρων και καταλήγει σε δοσοεξαρτώμενη αύξηση της προσκόλλησης
των μονοκυττάρων στο ενδοθήλιο. Αυτή η αύξηση της προσκόλλησης των μονοκυττάρων
προκαλείται με αύξηση της ιντεγκρίνης CD11b στην επιφάνεια των μονοκυττάρων.
Η προσκόλληση και η μετανάστευση των μονοκυττάρων στον υπενδοθηλιακό χώρο, η
φαινοτυπική τους μεταμόρφωση σε μακροφάγα και η πρόσληψη χοληστερόλης και εστέρων
χοληστερόλης, είναι μεταξύ των πρωτοπαθών αιτίων, τα οποία οδηγούν στην εμφάνιση
αθηρώματος. Ερευνητικά δεδομένα δείχνουν επίσης ότι η έκθεση στον καπνό προξενεί
ενεργοποίηση των αιμοπεταλίων, με διάφορους μηχανισμούς.
Αποτέλεσμα της ενεργοποίησης των αιμοπεταλίων και της χρόνιας χρήσης καπνού,
είναι η απελευθέρωση του αιμοπεταλιακού αυξητικού παράγοντα (platelet - derived
growth factor, PDFG). Ο PDFG προάγει την παραγωγή λείων μυϊκών κυττάρων, που
είναι ένα από τα αρχικά βήματα της εμφάνισης αθηροσκλήρυνσης. Ο καπνός του τσιγάρου
προκαλεί επίσης αλλαγές σε συστατικά του αίματος, αποτέλεσμα των οποίων είναι
ότι προδιαθέτει σε σχηματισμό θρόμβων, που μπορούν να οδηγήσουν σε έμφραγμα
του μυοκαρδίου ασθενείς με ή χωρίς αρτηριοσκλήρυνση των στεφανιαίων.
Κάπνισμα,
λιπίδια ορού και λιποπρωτεϊνες
Οι λιποπρωτεϊνες είναι υπεύθυνες για
τη συνοδεία των τριγλυκεριδίων και της χοληστερόλης στο αίμα και σκοπός τους
είναι η διατήρηση της ομοιόστασης των λιπιδίων στο σώμα. Ο ΜSS επηρεάζει τόσο
τα επίπεδα των λιποπρωτεϊνών στο αίμα όσο και το μεταβολισμό τους. Επίσης, η
νικοτίνη από τον εισπνεόμενο καπνό ενεργοποιεί το συμπαθητικό νευρικό σύστημα
και οδηγεί σε απελευθέρωση των κατεχολαμινών. Το συμπαθητικό νευρικό σύστημα
ενεργοποιεί την ορμονοευαίσθητη λιπάση και αυξάνει το ποσό των ελεύθερων λιπαρών
οξέων στο αίμα (free fatty acids, FFAs).Το ήπαρ απομακρύνει τα FFAs από το αίμα
και τα εκκρίνει πάλι στην κυκλοφορία, ως πολύ χαμηλής πυκνότητας λιποπρωτεϊνες
(VLDL). Αυτή η διαδικασία αυξάνει τα επίπεδα των VLDL και των LDL (μέσω του
ενδογενούς μονοπατιού της χοληστερόλης), σε τιμές υψηλότερες των φυσιολογικών
και οδηγεί σε ελάττωση της υψηλής πυκνότητας λιποπρωτεϊνών (HDL). Επιπλέον,
έχει αποδειχθεί ότι υπάρχει μία δοσοεξαρτώμενη σχέση μεταξύ του αριθμού των
τσιγάρων και των επιπέδων FFAs στο πλάσμα, που δείχνει ότι το κάπνισμα επιδρά
στα επίπεδα των LDL μέσω αλλαγών στο μεταβολισμό της τριγλυκερόλης.
Επίδραση
του καπνίσματος στο μυοκάρδιο
Η έκθεση στον καπνό αλλάζει τη λειτουργία
και τη δομή της καρδιάς. Η αύξηση της ανθρακυλαιμοσφαιρίνης στο αίμα, καταλήγει
σε μείωση της μεταφορικής χωρητικότητας του οξυγόνου, ενώ η ενεργοποίηση από
τη νικοτίνη του α-αδρενεργικού συμπαθητικού νευρικού συστήματος, οδηγεί σε αγγειοσύσπαση
των στεφανιαίων και ελάττωση της ροής του αίματος στο μυοκάρδιο. Άτομα τα οποία
εκτίθενται στο παθητικό κάπνισμα, αυξάνουν τα επίπεδα της ανθρακυλαιμοσφαιρίνης
στο αίμα >3%. Έκθεση πειραματοζώων σε συγκεντρώσεις CO της τάξης των 180ppm,
προκαλεί εκφυλιστικές βλάβες στους καρδιακούς ιστούς, νεκρώσεις μυϊκών ινιδίων,
βλάβες μιτοχονδρίων, ενδοκυττάριο και εξωκυττάριο οίδημα.
Επίδραση
του καπνίσματος στο τοίχωμα των αρτηριών
Τα μεγάλα σωματίδια του καπνού αποβάλλονται
από το αναπνευστικό. Τα μικρά όμως σωματίδια και η αέρια φάση του παθητικού
καπνίσματος μπορούν να περάσουν στο αίμα, όπου αντιδρούν με ποικίλους παράγοντες
(λιποπρωτεΐνες, αιμοπετάλια, λεμφοκύτταρα και ερυθρά αιμοσφαίρια) και προκαλούν
αποψίλωση και καταστροφή των ενδοθηλιακών κυττάρων των αγγείων. Προκαλούν ακόμη
σκλήρυνση των αγγείων, μέσω αδρενεργικών μηχανισμών, καθώς και με την εμφάνιση
τελικών προϊόντων αποδόμησης (advanced glycation end products, AGEs) στο τοίχωμα
των αγγείων. Με τους μηχανισμούς αυτούς προάγεται η αθηρογένεση.
Οι επιδράσεις του καπνίσματος στο αναπνευστικό και στο καρδιαγγειακό σύστημα,
είναι αποτέλεσμα πολλαπλών και πολύπλοκων μηχανισμών, οι οποίοι αποτελούν επί
του παρόντος πεδίο εντατικής έρευνας. Όπως προκύπτει από τα μέχρι τώρα αποτελέσματα,
είναι υψίστης σημασίας η ενημέρωση των πολιτών από τους ιατρούς, το νοσηλευτικό
προσωπικό και τους υπεύθυνους τομείς της πολιτείας, για τις ολέθριες συνέπειες
του καπνίσματος. Προγράμματα, τα οποία στοχεύουν σε σωστή ενημέρωση για την
καταπολέμηση της καπνιστικής συνήθειας, αποτελούν το θεμέλιο λίθο στη μάχη εναντίον
του καπνίσματος και στην πρόληψη επιπλοκών του από το αναπνευστικό και το καρδιαγγειακό
σύστημα.
Βιβλιογραφία
1) Casolaro M, Bernaudin JF, Saltini
C, et al. Accumulation of Langerhans' cells on the epithelial surface of the
lower respiratory tract in normal subjects in association with cigarette smoking.
Am Rev Respir Dis 1988; 137:406-411.
2) Di Stefano A, Capelli A, Lusuardi M, et al. Severity of airflow limitation
is associated with severity of airway inflammation in smokers. Am J Respir Crit
Care Med 1998; 158:1.277-1.285.
3) Eidelman D, Saetta MP, Ghezzo H, et al. Cellularity of the alveolar walls
in smokers and its relation to alveolar destruction. Am Rev Respir Dis 1990;
141:1.547-1.552.
4) Hartman TE, Primack SL, Kang E-Y, et al. Disease progression in usual interstitial
pneumonia compared with desquamative interstitial pneumonia. Chest 1996; 110:378-382.
5) Peinardo VI, Barbera JA, Abate P, et al. Inflammatory reaction in pulmonary
muscular arteries of patients with mild chronic obstructive pulmonary disease.
Am Respir Crit Care Med 1999; 159:1.605-1.611.
6) Saetta M, Shiner RJ, Angus GE, et al. Destructive index: A measurement of
lung parenchymal destruction in smokers. Am Rev Respir Dis 1985; 131:764-769.
7) Saetta M, Turato G, Facchini FM, et al. Inflammatory cells in the bronchial
glands of smokers with chronic bronchitis. Am J Resp Crit Care Med 1997; 156:1.633-1.639.
8) Anthonisen NR, Connet JE, Killey JP, et al. Effects of smoking intervention
and the use of an inhaled anticholinergic bronchodilator on the rate of decline
of FEV1.The Lung Health Study, JAMA 1994; 272:1.497-1.505.
9) Barbera JA, Riverola A, Roca J, et al. Pulmonary vascular abnormalities and
ventilation-perfusion relationships in mild chronic obstructive pulmonary disease.
Am J Respir Crit Care Med 1994; 149:423-429.
10) Bluman LG, Mosca L, Newman N, et al. Preoperative smoking habits and postoperative
pulmonary complications. Chest 1998; 113:883-889.
11) Burnet TD, Chamba A, Hill SL, et al. Neutrophils from subjects with chronic
obstructive lung disease show enhanced chemotaxis and extracellular proteolysis.
Lancet 1987; 2:1.043-1.046.
12) Hasday JD, Bascom R, Costa JJ, et al. Bacterial enotoxin is an active component
of cigarette smoke. Chest 1999; 115:829-835.
13) Hohlfeld J, Fabel H, Hamm H. The role of pulmonary surfactant in obstructive
airways disease. Eur Respir J 1997; 10:482-491.
14) Jensen EJ, Dahl R, Steffensen F. Bronchial reactivity to cigarette smoke
in smokers: Repeatability, relationship to metacholine reactivity, smoking and
atopy. Eur Respir J 1998; 11:670-676.
15) Kanner RE, Connett JE, Williams DE, et al. Effects of randomized assignment
to a smoking cessation intervention and changes in smoking habits on respiratory
symptoms in smokers with early chronic obstructive pulmonary disease: The Lung
Health Study. Am J Med 1999; 106:410-416.
16) Monso E, Rosell A, Bonet G, et al. Risk factors for lower airway bacterial
colonization in chronic bronchitis. Eur Respir J 1999; 13:338-342.
17) O'Shaughnessy TC, Ansari TW, Barnes NC, et al. Inflammatory cells in the
airway surface epithelium of bronchi tic smokers with and without airflow obstruction.
Am J Respir Crit Care Med 1997; 155:852-857.
18) Ofulue AF, Ko M, Abdoud RT. Time course of neutrophil and macrophage elastinolytic
activities in cigarette smoke-induced emphesema. Am J Physiol 1998; 275:L1.134-L1.144.
19) Alcaide J, Kane MA, King TA, et al. Cigarette smoking as a risk factor for
tuberculosis in young adults: A case-control study. Tuber Lung Dis 1996; 77:112-116.
20) Almirall J, Gonzalez CA, Balanzo X, et al. Proportion of community-acquired
pneumonia cases attributable to tobacco smoking. Chest 1999; 116:375-379.
21) Altet MN, Alcaide J, Plans P, et al. Passive smoking and risk of pulmonary
tuberculosis in children immediately following infection. A case control study.
Tuber Lung Dis 1996; 77:537-544.
22) Anderson RH, Sy SFS, Thompson S, et al. Cigarette smoking and tuberculin
skin test conversion among incarcerated adults. Am J Prevent Med 1997; 13:175-181.
23) Arvin AM. Varicella-zoster virus. Clin Microbiol 1996; Rev 9:361-381.
24) Bartlett GS, Breiman RF, Mantel LA, et al. Community acquired pneumonia
in adults: Guidelines for management. The Infectious Disease Society of America.
Clin Infect Dis 1998; 25:811-838.
25) Douglas JG, Middleton WG, Gaddie J, et al. Sarcoidosis: A disorder commoner
in non smokers? Thorax 1986; 41:787-791.
26) Markowitz SB, Morabia A, Lilis R, et al: Clinical predictors of mortality
from asbestosis in the North American Insulator Cohort, 1981-1991. Am J Respir
Crit Care Med 1997; 156:101-108.
27) Mc Gurdy SA, Arretz DS, Bates RO. Tuberculin reactivity among California
Hispanic migrant farm workers. Am J Indust Med 1997; 32:600-605.
28) Murin S. Cigarette smoking and the risk of pulmonary metastases from breast
cancer. Journal of Investigative Medicine 1999; 47(2):36A.
29) Sadikot RT, Greene T, Meadows K, et al. Recurrence of primary spontaneous
pneumothorax. Thorax 1997; 52:805-809.
30) Terashima T, Wiggs B, English D, et al. The effect of cigarette smoking
on the bone marrow. Am J Crit Care Med 1997; 155:1.021-1.026.
31) Barisione G, Rovida S, Gazzaniga GM, et al. Upper abdominal surgery: does
a lung function test exist to predict early severe postoperative respiratory
complications? Eur Respir J 1997; 10:1.301-1.308.
32) Bluman LG, Mosca L, Newman N, et al. Preoperative smoking habits and postoperative
pulmonary complications. Chest 1998; 113:883-889.
33) Brooks-Brunn JA. Predictors of postoperative pulmonary complications following
abdominal surgery. Chest 1997; 111:564-571.
34) Brooks-Brunn JA. Validation of a predictive model for postoperative pulmonary
complications. Heart Lung 1998; 27:151-158.
35) Mitchell CK, Smoger SH, Pfeifer MP, et al. Multivariate analysis of factors
associated with postoperative pulmonary complications following general elective
surgery. Arch Surg 1998; 133:194-198.
36) Warner DO, Warner MA, Offord KP, et al. Airway obstruction and perioperative
complications in smokers undergoing abdominal surgery. Anesthesiology 1999;
90:372-379.
37) Agius AM, Smallman LA, Pahor Al. Age, smoking and nasal ciliary beat frequency.
Clin Otolaryngol 1998; 23:227-230.
38) Hoffman HT, Karnell LH, Funk GF, et al. The National Cancer Data Base report
on cancer of the head and neck. Arc Otolaryngol Head Neck Surg 1998; 1.124:951-963.
39) Klein JO, Tos M, Casselbrandt ML, et al. Recent advances in otitis media.
In Lim DJ (ed); Report Of The Sixth Research Conference. Ann Otol Rhinol Laryngol
1998; 107(10, part 2):9-13.
40) McGuirt WF. Commentary: Cigar smoking. Otolaryngol Head Neck Surg 1998;
119:151-152.
41) Raabe J, Pascher W. Reinke's edema: An investigation of questions related
to etiology, prognosis and effectiveness of therapeutic methods. Laryngootologie
1999; 78:97-102.
42) Vories AA, Ramirez SG. Warthin' s tumor and cigarette smoking. South Med
J 1997; 90:416-418.
43) Wilson TG, Higginbottom FL. Periodontal diseases and dental implants in
older adults. Journal of aesthetic Dentistry 1998; 10:265-271.
44) Zieske AE, Takei H, Fallon KB, et al. Smoking and atherosclerosis in youth.
Atherosclerosis 1999; 144:403-408.
45) Morrow JD, Frei B, Longmire AW, et al. Increase in circulating products
of lipid peroxidation in smokers; smoking as a cause of oxidative damage. N
Engl J Med 1995; 332:1.198-1.203.
46) Raitakari OT, Adams MR, McCredie RJ, et al. Arterial endothelial dysfunction
related to passive smoking is potentially reversible in healthy young adults.
Ann Intern Med 1999; 130:578-581.
47) Weber C, Erl W, Weber K, et al. Increased adhesiveness of isolated monocytes
to endothelium is prevented by vitamin C intake in smokers. Circulation 1996;
93:1.488-1.492.
48) Witztum JL, Palinski W. Are immunological mechanisms relevant for the development
of atherosclerosis? Clin Immunol 1999; 90:153-156.
49) Haraguchi M, Shimura S, Shirato K: Morphometric analysis of bronchial cartilage
in chronic obstructive pulmonary disease and bronchial asthma. Am J Respir Crit
Care Med 1999; 159:1.005-1.013.